Yêu cầu chung
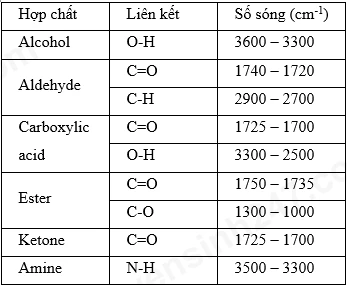
Bảng phổ IR của một số liên kết trong nhóm chức
1
Câu 1
Cho phản ứng thuận nghịch sau: CO(g)+H_2O(g)\xrightleftharpoons {t^\circ} H_2(g)+CO_2(g). Biểu thức hằng số cân bằng của phản ứng là
Cho phản ứng thuận nghịch sau: CO(g)+H_2O(g)\xrightleftharpoons {t^\circ} H_2(g)+CO_2(g). Biểu thức hằng số cân bằng của phản ứng là
K_c=\dfrac{[H_2][CO_2]}{[CO][H_2O]}
K_c=\dfrac{[CO_2][H_2O]}{[H_2][CO]}
K_c=\dfrac{[H_2][CO]}{[CO_2][H_2O]}
K_c=\dfrac{[CO][H_2O]}{[H_2][CO_2]}
Giải thích câu 1
Giải thích chi tiết
😎 Cùng DOL xem qua cách giải câu này nhé!
📃 Thông tin đề bài cho:
Phản ứng thuận nghịch: CO(g) + H_2O(g) \xrightleftharpoons{t^\circ} H_2(g) + CO_2(g)
Yêu cầu: viết biểu thức hằng số cân bằng K_c.
❓ Hiểu câu hỏi:
Với phản ứng tổng quát: aA + bB \rightleftharpoons cC + dD
Biểu thức hằng số cân bằng: K_c = \dfrac{[C]^c [D]^d}{[A]^a [B]^b}
Chỉ xét các chất khí, hệ số cân bằng chính là số mũ.
🔎 Hướng dẫn cách làm:
Áp dụng cho phản ứng đã cho:
Chất sản phẩm: H_2, CO_2
Chất tham gia: CO, H_2O
Các hệ số đều bằng 1
Do đó: K_c = \dfrac{[H_2][CO_2]}{[CO][H_2O]}
✅ Đáp án: K_c=\dfrac{[H_2][CO_2]}{[CO][H_2O]}