1
Câu 1
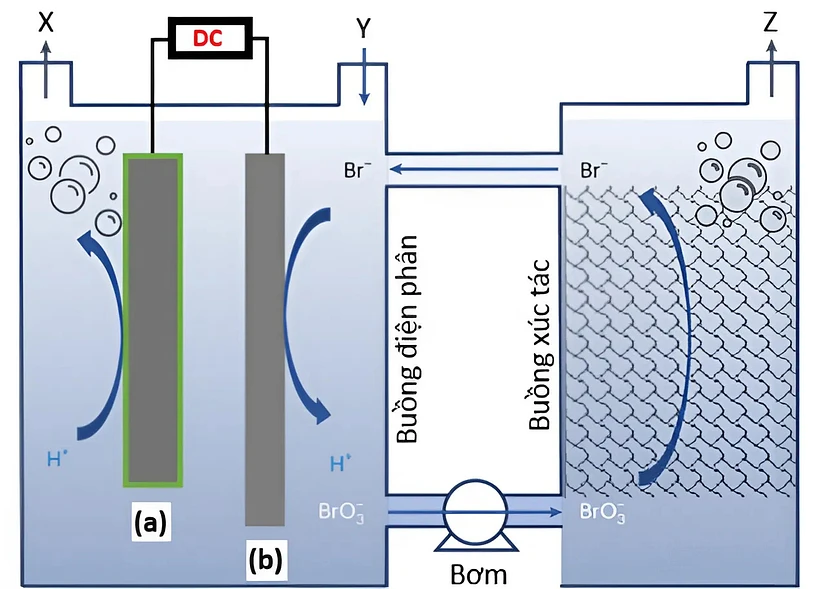
Bằng cách sử dụng điện cực làm bằng Pt được biến tính thông qua các vật liệu khác nhau và chất điện giải NaBr, ta có được một chu trình kết hợp giữa quá trình điện phân và xúc tác để thu được H_2 và O_2 một cách có hiệu quả. Sơ đồ thiết bị được mô tả như hình bên, biết quá trình xảy ra ở điện cực b như sau:
Br^- + 3H_2O \rightarrow BrO_3^- + 6H^+ + 6e^-.
Bằng cách sử dụng điện cực làm bằng Pt được biến tính thông qua các vật liệu khác nhau và chất điện giải NaBr, ta có được một chu trình kết hợp giữa quá trình điện phân và xúc tác để thu được H_2 và O_2 một cách có hiệu quả. Sơ đồ thiết bị được mô tả như hình bên, biết quá trình xảy ra ở điện cực b như sau: Br^- + 3H_2O \rightarrow BrO_3^- + 6H^+ + 6e^-.
Phát biểu
Đúng
Sai
a
Tỉ lệ sản phẩm trong pha xúc tác là n_{Z} : n_{Br} = 3 : 2.
b
Điện cực a mắc vào cực âm của nguồn.
c
hương trình của phản ứng trong bình điện phân của hệ là: Br^- + 3H_2O \rightarrow BrO_3^- + 3H_2.
d
Mục đích của việc thêm Y là bổ sung NaBr.
Giải thích câu 1
Giải thích chi tiết
😎 Cùng DOL xem qua cách giải câu này nhé!
📃 Thông tin đề bài cho:
Buồng xúc tác cho sản phẩm Z là \ce{BrO3^-} và tái sinh Br là \ce{Br^-}.
Đề bài ghi nhận tỉ lệ số mol giữa Z và Br sau pha xúc tác là 3:2.
❓ Hiểu câu hỏi:
Câu khẳng định: “Tỉ lệ sản phẩm trong pha xúc tác là n_Z : n_{Br} = 3 : 2”.
Cần đối chiếu tỉ lệ này với thông tin đã cho.
🔎 Hướng dẫn cách làm:
Buồng điện phân:
Anode: Br^- + 3H_2O → BrO^{3-} + 6H^+ + 6e.
Cathode: 2H^+ + 2e → H_2
Phản ứng: Br^- + 3H_2O → BrO^{3-} + 3H_2.
Buồng xúc tác: 2BrO^{3-} → 2Br^- + 3O_2
X là khíH_2, Y là H_2O, Z là khí O_2.
Xác định Z là ion \ce{BrO3^-}, Br là ion \ce{Br^-} trong buồng xúc tác.
Theo đề bài, sau pha xúc tác tỉ lệ mol giữa hai ion đó đúng là 3:2.
✅ Đáp án: Đúng