Đáp án & giải thích đề môn Hoá k12
Đề chính thức tốt nghiệp THPT môn Hóa Học năm 2025 - Mã đề 0310

DOL THPT
Mar 27, 2026
Đề chính thức tốt nghiệp THPT môn Hóa Học năm 2025 - Mã đề 0310 được thiết kế dưới mô hình thi thử trắc nghiệm online, hỗ trợ bạn hiểu rõ bố cục đề thi. Nền tảng chấm điểm tự động sau khi bạn nộp bài, đồng thời lưu quá trình làm bài để bạn theo dõi hiệu quả lộ trình ôn tập, đi kèm lời giải chi tiết, dễ hiểu và tải file PDF đề thi HOÀN TOÀN MIỄN PHÍ.

Đề chính thức tốt nghiệp THPT môn Hóa Học năm 2025 - Mã đề 0310
Download PDF
Miễn phí dowload
Câu hỏi đề bài
28 Câu hỏi
Phần I
Cho biết nguyên tử khối: H = 1; C = 12; O = 16; Al = 27; S = 32; K = 39; Mn = 55; Fe = 56. Các kí hiệu và chữ viết tắt: s: rắn; l: lỏng; g: khí; aq: dung dịch nước.
Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Phản ứng điều chế ethanol từ ethene theo phương trình hoá học C_2H_4 + H_2O \xrightarrow{H_3PO_4, t^o} C_2H_5OH là phản ứng
hydrogen hoá
hydrate hoá
ester hoá
trùng ngưng
Cho các phát biểu sau về tính chất của ethylamine: (a) Ethylamine làm giấy quỳ tím ẩm hoá đỏ. (b) Ethylamine phản ứng được với HCl trong dung dịch. (c) Ethylamine phản ứng được với dung dịch FeCl_3 ở điều kiện thường. (d) Dung dịch ethylamine phản ứng được với Cu(OH)_2. Số phát biểu đúng là
1
2
3
4
Cho cặp điện cực chuẩn của Ag^+/Ag và Zn^{2+}/Zn lần lượt là E^0 = +0,799 V và E^0 = -0,763 V. Suất điện động chuẩn E_{pin} của pin điện hoá Ag^+/Ag và Zn^{2+}/Zn được tính theo
E_{pin} = E_2^0 - E_1^0
E_{pin} = E_1^0 + E_2^0
E_{pin} = E_1^0 - E_2^0
E_{pin} = -E_2^0 - E_1^0
Cho phản ứng thuận nghịch: 2HI(g) ⇌ H_2(g) + I_2(g). Ở trạng thái cân bằng, nồng độ (mol L⁻¹) của H_2(g), I_2(g), HI(g) được kí hiệu lần lượt là [H_2], [I_2], [HI]. Biểu thức hằng số cân bằng K_C của phản ứng là
K_c = \dfrac{[H_2][I_2]}{[HI]}
K_c = \dfrac{[H_2][I_2]}{[HI]^2}
K_c = \dfrac{[HI]^2}{[H_2][I_2]}
K_c = \dfrac{[HI]}{[H_2][I_2]}
“...(1)... là những hợp chất hữu cơ trong phân tử có nhóm hydroxyl liên kết với nguyên tử carbon no”. Nội dung phù hợp trong chỗ trống (1) là
Phenol
Aldehyde
Alcohol
Ketone
Trong các phân tử hữu cơ thường có sự tạo thành các tiểu phân trung gian hoạt động như gốc tự do, carbanion, carbocation. Carbocation là ion mang điện tích dương trên nguyên tử carbon. Có bao nhiêu carbocation trong số các tiểu phân (CH_3)_3C^+, (CH_3)_2CH^-, CH_3^+ và (CH_3)_2CH^+?
1
4
3
2
Trong phòng thí nghiệm, dung dịch chất nào sau đây phù hợp để kiểm tra sự có mặt của ion Ca^{2+}(aq)?
Na_2CO_3
HCl
NaCl
NaNO_3
Từ phổ khối lượng, phân tử khối của ester X được xác định là 88. Công thức phù hợp với X là
HCOOC_2H_5
C_3H_7COOH
CH_3COOC_2H_5
C_5H_{11}OH
Trong phản ứng tách kim loại Cu từ CuSO_4 theo phương trình hoá học Zn(s) + CuSO_4(aq) \rightarrow ZnSO_4(aq) + Cu(s), phương pháp tách kim loại nào sau đây đã được áp dụng?
Điện phân nóng chảy
Nhiệt luyện
Điện phân dung dịch
Thủy luyện
Trong phức chất, số liên kết σ (sigma) tạo thành giữa một phối tử với nguyên tử trung tâm được gọi là dung lượng phối trí của phối tử đó. Cấu tạo của phức chất [Co(NH_3)_6]^{3+} được cho ở hình bên. Dung lượng phối trí của mỗi phối tử NH_3 trong phức chất đã cho là
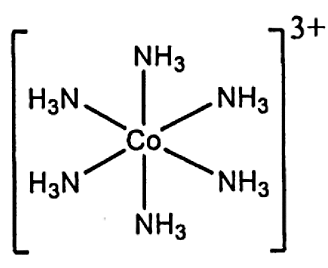
2
6
1
3
Tên gọi theo danh pháp thay thế của chất có công thức cấu tạo CH_3–NH_2 là
ethylamine
methylamine
ethanamine
methanamine
Silicon (Si) là chất bán dẫn quan trọng, được sử dụng rộng rãi trong chế tạo các vi mạch và thiết bị điện tử. Ở trạng thái cơ bản, cấu hình electron của nguyên tử Si (Z = 14) là
1s^2 2s^2 2p^6 3s^3 3p^1
1s^2 2s^2 2p^6 3s^2
1s^2 2s^2 2p^6 3s^23p^2
1s^2 2s^2 2p^6 3s^2 3p^1
Số lượng phối tử trong phức chất [Zn(NH_3)_4]^{2+} là
3
5
4
2
Phát biểu nào sau đây về fructose không đúng?
Fructose thuộc loại monosaccharide
Fructose làm mất màu nước bromine ở điều kiện thường
Fructose có công thức phân tử C_6H_{12}O_6
Fructose phản ứng với Cu(OH)_2 trong môi trường kiềm ở điều kiện thường
Nhiệt độ tạo thành chuẩn \Delta H^o_{f298} của MgCO_3(s), MgO(s), CO_2(g) lần lượt là –602,0 kJ/mol, –1096,0 kJ/mol và –393,5 kJ/mol. Biến thiên enthalpy chuẩn \Delta H^o_{r298} của phản ứng MgO(s) + CO_2(g) \rightarrow MgCO_3(s) là bao nhiêu?
494,0 kJ
100,5 kJ
–100,5 kJ
–494,0 kJ
Ở điều kiện thường, kim loại nào sau đây tồn tại ở thể lỏng?
Au
Zn
Fe
Hg
Question 17 - 18
.Sử dụng thông tin cho dưới đây để trả lời các câu hỏi
Các công trình làm bằng thép (hợp kim của Fe và C) dễ bị ăn mòn điện hóa khi tiếp xúc với nước biển. Một trong số các phương pháp bảo vệ các công trình bằng thép khỏi sự ăn mòn điện hóa là gắn các khối nhôm (aluminium, Al) hoặc kẽm (zinc, Zn) hoặc hợp kim của chúng vào phần chìm dưới nước biển của các công trình đó.
Cho các phát biểu sau về ăn mòn điện hoá và phương pháp bảo vệ đối với các công trình bằng thép: (a) Các khối nhôm hoặc kẽm bảo vệ thép theo phương pháp điện hoá. (b) Khi thép bị ăn mòn điện hoá, sắt trong thép bị oxi hoá. (c) Thép bị ăn mòn điện hoá mà không cần tiếp xúc với dung dịch chất điện li. (d) Khi được bảo vệ bằng phương pháp điện hoá, sắt đóng vai trò là anode nên không bị ăn mòn. Số phát biểu đúng là
2
4
1
3
Cho biết thế điện cực chuẩn của Ca^{2+}/Ca và Fe^{2+}/Fe lần lượt là –2,870 V và –0,440 V. Khi thảo luận về phương pháp bảo vệ các công trình thép nêu trên khỏi sự ăn mòn điện hoá, một học sinh đề xuất: “Có thể sử dụng khối kim loại calciumlcium (calcium) thay thế cho các khối nhôm hoặc kẽm để bảo vệ các công trình bằng thép đó”. Một số nhận định được đưa ra như sau: (1) Có thể sử dụng kim loại calcium vì có tính khử mạnh hơn sắt. (2) Có thể sử dụng calcium vì calcium và nhôm đều có khối lượng riêng nhỏ. (3) Không thể sử dụng calcium do kim loại này dễ phản ứng với nước biển. (4) Không thể sử dụng calcium do kim loại này có tính khử yếu hơn sắt. Nhận định đúng là
nhận định (2)
nhận định (3)
nhận định (1)
nhận định (4)
Phần II
Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Nylon–6,6 là loại tơ có tính dai, bền, ít thấm nước và được sử dụng để dệt vải may mặc. Nylon–6,6 được tổng hợp từ adipic acid và hexamethylenediamine theo phương trình hoá học: nHOOC–[CH_2]_4–COOH+nH_2N–[CH_2]_6–NH_2\xrightarrow{t^o}(–CO–[CH_2]_4–CO–NH–[CH_2]_6–NH–)_n+2nH_2O
Phát biểu
Đúng
Sai
a
Do tơ nylon–6,6 và tơ capron đều có các nhóm –CO–NH– nên hai loại tơ này đều bền với dung dịch kiềm mạnh.
b
Tơ nylon–6,6 là tơ tổng hợp.
c
Phản ứng giữa adipic acid và hexamethylenediamine để tạo nylon–6,6 là phản ứng trùng ngưng.
d
Do tơ nylon–6,6 có các nhóm –CO–NH– nên tơ nylon–6,6 là peptide.
Một nhà máy sản xuất sodium hydroxide (NaOH) và chlorine (Cl_2) bằng phương pháp điện phân dung dịch sodium chloride (NaCl) có màng ngăn với điện cực trơ theo phương trình hóa học: 2NaCl(aq)+2H_2O(l)\xrightarrow{\text{ điện phân, có màng ngăn }}2NaOH(aq)+H_2(g)+Cl_2(g) Sodium hydroxide rắn thu được bằng cách cô dặc rồi hạ nhiệt độ dung dịch chứa NaOH sau điện phân.
Phát biểu
Đúng
Sai
a
Màng ngăn giúp ngăn phản ứng giữa sodium hydroxide và chlorine trong quá trình điện phân.
b
Sodium hydroxide rắn thu được từ dung dịch chứa NaOH bằng phương pháp kết tinh.
c
Trong quá trình điện phân, dung dịch ở khu vực cathode có pH > 7.
d
Tại cathode, khí hydrogen thu được từ phản ứng giữa ion sodium (Na^+) và nước.
Trong phòng thí nghiệm, benzoic acid được điều chế từ toluene theo sơ đồ gồm hai giai đoạn được đánh số (1) và (2) như hình. Trong một thí nghiệm tổng hợp benzoic acid theo sơ đồ trên, từ 2,0 mL toluene (khối lượng riêng bằng 0,867 g/mL) thu được 1,40 gam benzoic acid. Biết KMnO_4 và HCl được lấy dư. Hiệu suất của quá trình tổng hợp benzoic acid từ toluene là h%. Cho biết số sóng hấp thụ đặc trưng của một số liên kết trên phổ hồng ngoại như bảng dưới
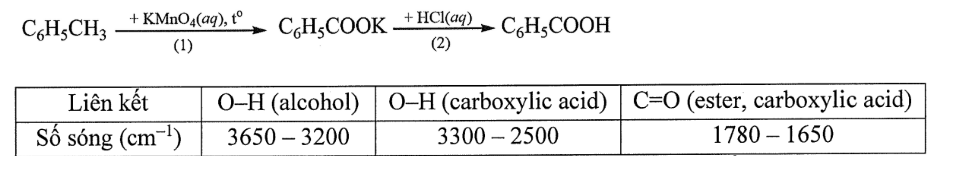
Phát biểu
Đúng
Sai
a
Trong phản ứng với KMnO_4(aq) ở giai đoạn (1), toluene đóng vai trò là chất oxi hóa.
b
Trong phản ứng ở giai đoạn (2), anion C_6H_5COO^- là một base theo thuyết Brønsted–Lowry.
c
Giá trị của hiệu suất là 60,9. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần mười.)
d
Trên phổ hồng ngoại của benzoic acid, tín hiệu (peak) ở 1690 cm⁻¹ đặc trưng cho liên kết O–H
Trong phòng thí nghiệm, một nhóm học sinh tìm hiểu ảnh hưởng của thời gian lưu giữ tới nồng độ FeSO_4 trong dung dịch. Giả thuyết của nhóm học sinh là: “Khi để lâu, nồng độ FeSO_4 trong dung dịch giảm”. Nhóm học sinh chuẩn bị 250,0 mL dung dịch FeSO_4 (nồng độ khoảng 0,1 M) đựng trong bình kín (dán nhãn bình là Y) và tiến hành các thí nghiệm ở hai thời điểm khác nhau như sau:
Ngày thứ nhất: Bước 1: Lấy 10,00 mL dung dịch trong bình Y cho vào bình tam giác rồi thêm tiếp 5 mL dung dịch H_2SO_4 2 M. Bước 2: Chuẩn độ bằng dung dịch KMnO_4 2,20.10^{-2} M đến khi xuất hiện màu hồng nhạt (bền khoảng 20 giây) thì dừng. Ghi lại thể tích dung dịch KMnO_4 đã dùng. Lặp lại thí nghiệm chuẩn độ thêm 2 lần. Thể tích trung bình của dung dịch KMnO_4 sau 3 lần chuẩn độ là 10,70 mL. Nồng độ của Fe(II) xác định được là C_1 M.
Ngày thứ tám: Xác định lại hàm lượng Fe(II) của dung dịch chứa trong bình Y theo các bước tương tự như ngày thứ nhất. Thể tích trung bình của dung dịch KMnO_4 sau 3 lần chuẩn độ là 9,92 mL. Nồng độ của Fe(II) xác định được là C_2 M. Nồng độ dung dịch KMnO_4 như nhau cho các thí nghiệm chuẩn độ. Sự thay đổi nồng độ Fe(II) (q%) được tính theo công thức: q\%=\frac{C₁–C₂}{C₁}\times100\%
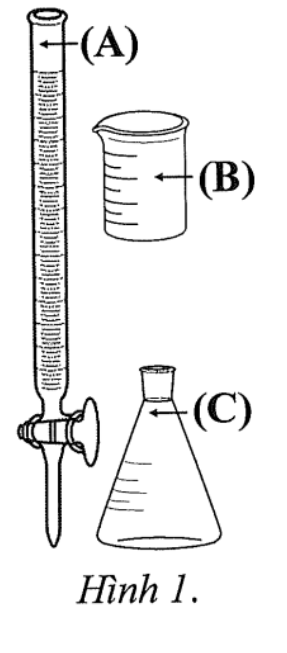
Phát biểu
Đúng
Sai
a
Khi chuẩn độ, dung dịch KMnO_4 được nhỏ trực tiếp vào bình tam giác từ dụng cụ kí hiệu là (B) được minh họa ở hình 1.
b
Kết quả thu được từ các thí nghiệm phù hợp với giả thuyết ban đầu của nhóm học sinh.
c
Giá trị của q là 7,9. (Kết quả có phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần mười.)
d
Giá trị của C_2 là 0,109 M. (Kết quả có phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần trăm.)
Phần III
Thí sinh trả lời từ câu 1 đến câu 6.
Luyện thép từ gang là quá trình làm giảm hàm lượng carbon và một số nguyên tố khác có trong gang. Một nhà máy luyện thép sử dụng loại gang nguyên liệu trong đó carbon chiếm 4,60% về khối lượng, còn lại là sắt (coi làm khô, nguyên tố khác không đáng kể). Khi tiến hành luyện thép, một lượng 2,88 tấn khí oxygen được thổi vào 45,0 tấn gang trong lò luyện nóng chảy để oxi hóa carbon thành CO và CO_2. Hỗn hợp khí thu được có mol CO và CO_2 có số mol bằng nhau. Phần trăm khối lượng carbon trong thép thu được là w%, còn lại là sắt. Coi sắt không bị mất đi trong quá trình luyện thép. Giá trị của w là bao nhiêu? (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần trăm.)
Oleum Z (H_2SO_4·nSO_3) được tạo thành khi cho 100 kg dung dịch H_2SO_4 98% hấp thụ hoàn toàn 30 kg SO_3. Phần trăm khối lượng SO_3 trong Z là b%. Xác định giá trị của b. (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần mười.)
Trong phân tử peptide cho dưới đây có bao nhiêu liên kết peptit?
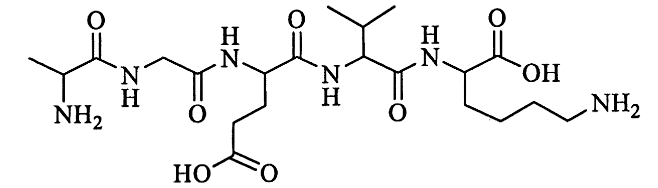
Lượng nhiệt tỏa ra khi đốt cháy hoàn toàn 1 gam nhiên liệu (kí hiệu là Q, tính theo kJ g⁻¹) được sử dụng để đánh giá mức độ “giàu năng lượng” của nhiên liệu đó. Ở điều kiện chuẩn, giả sử Q của ethanol lỏng và một loại khí đốt G lần lượt là Q_E và Q_G. Cho biết: G chứa propane và butane với tỉ lệ mol tương ứng là 1 : 3; nhiệt tỏa thành chuẩn (ΔH⁰_{298}) của các chất được cho trong bảng. Đặt k = \frac{Q_G} {Q_E}, giá trị của k bằng bao nhiêu? (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần trăm.)

Phần trăm khối lượng carbon trong benzene là a%. Giá trị của a là bao nhiêu? (Làm tròn kết quả đến hàng phần mười.)
Có bao nhiêu công thức cấu tạo của aldehyde ứng với công thức phân tử C_5H_{10}O?
Xem đáp án và bài mẫu
Answer key
Phản ứng điều chế ethanol từ ethene theo phương trình hoá học C_2H_4 + H_2O \xrightarrow{H_3PO_4, t^o} C_2H_5OH là phản ứng
hydrogen hoá
hydrate hoá
ester hoá
trùng ngưng
Giải thích câu 1
Giải thích chi tiết
😎 Cùng DOL xem qua cách giải câu này nhé!
📃 Thông tin đề bài cho:
Phương trình phản ứng: \mathrm{C_2H_4 + H_2O \xrightarrow{H_3PO_4,\,t^o} C_2H_5OH}
Chất xúc tác: H_3PO_4
Nhiệt độ cao (t°)
❓ Hiểu câu hỏi:
Câu hỏi yêu cầu xác định loại phản ứng hữu cơ dùng để điều chế ethanol từ ethen.
Cần vận dụng khái niệm về các loại phản ứng:
Hydrate hoá
Hydrogen hoá
Este hoá
Trùng ngưng
🔎 Hướng dẫn cách làm:
Phản ứng hydrate hoá là phản ứng cộng nước (H_2O) vào liên kết đôi C=C của ankene, tạo ra ancol.
Ở đây, ethene (C_2H_4) cộng với H_2O dưới xúc tác axit H_3PO_4 và nhiệt độ cao, sinh ra ethanol (C_2H_5OH).
Kết luận: đây chính là phản ứng hydrate hoá.
✅ Đáp án: hydrate hoá
❌ Các đáp án khác:
A. hydrogen hoá: thêm H_2 chứ không phải H_2O, tạo ankane.
C. este hoá: không hình thành este mà tạo ancol.
D. trùng ngưng: không sinh polymer, chỉ tạo một phân tử ethanol.
Hiện bạn đang luyện đề THPTQG Môn Hoá thuộc chuyên mục luyện thi THPT Quốc gia. Để tiếp tục rèn luyện với nhiều đề thi khác, bạn học có thể luyện tập thêm những đề thi liên quan khác dưới đây.


