Đáp án & giải thích đề môn Hoá k12
Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Long An 2025 - Đề 01

DOL THPT
Mar 27, 2026
Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Long An 2025 - Đề 01 được xây dựng dưới dạng thi thử trắc nghiệm online, hỗ trợ bạn nắm rõ format đề thi. Hệ thống chấm điểm tự động sau khi bạn hoàn thành bài thi, đồng thời lưu kết quả bài làm để bạn theo dõi hiệu quả lộ trình ôn tập, đi kèm đáp án giải thích rõ ràng và download PDF đề thi miễn phí HOÀN TOÀN MIỄN PHÍ.

Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Long An 2025 - Đề 01
Download PDF
Miễn phí dowload
Câu hỏi đề bài
28 Câu hỏi
Phần I
Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Chất nào dưới đây là ester?
CH_3-COO-CH_3
C_2H_5-COOH
CH_3-CO-C_2H_5
CH_3-CH_2OH
“Chất béo là các triester (ester ba chức) của …(1)… và các …(2)… , gọi chung là các triglyceride.” Nội dung phù hợp với các phần còn trống (1), (2) lần lượt là
glycerol, acid béo
glycerol, carboxylic acid
glucose, acid béo
glucose, carboxylic acid
Công thức phân tử của maltose là
C_{12}H_{22}O_{11}
C_6H_{12}O_6
C_6H_{10}O_5
C_{12}H_{24}O_{12}
Chất nào dưới đây là amine bậc một?
CH_3-CH_2-OH
CH_3-NH-CH_3
CH_3-CH_2-NH_2
CH_3-O-CH_3
Peptide mạch hở X được biểu diễn bằng công thức Ala-Gly-Val-Ala. Cho các phát biểu sau: (a) X là tetrapeptide. (b) Trong phân tử X có 4 liên kết peptide. (c) X không bị thuỷ phân trong môi trường acid. (d) X phản ứng được với Cu(OH)_2 tạo màu tím buiret. Số phát biểu đúng là
3
2
1
4
Ở pH = 6, các amino acid: glycine, alanine, glutamic acid và lysine chủ yếu tồn tại ở dạng như hình bên dưới. Đặt một điện trường vào mỗi dung dịch có pH = 6 chứa một trong các amino acid trên. Cho các nhận định sau: (a) Glycine di chuyển về phía điện cực dương. (b) Alanine hầu như không di chuyển về các điện cực. (c) Glutamic acid di chuyển về phía điện cực âm. (d) Lysine di chuyển về phía điện cực dương. Trong các nhận định trên, có bao nhiêu nhận định đúng?
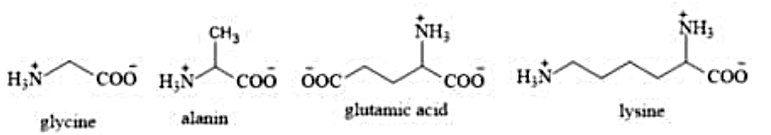
4
2
3
1
Poly(vinyl chloride) được điều chế bằng phản ứng trùng hợp monomer nào dưới đây?
CH_2=CH-Cl
CH_2=CCl-CH=CH_2
CH_2=CH-CH_3
CH_2=CH_2
Ở điều kiện chuẩn, dãy nào dưới đây sắp xếp theo chiều giảm dần tính khử của kim loại?
Ag, Fe, Cu
Fe, Ag, Cu
Ag, Cu, Fe
Fe, Cu, Ag
Ở điều kiện chuẩn, kim loại nào dưới đây không khử được ion H^+ trong dung dịch HCl?
Zn
Fe
Cu
Mg
Dây chảy, thường làm bằng chì (lead, kí hiệu Pb), là một chi tiết trong cầu chì... Khi có sự cố xảy ra làm tăng nhiệt độ, dây chảy bị đứt và ngăn dòng điện, bảo vệ các thiết bị điện. Kim loại chì (lead) được sử dụng làm dây chảy trong cầu chì chủ yếu là do tính chất nào dưới đây?
Nhiệt độ nóng chảy tương đối thấp.
Khối lượng riêng tương đối nhỏ.
Độ cứng tương đối thấp.
Độ dẫn điện tương đối thấp.
Trong công nghiệp, để tách kim loại Al khỏi hợp chất Al_2O_3 thì cần sử dụng phương pháp nào dưới đây?
Điện phân dung dịch AlCl_3.
Điện phân Al_2O_3 nóng chảy.
Nung Al_2O_3 với khí CO ở 600^\circ C.
Cho kim loại Na tác dụng với dung dịch AlCl_3.
Nguyên tố Na thuộc nhóm IA. Kim loại Na được bảo quản bằng cách ngâm trong chất lỏng nào dưới đây?
Ethanol.
Nước cất.
Dầu hoả.
Acetic acid.
Đá vôi có thành phần chính là CaCO_3. Tên gọi của CaCO_3 là gì?
Sodium carbonate.
Calcium carbonate.
Calcium sulfate.
Sodium sulfate.
Phương pháp nào dưới đây không làm mềm được nước có tính cứng tạm thời?
Dùng vừa đủ dung dịch HCl.
Đun sôi.
Dùng vừa đủ Ca(OH)_2.
Dùng vừa đủ Na_2CO_3.
Kết quả phân tích phổ khối lượng (MS) của một hydrocarbon X cho biết phân tử khối của nó là 58. X có công thức phân tử là
C_5H_8
C_6H_6
C_3H_8
C_4H_{10}
Propene tác dụng với dung dịch HBr tạo ra hai dẫn xuất bromo là CH_3–CHBr–CH_3 (sản phẩm chính) và CH_3–CH_2–CH_2Br (rất ít). Giai đoạn (1) trong cơ chế phản ứng này có sự tạo thành các tiểu phân trung gian là carbocation I và carbocation II như sau: CH_3–CH=CH_2 + H^+ \leftrightarrow CH_3–\overset{+}{C}H–CH_3 (carbocation I) CH_3–CH=CH_2 + H^+ \leftrightarrow CH_3–CH_2–\overset{+}{C}H_2 (carbocation II). Trong giai đoạn (1) này, CH_3–CH=CH_2 là chất phản ứng, H^+ là tác nhân. Ở giai đoạn (2), ion Br^- sẽ kết hợp với các tiểu phân trung gian tạo thành sản phẩm.
Trong giai đoạn (1), khi phân cắt liên kết \pi, cặp electron được chia đều cho mỗi nguyên tử carbon.
Ở giai đoạn (2), Br^- chỉ kết hợp với carbocation I mà không kết hợp được với carbocation II.
Ion H^+ là tác nhân giàu electron, có khả năng nhường electron cho liên kết \pi.
Carbocation I bền hơn carbocation II.
Điểm chớp cháy là nhiệt độ thấp nhất mà một chất lỏng hoặc vật liệu dễ bay hơi tạo thành lượng hơi đủ để bốc cháy trong không khí khi tiếp xúc nguồn lửa. Chất lỏng có điểm chớp cháy nhỏ hơn 37,8°C là chất lỏng dễ cháy. Nhiệt độ tự bốc cháy là nhiệt độ mà tại đó chất cháy tự bốc cháy mà không cần nguồn lửa. Nhiệt độ ngọn lửa là nhiệt độ cao nhất có thể tạo ra bởi chất cháy. Áp suất đều bằng áp suất khí quyển. Hexane là chất lỏng (khối lượng riêng 0,66 g/cm³) nhẹ hơn nước. Hexane có điểm chớp cháy là –22°C, nhiệt độ tự bốc cháy là 259°C và nhiệt độ ngọn lửa là 2040°C. Cho các phát biểu dưới đây (ở áp suất khí quyển): (a) Hexane là chất lỏng dễ cháy. (b) Ở 100°C, hexane tự bốc cháy mà không cần nguồn lửa. (c) Có thể dùng hexane để nấu chảy chì (lead, nhiệt độ nóng chảy là 328°C). (d) Khi xảy ra đám cháy với lượng lớn hexane nên dùng H₂O để dập tắt. Trong các phát biểu trên, có bao nhiêu phát biểu đúng?
2
3
1
4
Đối với vùng đất phèn có pH thấp, khi trồng trọt không nên bón loại phân đạm nào dưới đây để tránh làm đất chua hơn?
KNO_3.
(NH_2)_2CO.
(NH_4)_2SO_4.
(NH_4)_2HPO_4.
Phần II
Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Một nhóm học sinh làm thí nghiệm để nghiên cứu sự phụ thuộc của thế điện cực vào nồng độ của ion kim loại. Giả thuyết mà nhóm học sinh này đặt ra là: "khi giảm nồng độ ion kim loại trong dung dịch thì thế điện cực cũng giảm". Để kiểm chứng giả thuyết trên, nhóm học sinh tiến hành thí nghiệm như sau: – Bước 1: chuẩn bị 5 cốc chứa dung dịch CuSO_4 1M; 5 cốc chứa dung dịch ZnSO_4 có nồng độ lần lượt là 1M; 0,5M; 0,1M; 0,05M; 0,01M; Các thanh điện cực Zn và Cu có kích thước như nhau; cầu muối; điện kế để đo sức điện động. – Bước 2: Tiến hành lắp các dụng cụ theo sơ đồ như hình vẽ bên dưới. – Bước 3: Lần lượt thay các cốc chứa ZnSO_4 có nồng độ khác nhau, tiến hành đo sức điện động của pin. Kết quả thí nghiệm được học sinh thu thập được theo bảng dưới.
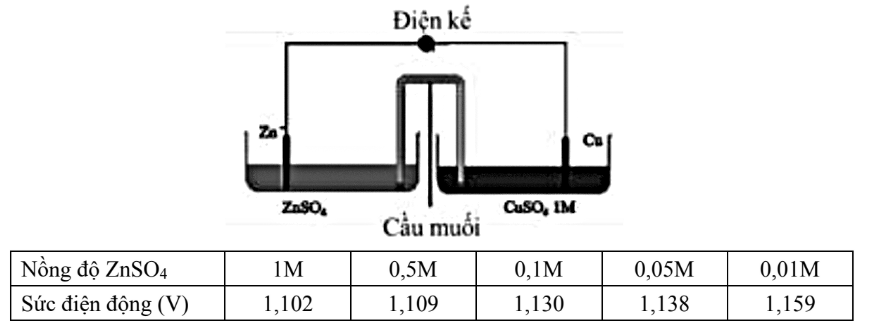
Phát biểu
Đúng
Sai
a
Trong thí nghiệm trên, Zn là anode còn Cu là cathode.
b
Cần phải đồng thời thay đổi cả nồng độ ZnSO_4 và CuSO_4 mới kiểm định được giả thuyết.
c
Từ kết quả thí nghiệm, tính được thế điện cực của Zn^{2+}/Zn khi nồng độ Zn^{2+} bằng 0,01M là –0,819V.
d
Dựa vào kết quả thí nghiệm, có thể kết luận khi giảm nồng độ ion kim loại thì thế điện cực tăng.
Khi có mặt enzyme lactococcus lactis, glucose lên men thành lactic acid theo phương trình hoá học: C_6H_{12}O_6 ⟶ 2CH_3–CH(OH)–COOH. Để nghiên cứu sự phụ thuộc của phản ứng lên men lactic bằng enzyme lactococcus lactis vào pH của môi trường, một nhóm học sinh nêu giả thuyết như sau: "nếu pH của môi trường càng cao thì hiệu suất phản ứng lên men lactic glucose bằng enzyme lactococcus lactis càng cao." Từ đó nhóm học sinh tiến hành thí nghiệm như sau: – Bước 1: Chuẩn bị 5 cốc chứa 50 mL dung dịch glucose 10%, thêm hoá chất để ổn định pH của mỗi cốc lần lượt bằng 4, 5, 6, 7, 8. Hấp ở 110°C trong thời gian 20 phút để khử trùng môi trường rồi để nguội. – Bước 2: Thêm vào mỗi cốc một lượng bằng nhau enzyme lactococcus lactis, đậy kín, để trong tủ ấm 48 giờ ở nhiệt độ 37°C. – Bước 3: Phân tích mẫu (bằng phương pháp thích hợp) để xác định hiệu suất. Nhóm học sinh ghi lại được biểu đồ liên quan giữa pH và hiệu suất phản ứng như hình bên dưới.
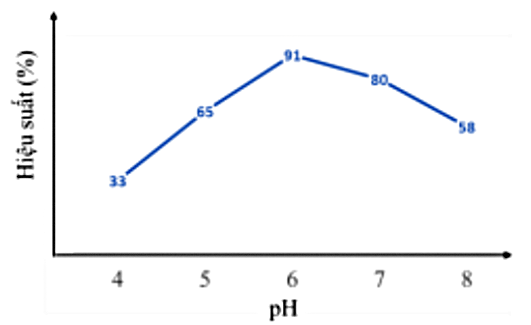
Phát biểu
Đúng
Sai
a
Nếu dùng enzyme khác, glucose có thể lên men tạo thành các sản phẩm khác.
b
Lactic acid và glucose đều thuộc loại carbohydrate.
c
Kết quả thí nghiệm chứng minh giả thuyết của nhóm học sinh là đúng.
d
Trong các môi trường pH đã thử nghiệm, hiệu suất phản ứng đạt cao nhất ở pH=6.
Poly(ethylene terephtalate) (hay còn gọi là PET) là một loại polymer có nhiều ứng dụng trong công nghiệp và đời sống như làm vỏ chai, hộp, vải may quần áo, rèm cửa, vỏ máy móc, linh kiện điện tử, ... PET được điều chế từ terephtalic acid và ethylene glycol theo phản ứng:
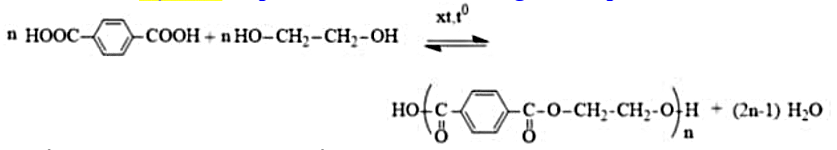
Phát biểu
Đúng
Sai
a
Các mắt xích trong phân tử PET liên kết với nhau bởi nhóm chức ester.
b
Mỗi phân tử PET có phân tử khối là 194.
c
Phản ứng điều chế PET từ terephtalic acid và ethylene glycol là phản ứng trùng ngưng.
d
PET bền cả trong môi trường acid mạnh lẫn môi trường base mạnh.
Nguyên tố copper (Cu) có cấu hình electron nguyên tử là [Ar]3d^{10}4s^{1}. Trong tự nhiên có nhiều dạng khoáng của copper như malachite (CuCO_3.Cu(OH)_2), chalcocit (Cu_2S), … Nước Schweizer có khả năng hoà tan cellulose được điều chế từ CuSO_4 và dung dịch NH_3 theo các phản ứng sau: CuSO_4 + 2NH_3 + 2H_2O → Cu(OH)_2 + (NH_4)_2SO_4; Cu(OH)_2 + 4NH_3 + 2H_2O → [Cu(NH_3)_4(H_2O)_2](OH)_2. Cu(OH)_2 là chất rắn, màu xanh, không tan trong nước, còn [Cu(NH_3)_4(H_2O)_2](OH)_2 tồn tại trong dung dịch dưới dạng ion[Cu(NH_3)_4(H_2O)_2]^{2+} và ion OH^{-}.
Phát biểu
Đúng
Sai
a
Copper là nguyên tố kim loại dãy chuyển tiếp thứ nhất.
b
Trong các hợp chất, copper chỉ thể hiện mức oxi hoá +2.
c
Nước Schweizer chứa phức của Cu^{2+} với các phối tử là NH_3 và OH^-.
d
Khi cho từ từ NH_3 vào dung dịch CuSO_4 thì ban đầu có kết tủa màu xanh, sau đó kết tủa tan khi NH_3 dư.
Phần III
Thí sinh trả lời từ câu 1 đến câu 6.
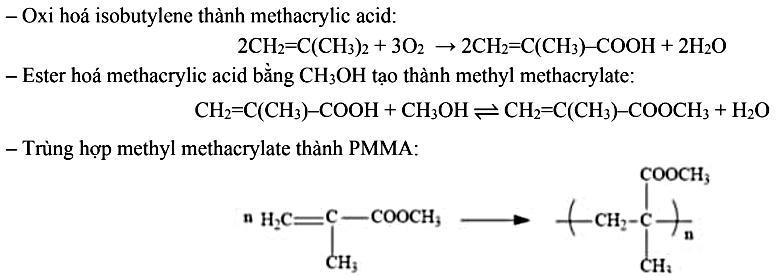
Poly(methylmethacrylate) (viết tắt PMMA ‒ còn gọi là plexiglass hay thủy tinh hữu cơ) là một loại vật liệu polymer được ứng dụng sản xuất kính ô tô, thiết bị y tế, đèn LED, … Quy trình hiện đại để sản xuất PMMA từ isobutylene (với các điều kiện thích hợp) như hình. Hiệu suất toàn bộ quá trình điều chế là 70% (tính theo isobutylene). Để sản xuất 1,5 tấn PMMA thì cần dùng m kg isobutylene. Tính giá trị của m (lấy đến hàng đơn vị).
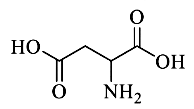
Aspartic acid là một α-amino acid thiên nhiên có công thức cấu tạo như bên dưới. Hãy tính khối lượng mol (gam/mol) của aspartic acid.
Cho các mệnh đề được đánh số thứ tự như sau: (1) Khi đặt một hiệu điện thế vào hai đầu kim loại, các electron hoá trị tự do sẽ chuyển động thành dòng có hướng từ cực âm đến cực dương. (2) Các cation trong tinh thể kim loại có thể trượt lên nhau mà không tách rời nhau do lực hút tĩnh điện giữa chúng với các electron hoá trị tự do. (3) Các electron hoá trị tự do trong tinh thể kim loại phản xạ hầu hết những tia sáng mà mắt con người nhìn thấy được. (4) Các electron ở vùng có nhiệt độ cao có động năng lớn sẽ di chuyển đến vùng có nhiệt độ thấp hơn trong tinh thể kim loại và truyền năng lượng cho các cation ở vùng này. Hãy gán số thứ tự của các mệnh đề trên tương ứng với nguyên nhân gây ra lần lượt các tính chất: tính dẻo, tính dẫn điện, tính dẫn nhiệt, ánh kim của kim loại theo trình tự thành dãy bốn số (Ví dụ 4231).
Tổng số đồng phân cấu tạo ester có công thức phân tử C_{5}H_{10}O_{2} là bao nhiêu?
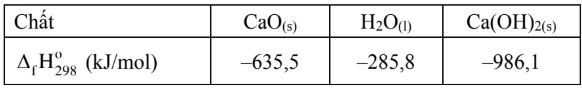
Túi gia nhiệt của lẩu tự sôi có thành phần là hỗn hợp gồm CaO, Mg, Al, Fe, NaCl. Khi đổ nước vào khay có túi gia nhiệt, CaO phản ứng nhanh và tỏa ra một lượng nhiệt lớn làm cho nước lẩu sôi. Phương trình phản ứng hoá học của CaO với H_{2}O như sau: CaO_{(s)}+H_{2}O_{(l)}\to Ca(OH)_{2(s)}. 90% nhiệt sinh ra do phản ứng trên dùng để đun sôi nước. Các kim loại Mg, Al, Fe cũng phản ứng chậm với nước và tỏa nhiệt để duy trì nhiệt độ của phần nước lẩu. Cho bảng giá trị enthalpy tạo thành chuẩn của các chất sau. Biết rằng để tăng nhiệt độ của 1 L nước lỏng lên 1 °C cần cung cấp năng lượng 4,18 kJ. Một túi gia nhiệt của gói lẩu tự sôi chứa 84 gam CaO thì đun được tối đa V L nước từ 25 °C lên 100 °C. Tính giá trị của V (làm tròn đến hàng phần trăm).
Hàm lượng sắt (iron) trong nước là số miligam nguyên tố sắt có trong 1 lít nước, đơn vị tính là mg/L. Để xác định hàm lượng sắt trong một mẫu nước giếng, một nhóm học sinh tiến hành thí nghiệm sau: – Bước 1: Lấy 200 mL mẫu nước vào bình tam giác, thêm 1 mL dung dịch H_{2}SO_{4} 1 M rồi dẫn dư khí SO_{2} qua dung dịch hỗn hợp để khử toàn bộ Fe^{3+} thành Fe^{2+} theo phản ứng: 2Fe^{3+}+SO_{2}+2H_{2}O\to2Fe^{2+}+H_{2}SO_{4}. – Bước 2: Đun nhẹ bình chứa dung dịch mẫu ở 60 °C để đuổi hết khí SO_{2} dư. – Bước 3: Chuẩn độ 25,00 mL dung dịch mẫu bằng dung dịch KMnO_{4} 0,02 M. Sau 5 lần chuẩn độ, thể tích trung bình KMnO_{4} là 8,00 mL. Hãy tính hàm lượng của sắt (mg/L) trong mẫu nước giếng (lấy đến hàng đơn vị).
Xem đáp án và bài mẫu
Answer key
Chất nào dưới đây là ester?
CH_3-COO-CH_3
C_2H_5-COOH
CH_3-CO-C_2H_5
CH_3-CH_2OH
Giải thích câu 1
Giải thích chi tiết
😎 Cùng DOL xem qua cách giải câu này nhé!
📃 Thông tin đề bài cho:
Chuyên đề: Hợp chất hữu cơ (este, axit, xeton, ancol)
Các công thức của 4 chất cần lựa chọn (theo hình ảnh đính kèm):
A: CH_3-COO-CH_3
B: C_2H_5-COOH
C: CH_3-CO-C_2H_5
D: CH_3-CH_2OH
❓ Hiểu câu hỏi:
Câu hỏi yêu cầu xác định chất nào trong danh sách là este.
Nhóm chức đặc trưng của este có cấu trúc chung: R-COO-R'
🔎 Hướng dẫn cách làm:
Quan sát công thức mỗi lựa chọn và tìm nhóm chức: • A: CH_3-COO-CH_3 → có nhóm -COO- nối giữa hai gốc → thỏa nhóm chức este. • B: C_2H_5-COOH → có nhóm -COOH → axit cacboxylic, không phải este. • C: CH_3-CO-C_2H_5 → có nhóm -CO- → xeton, không phải este. • D: CH_3-CH_2OH → có nhóm -OH → ancol, không phải este.
Chỉ có A chứa đúng nhóm chức -COO- của este.
✅ Đáp án: CH_3-COO-CH_3
Hiện bạn đang luyện đề THPTQG Môn Hoá thuộc chuyên mục luyện thi THPT Quốc gia. Để tiếp tục rèn luyện với nhiều đề thi khác, bạn có thể luyện tập thêm những đề thi liên quan trực tiếp khác bên dưới.


