Đáp án & giải thích đề môn Hoá k12
Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Nghệ An 2025 - Đề 06

DOL THPT
Mar 27, 2026
Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Nghệ An 2025 - Đề 06 được thiết kế dưới hình thức thi thử trắc nghiệm online, giúp người học nắm rõ bố cục đề thi. Hệ thống chấm điểm ngay sau khi bạn làm xong bài, đồng thời lưu quá trình làm bài để bạn dễ theo dõi lộ trình ôn tập, đi kèm đáp án giải thích rõ ràng và tải file PDF đề thi HOÀN TOÀN MIỄN PHÍ.

Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Nghệ An 2025 - Đề 06
Download PDF
Miễn phí dowload
Câu hỏi đề bài
28 Câu hỏi
Phần I
Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Nguyên tố potassium (K) có số hiệu nguyên tử là 19. Ở trạng thái cơ bản, cấu hình electron của nguyên tử K là:
[Ar]4s^{1}
[Kr]4s^{2}
[Ar]4s^{2}
[Kr]4s^{1}
Cao su tự nhiên có tính đàn hồi, không dẫn điện, chịu mài mòn, không thấm khí và nước, không tan trong nước và một số dung môi hữu cơ như ethanol, nhưng tan trong xăng, benzen,... Do có liên kết đôi trong phân tử polymer nên cao su tự nhiên có thể tham gia các phản ứng cộng với H_2, HCl, Cl_2,... Khi cho cao su tác dụng với lưu huỳnh thu được cao su lưu hóa, có cấu trúc mạng lưới không gian. Cho các phát biểu sau: (a) Cao su tự nhiên được điều chế từ phản ứng trùng hợp isoprene C_5H_8. (b) Cao su lưu hóa có mạch mạng lưới không gian. (c) Phản ứng lưu hóa cao su thuộc loại phản ứng tăng mạch polymer. (d) Phản ứng cộng HCl vào cao su tự nhiên thuộc loại phản ứng tăng mạch polymer. Các phát biểu đúng là:
(a), (b), (d)
(a), (b), (c)
(b), (c)
(a), (b), (c)
Cho bảng giá trị thế điện cực chuẩn của các cặp oxi hóa – khử như dưới. Sức điện động chuẩn lớn nhất của pin Galvani thiết lập từ hai cặp oxi hóa – khử trong số các cặp trên là:

1{,}56\ \text{V}
2{,}48\ \text{V}
1{,}60\ \text{V}
1{,}24\ \text{V}
Polypropylene là chất dẻo được sử dụng phổ biến thứ 2 sau polyethylene. Trùng hợp chất nào sau đây thu được Polypropylene?
CH_2{=}CH_2
CH_2{=}CH{-}C_6H_5
CH_2{=}CH{-}Cl
CH_2{=}CH{-}CH_3
Nguyên tắc tách kim loại ra khỏi hợp chất của chúng là:
Khử ion kim loại trong hợp chất thành nguyên tử.
Dựa trên tính chất của kim loại như tỉ trọng, khối lượng riêng lớn để tách.
Oxi hóa ion kim loại trong hợp chất thành nguyên tử.
Hòa tan các khoáng vật có trong quặng để thu được kim loại.
Câu ca dao “Lúc chiêm lấp ló đầu bờ. He nghe tiếng sấm phất cờ mà lên” phản ánh hiện tượng gì trong hóa học liên quan đến sự phát triển của cây lúa?
Tiếng sấm là tín hiệu báo mùa mưa, tạo điều kiện cho cây lúa phát triển nhanh.
Mưa đầu mùa làm tăng độ ẩm trong đất, thúc đẩy sự phát triển.
Nước mưa giúp rửa mặn cho đất, thúc đẩy sự phát triển của cây.
Nước mưa sau sấm sét làm đất giàu nitrat, thúc đẩy sự sinh trưởng của cây lúa.
Cho các hợp chất có công thức cấu tạo như hình dưới. Những hợp chất nào trong số các chất trên thuộc loại \alpha-amino acid?
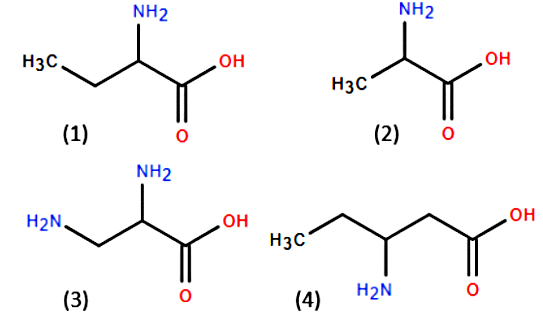
Chất (1) và chất (3).
Chất (2), chất (3) và chất (4).
Chất (1) và chất (2).
Chất (1), chất (2) và chất (3).
Phản ứng giữa HCl với ethylene: CH_2{=}CH_2 + HCl \rightarrow CH_3CH_2Cl. Cơ chế phản ứng qua 2 giai đoạn như sau: Giai đoạn 1 xảy ra chậm, quyết định tốc độ phản ứng. Nhận định nào sau đây không đúng?
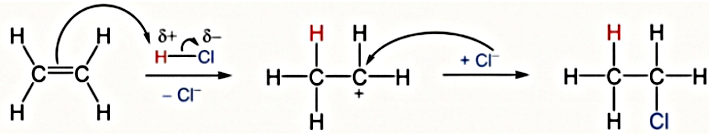
Trong phân tử ethylene có 5 liên kết \sigma (xích ma).
Phản ứng trên thuộc loại phản ứng cộng.
Trong dãy đồng đẳng alkene, ethylene tham gia phản ứng cộng HCl dễ nhất.
Trong giai đoạn 1 của phản ứng trên có sự phân cắt liên kết \pi.
Kim loại tungsten (W) được sử dụng làm dây tóc bóng đèn. Ứng dụng này dựa trên cơ sở tính chất vật lí nào sau đây của tungsten?
Nhiệt độ nóng chảy cao
Tính dẫn nhiệt
Tính dẻo
Tỉ trọng nhnhỏ
Nước Javel là sản phẩm của quá trình:
Sục khí chlorine vào vôi sữa.
Điện phân dung dịch NaCl không màng ngăn giữa hai điện cực.
Điện phân dung dịch NaCl có màng ngăn giữa hai điện cực.
Điện phân dung dịch NaCl không màng ngăn.
Cho đồ thị sau về sự thay đổi nồng độ glucose trong máu sau khi uống đồ uống có đường. Khi sử dụng đồ uống có đường, nồng độ glucose trong máu tăng cao nhất sau khi:
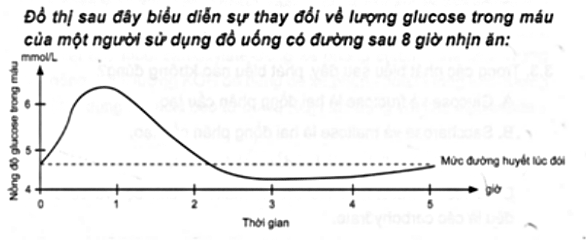
Sử dụng khoảng 20 phút.
Sử dụng khoảng 2 giờ.
Sử dụng khoảng 50 phút.
Sử dụng khoảng 3 giờ.
Cho bảng giá trị thế điện cực chuẩn của các cặp oxi hóa – khử như dưới. Trong số các ion kim loại gồm \text{Fe}^{2+}, \text{Cu}^{2+}, \text{Al}^{3+}, \text{Zn}^{2+}; ở điều kiện chuẩn ion nào có tính oxi hóa yếu hơn \text{Ag}^{+}, nhưng mạnh hơn \text{Pb}^{2+}?
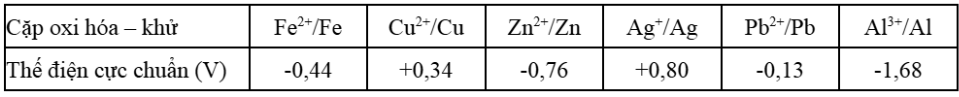
\text{Cu}^{2+}
\text{Zn}^{2+}
\text{Fe}^{2+},\text{ Cu}^{2+},\text{ Zn}^{2+}
\text{Fe}^{2+},\text{ Cu}^{2+}
Ester nào sau đây được tạo thành từ acetic acid và ethanol?
Ethyl acetate
Propyl acetate
Methyl acetate
Isopropyl acetate
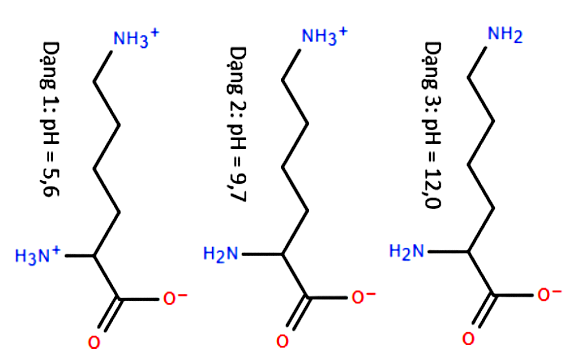
Lysine là một trong những amino acid thiết yếu đối với cơ thể người. Với mỗi môi trường có giá trị pH bằng 5,6; 9,7; 12,0, ion lysine tồn tại ở dạng như hình dưới. Trong quá trình điện di, ion sẽ di chuyển về phía điện cực trái dấu với ion. Cho các nhận định sau về quá trình điện di của lysine: (a) Với môi trường pH = 9{,}7 thì dạng (II) hầu như không dịch chuyển về các điện cực. (b) Với môi trường pH = 5{,}6 thì dạng (I) di chuyển về phía cực âm. (c) Với môi trường pH = 12{,}0 thì dạng (III) di chuyển về phía cực dương. (d) Với môi trường pH = 9{,}7 thì dạng (II) di chuyển về phía cực âm. Các nhận định đúng là:
(a), (b), (d)
(a), (c), (d)
(a), (b), (c)
(b), (c), (d)
Hợp chất nào sau đây chứa nhóm chức amino (-NH_2)?
Aniline
Benzen
Glucose
Acetic acid
Kim loại nào sau đây phản ứng dung dịch CuSO_4, dựa vào tính khử tạo thành 2 chất kết tủa?
Ba
Fe
Na
Zn
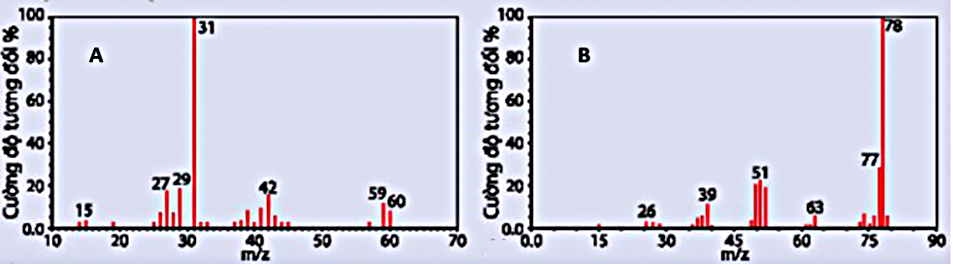
Phổ khối lượng (MS) là phương pháp điện đại để xác định phân tử khối của các hợp chất hữu cơ. Hai chất (A), (B) có công thức phân tử không theo thứ tự là C_3H_6 và C_3H_6O. Cho biết hình ảnh phổ khối lượng như hình. Kết luận nào sau đây đúng?
(A) và (B) thuộc cùng dãy đồng đẳng.
(B) thuộc loại hợp chất hữu cơ có nhóm chức.
(A) là C_3H_6, (B) là C_3H_6O.
(A) là C_3H_6O, (B) là C_3H_6.
Ester có công thức CH_3COOCH_3 có tên gọi là:
Methyl formate
Methyl methanoate
Methyl propionate
Methyl acetate
Phần II
Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Aspirin (hay acetylsalicylic acid) là một dẫn xuất của salicylic acid được sử dụng để hạ sốt và giảm đau nhẹ đến trung bình do tình trạng đau nhức cơ, răng, cảm lạnh, đau đầu và viêm khớp. Một nhóm học sinh thực hiện tổng hợp aspirin trong phòng thí nghiệm như sau:
Bước 1: Cho 75,0 gam salicylic acid khan và 105,0 mL acetic anhydride (d = 1,08 g/mL) vào bình cầu 250 mL; thêm 4,0 mL sulfuric acid đặc và lắc kĩ. Sau đó, khuấy hỗn hợp phản ứng ở 50{-}60^\circ C trong khoảng 45 phút cho đến khi tan hết phản chất rắn.
Bước 2: Dùng nước đá để làm lạnh hỗn hợp phản ứng đến nhiệt độ nhỏ hơn 10^\circ C. Cho hỗn hợp vào cốc lớn, thêm từ từ 750 mL nước cất và khuấy kĩ, aspirin sẽ kết tinh. Lọc lấy sản phẩm bằng phễu lọc Buchner.
Bước 3: Hòa tan aspirin thô trong 100 mL ethanol 90°, đun nóng đến tan hoàn toàn, sau đó đổ dung dịch này từ từ vào 450 mL nước nóng khoảng 50^\circ C, đun nóng nhẹ cho chất rắn tan hết. Để nguội dung dịch thu được đến nhiệt độ phòng. Aspirin kết tinh dưới dạng tinh thể, lọc và rửa hết nước, sấy khô ở 50^\circ C.
Bước 4: Cân sản phẩm thu được 83,1 gam aspirin.
Biết phương trình hóa học điều chế aspirin từ salicylic acid được biểu diễn như sau:
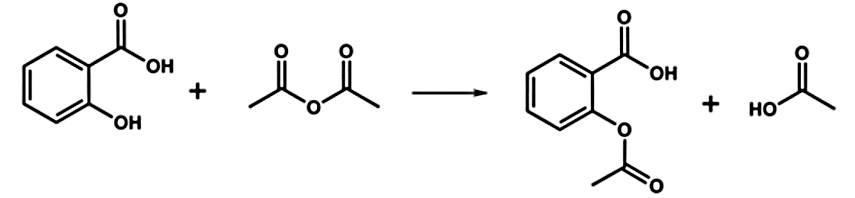
Phát biểu
Đúng
Sai
a
Phương pháp tách và tinh chế aspirin ở trên là phương pháp kết tinh.
b
Aspirin tan trong nước nhiều hơn salicylic acid.
c
Hiệu suất quá trình tổng hợp aspirin ở thí nghiệm trên đạt khoảng 85%.
d
Aspirin là hợp chất hữu cơ tạp chức, trong đó có chức ester và chức phenol.
Một nhóm học sinh tiến hành mạ đồng (copper) cho một chiếc chìa khóa bằng hợp kim Fe-Zn. Quá trình tiến hành được thực hiện như sau:
Cho vào cốc thủy tinh 200 mL dung dịch CuSO_4 1M.
Nhúng 1 lá đồng vào dung dịch và nối với cực dương của nguồn điện 1 chiều.
Nhúng chìa khóa chìm trong dung dịch và nối với cực âm của nguồn điện.
Phát biểu
Đúng
Sai
a
Khối lượng dung dịch trong cốc không đổi trong quá trình phản ứng (coi nước bay hơi không đáng kể).
b
Nếu không nối chìa khóa với nguồn điện thì trên bề mặt chìa khóa vẫn có lớp kim loại màu đỏ bám vào.
c
Chiếc chìa khóa đóng vai trò là anode.
d
Màu xanh của dung dịch trong cốc nhạt dần.
Một nhóm học sinh tiến hành dự án nấu rượu truyền thống bằng cách lên men tinh bột, nhằm kiểm tra giả thuyết “sau khi thủy phân, lên men, chưng cất sẽ thu được rượu chỉ chứa C_2H_5OH và H_2O”. Tinh bột từ gạo nếp sau khi nấu cơm, ủ lên men, thêm nước đủ ngày, sau đó chưng cất thu được rượu 30°. Trong quá trình chưng cất, chất lỏng ban đầu thu được có vị rất nóng, sau đó nhạt dần và cuối cùng có vị chua.
Phát biểu
Đúng
Sai
a
Do rượu có vị chua nên giả thuyết của nhóm học sinh là sai.
b
Từ 20 kg gạo nếp (chứa 48,6% tinh bột) nhóm học sinh chưng cất được 18,4 Lít rượu 30° (biết khối lượng riêng C_2H_5OH là 0,8 g/mL, hiệu suất quá trình sản xuất là 80%).
c
Tinh bột thuộc loại polysaccharide.
d
Để rượu ngon, khi chưng cất ta nên bỏ đi 100–200 mL chất lỏng chảy ra đầu tiên.
Tiến hành thí nghiệm theo các bước sau: Bước 1: Cho vào 3 ống nghiệm, mỗi ống 2 mL dung dịch H_2SO_4 0,5 M. Bước 2: Cho 3 lá kim loại có kích thước như nhau đã làm sạch bề mặt gồm lá Zn (ống 1), Fe (ống 2), Mg (ống 3). Biết: E^\circ_{\text{Zn}^{2+}/\text{Zn}} = -0{,}762\ \text{V} E^\circ_{\text{Fe}^{2+}/\text{Fe}} = -0{,}44\ \text{V} E^\circ_{\text{Mg}^{2+}/\text{Mg}} = -2{,}356\ \text{V} E^\circ_{\text{Cu}^{2+}/\text{Cu}} = +0{,}34\ \text{V} E^\circ_{\text{2H}^+/\text{H}_2} = 0{,}0\ \text{V}
Phát biểu
Đúng
Sai
a
Nếu thay H_2SO_4 loãng bằng H_2SO_4 đặc, nguội thì cả 3 kim loại đều tan nhanh hơn.
b
Ở bước 2, ở cả ba ống nghiệm đều có khí thoát ra.
c
Sau bước 2, nếu nhỏ 1 giọt dung dịch CuSO_4 1M vào cả 3 ống thì các kim loại đều tan nhanh hơn.
d
Tốc độ thoát khí ở ống (3) > (1) > (2).
Phần III
Thí sinh trả lời từ câu 1 đến câu 6.
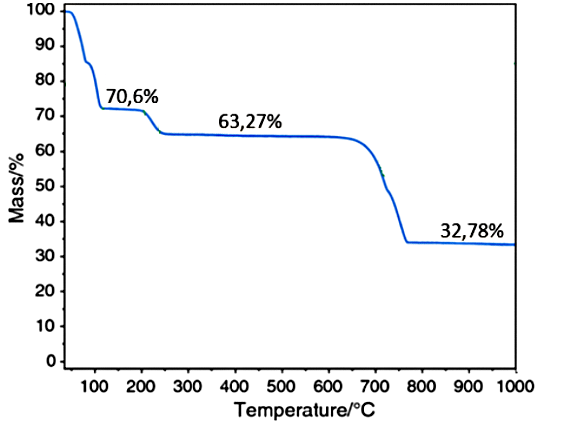
Một nhà hóa học trẻ quyết định nghiên cứu về sự nhiệt phân muối cobalt(II) pentahydrate (CoSO_4.5H_2O) để phục vụ cho dự án khoa học. Để tiến hành, anh ta đặt một mẫu muối màu hồng tươi vào thiết bị phân tích nhiệt trọng (TGA) và bắt đầu quá trình đun nóng đến 950°C. Kết quả là anh ta nhận được đồ thị về sự phụ thuộc vào khối lượng mẫu của nhiệt độ như trong hình. Số nguyên tử trong một phân tử mẫu ở 520^\circ C là bao nhiêu?
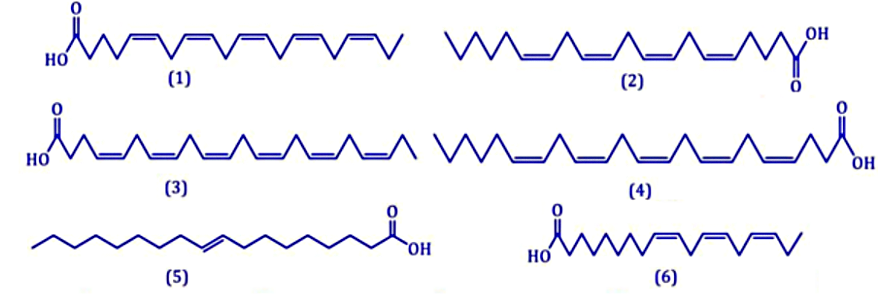
Acid béo omega-3 và omega-6 đều có vai trò quan trọng đối với cơ thể, giúp phòng ngừa nhiều loại bệnh. Cho các công thức cấu tạo của 6 acid béo đánh số từ (1) đến (6). Số acid béo omega-3 và omega-6 lần lượt là x, y. Giá trị xy là?
Cho các chất sau: CaCO_3(s),\ Br_2(l),\ H_2(g),\ O_2(g),\ HCl(g),\ Na(g),\ CO_2(g),\ Cl_2(g),\ N_2(g). Có bao nhiêu chất có \Delta H^\circ_{f} = 0?
Bột ngọt (monosodium glutamate) là một loại gia vị, được sản xuất từ dung dịch NaOH 40% và tinh thể glutamic acid (chứa 81% khối lượng acid) bằng cách dùng dung dịch NaOH trung hòa dung dịch glutamic acid đến pH = 6,8. Sau đó đem lọc, cô đặc và kết tinh dung dịch sản phẩm bằng phương pháp sấy chân không ở nhiệt độ thấp. Bột ngọt thu được có độ tinh khiết 99%. Giả thiết hiệu suất của cả quá trình tính theo glutamic acid là 95%. Để thu được 1 tấn bột ngọt cần m tấn tinh thể glutamic acid. Tính m? (kết quả làm tròn đến phần trăm).
Cho phương trình hóa học của các phản ứng được đánh số thứ tự từ 1 tới 4: (1) (C_6H_{10}O_5)_n (tinh bột) + nH_2O\ (H^+, t^\circ) \rightarrow nC_6H_{12}O_6 (glucose) (2) C_6H_{12}O_6 (glucose) (enzyme) \rightarrow 2C_2H_5OH + 2CO_2 (3) C_6H_{12}O_6 (glucose) (enzyme) \rightarrow 2CH_3CH(OH)COOH (4) C_6H_{12}O_6 + 2[Ag(NH_3)_2]OH\ (t^\circ) \rightarrow CH_2OH(CHOH)_4COONH_4 + 2Ag + 3NH_3 + H_2O Gán số thứ tự phương trình hóa học theo tiến trình: lên men rượu, thủy phân, lên men lactic, tráng gương. Dãy đúng là:
Kim loại sodium (Na) được điều chế bằng cách điện phân nóng chảy hỗn hợp NaCl và CaCl_2 với dòng điện có cường độ 3000 A và điện áp U = 25V. Hiệu suất điện phân là 80%. Tính điện năng (kWh) đã sử dụng để điều chế 1 kg Na. Biết: A = U \cdot n \cdot F với ne là số mol electron trao đổi giữa điện cực với các chất điện phân, F = 96485 C/mol, 1\ \text{kWh} = 3{,}6 \cdot 10^6\ \text{J} (Kết quả làm tròn đến phần mười).
Xem đáp án và bài mẫu
Answer key
Nguyên tố potassium (K) có số hiệu nguyên tử là 19. Ở trạng thái cơ bản, cấu hình electron của nguyên tử K là:
[Ar]4s^{1}
[Kr]4s^{2}
[Ar]4s^{2}
[Kr]4s^{1}
Giải thích câu 1
Giải thích chi tiết
😎 Cùng DOL xem qua cách giải câu này nhé!
📃 Thông tin đề bài cho:
Nguyên tố potassium (K) có số hiệu nguyên tử là 19.
Câu hỏi yêu cầu viết cấu hình electron ở trạng thái cơ bản.
Các phương án trả lời: • [Ar] 4s¹ • [Kr] 4s² • [Ar] 4s² • [Kr] 4s¹
❓ Hiểu câu hỏi:
Câu hỏi: Xác định cấu hình electron nguyên tử K (Z = 19) ở trạng thái cơ bản.
Áp dụng khái niệm: • Số hiệu nguyên tử cho biết tổng số electron trong nguyên tử trung hòa. • Sử dụng quy tắc thứ tự năng lượng các lớp electron và ký hiệu cấu hình rút gọn theo khí hiếm.
🔎 Hướng dẫn cách làm:
Bước 1: Xác định tổng số electron của K bằng số hiệu nguyên tử: • Z(K) = 19 ⇒ có 19 electron.
Bước 2: Nhận biết khí hiếm gần nhất có số electron nhỏ hơn 19 là argon (Ar) với 18 electron.
Bước 3: Viết cấu hình rút gọn: • Đã chiếm đủ 18 electron đầu tiên là cấu hình của Ar, ghi là [Ar].
Bước 4: Còn lại 1 electron (19 – 18 = 1) sẽ vào orbital có năng lượng tiếp theo, theo thứ tự 4s. • Do đó số electron ở 4s là 1.
Bước 5: Kết hợp lại thành cấu hình: • [Ar]\,4s^{1}
✅ Đáp án: [Ar]\,4s^{1}
❌ Các đáp án khác:
[Kr] 4s²: Sai vì Kr (Z=36) nhiều electron hơn K, không thể làm khí hiếm nền cho K.
[Ar] 4s²: Sai vì 4s² sẽ có tổng 18 + 2 = 20 electron, vượt quá 19.
[Kr] 4s¹: Sai vì vẫn dùng Kr làm cấu hình nền, không phù hợp với số electron thực tế của K.
Hiện bạn đang luyện đề THPTQG Môn Hoá thuộc chuyên mục luyện thi THPT Quốc gia. Để tiếp tục rèn luyện với nhiều đề thi khác, bạn có thể tham khảo các đề liên quan trực tiếp khác dưới đây.


