Đáp án & giải thích đề môn Hoá k12
Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Quảng Nam 2025 - Đề 02

DOL THPT
Mar 27, 2026
Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Quảng Nam 2025 - Đề 02 được xây dựng dưới mô hình thi thử trắc nghiệm online, giúp bạn hiểu rõ format đề thi. Hệ thống chấm điểm ngay sau khi bạn nộp bài, đồng thời lưu quá trình làm bài để bạn tiện theo dõi lộ trình ôn tập, đi kèm đáp án giải thích chi tiết và download PDF đề thi miễn phí HOÀN TOÀN MIỄN PHÍ.

Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Quảng Nam 2025 - Đề 02
Download PDF
Miễn phí dowload
Câu hỏi đề bài
28 Câu hỏi
Phần I
Cho biết nguyên tử khối: H = 1, C = 12, N = 14, O = 16, Na = 23, Mg = 24, Al = 27, Cl = 35,5, K = 39, Ca = 40, Fe = 56, Cu = 64, Zn = 65, Au = 197.
Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Cho phức chất có công thức [Fe(OH_2)_6](NO_3)_3.3H_2O. Nguyên tử trung tâm của phức chất trên là
H_2O
H_2O và NO_3^-
NO_3^-
Fe^{3+}
Thiết lập pin điện hóa ở điều kiện chuẩn gồm hai điện cực tạo bởi các cặp oxi hóa - khử E^0_{Ni^{2+}/Ni}=-0,257 \text{V} và E^0_{Cd^{2+}/Cd}=-0,403\text{V}. Sức điện động chuẩn của pin điện hóa trên là
-0{,}146V
+0{,}146V
0{,}000V
+0{,}660V
Các ký hiệu này thường được in trên bao bì, vỏ hộp, đồ dùng,… để giúp nhận biết vật liệu polymer cũng như thuận lợi cho việc thu gom, tái chế. Polymer có ký hiệu số 5 được điều chế bằng phản ứng trùng hợp monomer nào dưới đây?

CH_2=CH–Cl
CH_2=CH_2
CH_2=CH–C_6H_5
CH_2=CH–CH_3
Trong quá trình Solvay, ở giai đoạn tạo thành NaHCO_3 tồn tại cân bằng sau: NaCl + NH_3 + CO_2 + H_2O ⇌ NaHCO_3 + NH_4Cl. Khi làm lạnh dung dịch trên, muối bị tách ra khỏi dung dịch là
NaCl
NH_4Cl
NH_4HCO_3
NaHCO_3
Một thí nghiệm được mô tả như hình dưới. Thứ tự các amino acid ứng các vệt được đánh dấu (1), (2), (3) là
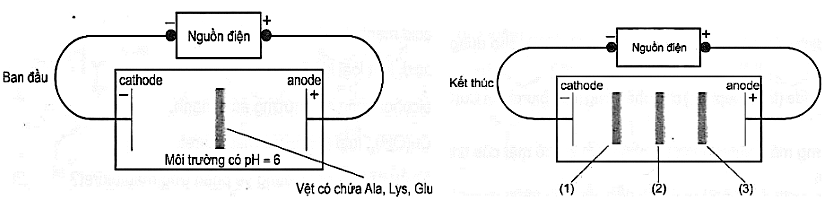
Ala, Lys, Glu
Lys, Ala, Glu
Lys, Glu, Ala
Glu, Ala, Lys
Dãy kim loại nào sau đây sắp xếp theo thứ tự độ dẫn điện giảm dần?
Ag, Cu, Au, Al
Au, Ag, Cu, Al
Cu, Al, Ag, Au
Ag, Au, Al, Cu
Trong cơ thể người, glucose được vận chuyển từ đường máu đến các tế bào, cung cấp năng lượng cho cơ thể hoạt động. Chất E sinh ra ở tuyến tụy sẽ giúp duy trì lượng glucose trong máu ổn định ở giá trị khoảng 4,4 - 7,2 mmol/l. Theo bạn, chất E là
triolein
enzyme amylaza
aspirin
insulin
Số nguyên tử hydrogen trong phân tử methyl formate là
4
6
2
8
Cho cân bằng hoá học: H_2 (g) + I_2 (g) \rightleftharpoons 2HI (g), \Delta_rH^0_{298}>0; Cân bằng không bị chuyển dịch khi
giảm nồng độ HI
giảm áp suất chung của hệ
tăng nhiệt độ của hệ
tăng nồng độ H_2
Cho bột kim loại Cu dư vào dung dịch gồm Fe(NO_3)_3 và AgNO_3, sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch chứa các muối nào sau đây?
Cu(NO_3)_2, Fe(NO_3)_2
AgNO_3, Fe(NO_3)_3
Cu(NO_3)_2, Fe(NO_3)_3
Cu(NO_3)_2, AgNO_3
Một thí nghiệm được mô tả như hình dưới. Chất lỏng thu được ở ống nghiệm X có mùi táo, có tên gọi là
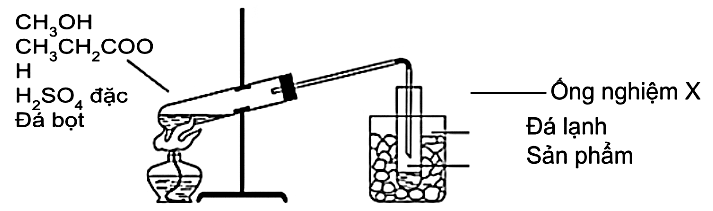
ethyl formate
propyl formate
methyl propionate
ethyl propionate
Cho các dung dịch có cùng nồng độ 0,1M: glucose, ammonia, aniline, ethylamine được kí hiệu ngẫu nhiên là X, Y, Z, T. Tiến hành đo giá trị pH của mỗi dung dịch thu được kết quả theo bảng. Các dung dịch glucose, ammonia, aniline, ethylamine tương ứng với các kí hiệu là

T, Y, X, Z
Z, X, Y, T
X, T, Y, Z
T, X, Z, Y
Chất nào sau đây có đồng phân hình học?
(CH_3)_2–CH–CH=CH_2
CH_2=CH–CH_2–CH_3
CH_3–CH=CH–CH_2–CH_3
CH_3–CH=C(CH_3)_2
Phối tử trong phức chất [PtCl_4]^{2-} và [Fe(CO)_5] lần lượt là
Pt và Fe
Cl và CO
Cl^- và C
Cl^- và CO
Phản ứng chuyển hóa hydrogen sulfide trong khí thiên nhiên thành sulfur được thực hiện theo sơ đồ phản ứng: H_2S + SO_2 \rightarrow S + H_2O. Khối lượng gam sulfur tối đa tạo ra khi chuyển hóa 1000 m^3 khí thiên nhiên (đkc) (chứa 5 mg H_2S/m^3) là
5,0
10,0
7,06
100,0
Khi làm lạnh dung dịch FeCl_3 thu được tinh thể FeCl_3.6H_2O. Cho độ tan của FeCl_3.6H_2O trong nước ở một số nhiệt độ như bảng dưới. Dung dịch bão hoà của FeCl_3 ở 0^\circC có nồng độ phần trăm là

25,6%
17,4%
18,2%
22,2%
Phosgene là chất khí không màu, mùi cỏ mục, dễ hóa lỏng, khối lượng riêng 1,420 g/cm^3 (ở 0^oC), t_s=8,2^{\circ}C. Phosgene ít tan trong nước, dễ tan trong các dung môi hữu cơ, bị thủy phân chậm bằng hơi nước; không cháy; là sản phẩm công nghiệp quan trọng; dùng trong tổng hợp hữu cơ để sản xuất phẩm nhuộm, chất diệt cỏ, polyurethane,…Phosgene được điều chế từ CO và Cl_2 theo phương trình sau: CO + Cl_2 → COCl_2 Phosgene là một chất độc, ở nồng độ 0,005mg/L đã nguy hiểm đối với người trong khoảng 0,1 – 0,3 mg/L gây tử vong sau 15 phút. Phosgene được điều chế bằng cách cho hỗn hợp CO và Cl_2 đi qua than hoạt tính. Biết giá trị năng lượng của các liên kết như bảng. Biến thiên enthalpy (kJ/mol) của phản ứng tạo thành phosgene từ CO và Cl_2 có giá trị là bao nhiêu?
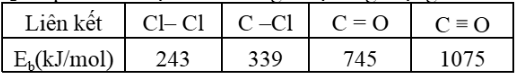
218
-108
-214
-105
Cho các phát biểu sau: (1) Nguyên tử của các nguyên tố kim loại thường có từ 1 electron đến 3 electron ở lớp electron ngoài cùng. (2) Đại lượng đánh giá khả năng khử giữa các dạng khử và khả năng oxi hóa giữa các dạng oxi hóa ở điều kiện chuẩn là dãy điện hóa. (3) Cho dung dịch KHSO_4 vào dung dịch Ba(OH)_2 thu được kết tủa trắng. (4) Nhúng thanh Fe vào dung dịch chứa hỗn hợp H_2SO_4 loãng và lượng nhỏ CuSO_4 xảy ra hiện tượng ăn mòn điện hóa, (5) Các kim loại chuyển tiếp dãy thứ nhất có cấu hình electron đều có phân lớp 3d bão hòa electron. Số phát biểu đúng là
3
4
2
5
Phần II
Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Soda được sản xuất theo phương pháp Solvay theo các phương trình hóa học sau: NaCl(aq) + CO_2(g) + H_2O(l) + NH_3(aq) \rightarrow NaHCO_3(s) + NH_4Cl(aq); 2NaHCO_3(s) \rightarrow Na_2CO_3(s) + CO_2(g) + H_2O(g); 2NH_4Cl(aq) + CaO(s) \rightarrow 2NH_3(g) + CaCl_2(aq) + H_2O(l). Những phát biểu nào sau đây đúng hay sai?
Phát biểu
Đúng
Sai
a
Phản ứng (1) cho thấy H_2CO_3 (CO_2 + H_2O) có tính acid mạnh hơn dung dịch HCl.
b
Trong phản ứng (2) khối lượng chất rắn giảm 45% sau khi nung (giả sử hiệu suất nung là 100%).
c
Phản ứng (3) nhằm thu hồi và tái sử dụng NH_3.
d
Muối sodium hydrogencarbonate ít tan trong nước và kém bền khi bị nung nóng.
Bộ phận quan trọng nhất của máy tạo nhịp tim là một hệ pin điện hóa lithium – iodine (gồm hai cặp oxi hóa khử Li^+/Li và I_2/2I^-). Hai điện cực được đặt vào tim, phát sinh dòng điện nhỏ kích thích tim đập ổn định. Cho biết: E^0_{Li^+/Li}=-3,04V, E^0_{I_2/2I^-}=+0,54V; Li = 6,9; điện tích của 1 mol electron là 96500 C/mol; q = I.t, trong đó q là điện tích (C), I là cường độ dòng điện (A), t là thời gian (s), 1 năm = 365 ngày.
Phát biểu
Đúng
Sai
a
Khi pin hoạt động Lithium đóng vai trò là anode, tại anode xảy ra quá trình khử.
b
Nếu pin tạo ra một dòng điện ổn định bằng 2{,}5 \times 10^{-5} A thì một pin được chế tạo bởi 0,5 gam lithium có thể hoạt động tối đa trong thời gian 8 năm. (Biết M_{Li} = 6,9g/mol)
c
Sức điện động chuẩn của pin E^0_{\text{pin}}=+3,58V.
d
Máy tạo nhịp tim có thể được đặt tạm thời hay vĩnh viễn trong cơ thể tùy theo tình trạng sức khỏe và các bệnh lý kèm theo của bệnh nhân.
Tiến hành các thí nghiệm theo các bước sau: Bước 1: Cho vào hai ống nghiệm (1) và (2) mỗi ống 1 mL ethyl acetate. Bước 2: Thêm 2 mL dung dịch H_2SO_4 20% vào ống nghiệm (1); 2 mL dung dịch NaOH 30% vào ống nghiệm (2). Bước 3: Đun cách thủy ống nghiệm (1) và (2) trong cốc thủy tinh ở nhiệt độ 60 – 70 ^{o}C khoảng 5 phút.
Phát biểu
Đúng
Sai
a
Sau bước 2, chất lỏng trong ống nghiệm (1) phân lớp, chất lỏng trong ống nghiệm (2) đồng nhất.
b
Phản ứng thủy phân ester trong môi trường kiềm xảy ra tốt hơn so với môi trường acid.
c
Sau bước 3, sản phẩm phản ứng thủy phân trong cả hai ống nghiệm đều tan tốt trong nước.
d
Sau bước 3, chất lỏng trong cả hai ống nghiệm đều đồng nhất.
Tinh bột là polymer thiên nhiên gồm amylose và amylopectin. Tinh bột có công thức phân tử là (C_6H_{10}O_5)_n. Một học sinh tiến hành thí nghiệm đối với tinh bột theo các bước sau: Bước 1: Cho khoảng 5 mL dung dịch hồ tinh bột vào ống nghiệm. Sau đó thêm khoảng 1 mL dung dịch HCl 1 M vào, lắc đều. Bước 2: Đặt ống nghiệm trong một cốc thuỷ tinh chứa nước nóng, đun cách thuỷ trong 10 phút. Sau đó để nguội. Bước 3: Thêm từ từ sodium hydrogencarbonate vào ống nghiệm đến khi ngừng sủi bọt khí. Bước 4: Cho khoảng 2 mL dung dịch thu được vào ống nghiệm chứa copper (II) hydroxide (được điều chế bằng cách cho 0,5mL dung dịch copper (II) sulfate vào 2 mL dung dịch sodium hydroxide, lắc nhẹ). Sau đó đặt ống nghiệm trong cốc thuỷ tinh chứa nước nóng khoảng 5 phút.
Phát biểu
Đúng
Sai
a
Trong bước 2 đã xảy ra phản ứng thủy phân tinh bột tạo glucose.
b
Sau bước 4, thu được dung dịch màu xanh lam.
c
Sau bước 1, thu được hai loại monosaccharide.
d
Trong bước 3, sodium hydrogencarbonate được thêm vào nhằm mục đích làm tăng tốc độ phản ứng thủy phân ở bước 2.
Phần III
Thí sinh trả lời từ câu 1 đến câu 6.
Cho dãy các chất sau: tripanmitin, aminoacetic acid, Ala-Gly-Glu, ethyl propionate, aniline. Có bao nhiêu chất trong dãy có phản ứng với dung dịch NaOH (đun nóng)?
Cho phương trình hóa học của phản ứng tổng hợp ammonia: N_2 + 3H_2 \rightarrow 2NH_3. Khi tăng nồng độ của hydrogen lên 2 lần, tốc độ phản ứng thuận tăng lên bao nhiêu lần?
Poly(ethylene terephthalate) (viết tắt là PET) là một polymer được điều chế từ terephthalic acid và ethylene glycol. PET được sử dụng để sản xuất tơ, chai đựng nước uống, hộp đựng thực phẩm. Để thuận lợi cho việc nhận biết, sử dụng và tái chế thì các đồ nhựa làm từ vật liệu chứa PET thường được in kí hiệu như hình bên. Cho các phát biểu sau: (a) PET thuộc loại polyester. (b) Tơ được chế tạo từ PET thuộc loại tơ tổng hợp. (c) Trong một mắt xích PET, phần trăm khối lượng cacbon là 62,5%. (d) Phản ứng tổng hợp PET từ terephthalic acid và ethylene glycol thuộc loại phản ứng trùng hợp. Có bao nhiêu phát biểu đúng?
Điện phân nóng chảy Al_2O_3 với các điện cực bằng than chì, thu được m kilogram Nhôm (Aluminium, Al) ở catot và 99,16 m^3 (đkc) hỗn hợp khí X ở anot. Tỉ khối của X so với H_2 bằng 16,7. Cho 1,2395 lít X (đkc) phản ứng với dung dịch Ca(OH)_2 dư, thu được 1,5 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Tính giá trị m? (Kết quả làm tròn đến hàng đơn vị)
Trong quá trình hô hấp tế bào, 1 mol glucose bị oxi hóa hoàn toàn sẽ giải phóng một năng lượng là 2880 kJ. Trong khẩu phần ăn hằng ngày của một người trưởng thành có 300 g gạo (chứa 80% hàm lượng tinh bột). Giả sử 60% lượng tinh bột trong gạo chuyển thành glucose và toàn bộ lượng glucose này tham gia vào quá trình hô hấp tế bào. Năng lượng giải phóng từ sự oxi hóa hoàn toàn lượng glucose trên chiếm bao nhiêu phần trăm so với nhu cầu năng lượng trung bình 2000 cal/ngày của một người trưởng thành. Cho 1cal = 4184 J. ( kết quả làm tròn đến hàng phần chục).
Theo QCVN 01-1:2018/BYT, hàm lượng sắt tối đa cho phép trong nước sinh hoạt là 0,30 mg/L. Một mẫu nước có hàm lượng sắt cao gấp 28 lần ngưỡng cho phép, giả thiết sắt trong mẫu nước tồn tại ở dạng Fe_2(SO_4)_3 và FeSO_4 với tỉ lệ mol tương ứng là 1 : 4. Quá trình tách loại sắt trong 10 m^3 mẫu nước được thực hiện bằng cách sử dụng m gam vôi tôi (vừa đủ) để tăng pH, sau đó sục không khí theo các phản ứng: (1) Fe_2(SO_4)_3 + Ca(OH)_2 \rightarrow Fe(OH)_3 + CaSO_4; (2) FeSO_4 + Ca(OH)_2 + O_2 + H_2O \rightarrow Fe(OH)_3 + CaSO_4. Tính giá trị của m? (Kết quả làm tròn đến hàng đơn vị)
Xem đáp án và bài mẫu
Answer key
Cho phức chất có công thức [Fe(OH_2)_6](NO_3)_3.3H_2O. Nguyên tử trung tâm của phức chất trên là
H_2O
H_2O và NO_3^-
NO_3^-
Fe^{3+}
Giải thích câu 1
Giải thích chi tiết
😎 Cùng DOL xem qua cách giải câu này nhé!
📃 Thông tin đề bài cho:
Công thức phức chất: [Fe(H_2O)_6](NO_3)_3\cdot3H_2O
Yêu cầu: Xác định nguyên tử trung tâm của phức chất.
❓ Hiểu câu hỏi:
Hỏi “nguyên tử trung tâm” trong phức chất là gì?
Biết rằng trong hóa học phối trí, nguyên tử trung tâm thường là kim loại nằm ở giữa ngoặc vuông.
🔎 Hướng dẫn cách làm:
Trong một phức chất viết dưới dạng [M(L)_x]^{n+}, chữ M đại diện cho nguyên tử trung tâm (thường là kim loại), còn L là các ligand (phân tử hoặc ion phối).
Ở đây phức chất của ta là [Fe(H_2O)_6]^{3+}, nghĩa là:
Nguyên tử trung tâm M = Fe
Ligand L = H₂O (6 phân tử nước)
Các thành phần bên ngoài ngoặc vuông (NO_3^-) là anion đối điện (counter-ions) để trung hòa điện tích và “3H₂O” phía sau là nước tinh thể, không phải nguyên tử trung tâm.
Vậy nguyên tử trung tâm chính là sắt ở oxi hóa mức +3, tức Fe^{3+}.
✅ Đáp án: Fe^{3+}
❌ Các đáp án khác:
A. H_2O: đây là ligand phối với Fe, không phải nguyên tử trung tâm.
B. H_2O\ và\ NO_3^-: H₂O là ligand, NO₃⁻ là anion đối điện, không phải trung tâm.
C. NO_3^-: đây chỉ là anion đối điện, không tham gia làm nguyên tử trung tâm.
Hiện bạn đang luyện đề THPTQG Môn Hoá thuộc chuyên mục luyện thi THPT Quốc gia. Để tiếp tục với nhiều đề thi khác, bạn có thể luyện tập thêm các đề thi liên quan trực tiếp khác bên dưới.


