Đáp án & giải thích đề môn Hoá k12
Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Quảng Ngãi 2025 - Đề 02

DOL THPT
Mar 27, 2026
Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Quảng Ngãi 2025 - Đề 02 được xây dựng dưới dạng thi thử trắc nghiệm online, giúp bạn làm quen cấu trúc đề thi. Nền tảng chấm điểm tự động sau khi bạn nộp bài, đồng thời lưu quá trình làm bài để bạn tiện theo dõi quá trình ôn luyện, đi kèm đáp án giải thích chi tiết và tải PDF đề thi miễn phí HOÀN TOÀN MIỄN PHÍ.

Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Quảng Ngãi 2025 - Đề 02
Download PDF
Miễn phí dowload
Câu hỏi đề bài
28 Câu hỏi
Phần I
Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Cho sơ đồ các phản ứng hoá học sau: X_1 + H_2O \rightarrow X_2 + X_3 + H_2 ; X_2 + X_4 \rightarrow BaCO_3 \downarrow + Na_2CO_3 + H_2O ; X_4 + X_5 \rightarrow BaSO_4 \downarrow + K_2SO_4 + CO_2 \uparrow + H_2O (phương trình phản ứng chưa được cân bằng và chưa ghi điều kiện phản ứng). Nhận định nào sau đây đúng?
X_1 là KCl.
X_4 là NaHCO_3.
X_5 là KHSO_4.
X_2 là KOH.
Các ký hiệu này thường được in trên bao bì, vỏ hộp, đồ dùng,… để giúp nhận biết vật liệu polymer cũng như thuận lợi cho việc thu gom, tái chế. Polymer có ký hiệu số 5 được điều chế bằng phản ứng trùng hợp monome nào dưới đây?
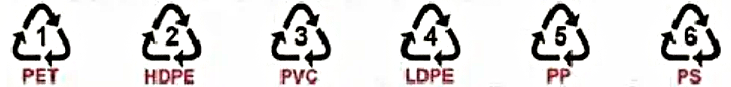
CH_2=CH_2
CH_2=CHCl
CH_2=CH-C_6H_5
CH_2=CH-CH_3
Vật liệu nào sau đây không phải là vật liệu cốt của vật liệu composite?
Sợi carbon.
Nhựa polymer.
Sợi vải.
Bột nhôm.
Hình dưới đây mô tả tính chất vật lí nào của kim loại? (hình tròn to mô tả ion kim loại, hình tròn nhỏ mô tả electron tự do)
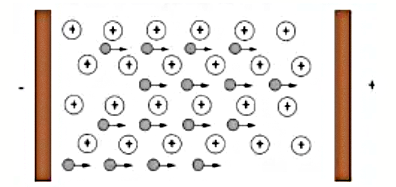
Tính dẻo.
Tính dẫn nhiệt.
Tính dẫn điện.
Tính cứng.
Hình ảnh dưới đây mô tả quá trình ăn mòn của gang và thép. Phát biều nào sau đây đúng?
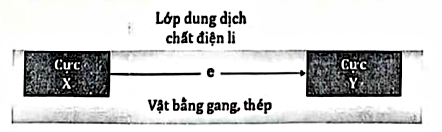
Sắt bị oxi hoá thành ion Fe^{2+} sau đó Fe^{2+} tiếp tục bị oxi hoá bởi O_2 trong không khí tạo ra sắt có thành phần chính là Fe_3O_4.nH_2O.
Cực X (anode) là carbon và cực Y (cathode) là sắt.
Có thể bảo vệ gang, thép theo phương pháp điện hoá bằng cách tráng lên bề mặt một kim loại khác như Zn, Sn.
Lớp dung dịch chất điện li có thể là dung dịch acid, base, muối hoặc không khí ẩm.
Một mẫu nước mưa có pH = 4,82. Vậy nồng độ H^+ trong mẫu nước mưa được xác định có giá trị
1,0.10^{-5} M
lớn hơn 1,0.10^{-5} M
nhỏ hơn 1,0.10^{-5} M
1,0.10^{-4} M
Cho các chất như hình dưới. Các chất arylamine là:
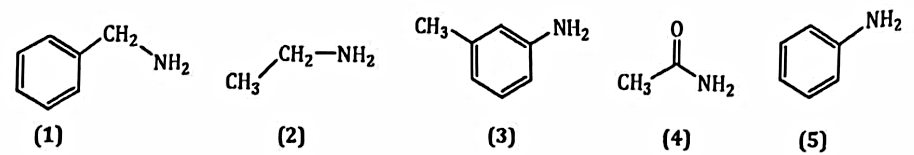
(1) và (5).
(3) và (5).
(1), (3), (5).
(3) và (4).
Cho dãy các nguyên tố: Mg, K, Ba, Na, Al, Sr. Số nguyên tố thuộc nhóm IIA là
2
4
1
3
Phản ứng đốt cháy methane xảy ra như sau: CH_4(g) + 2O_2(g) \rightarrow CO_2(g) + 2H_2O(l) (). Biết nhiệt tạo thành \Delta H^\circ_{298} của CH_4(g) là -74,8 kJ/mol, của CO_2(g) là -393,5 kJ/mol, của H_2O(l) là -285,8 kJ/mol. Giá trị biến thiên enthalpy chuẩn của phản ứng (*) là
+ 890,3 kJ
+ 604,5 kJ
- 604,5 kJ
- 890,3 kJ
Từ cấu hình electron của nguyên tử Cu ở trạng thái cơ bản là [Ar]3d^{10}4s^1, cấu hình electron của ion Cu^{2+} là
[Ar]3d^9
[Ar]3d^8 4s^1
[Ar]3d^8
[Ar]3d^{10}
Cho các phát biểu sau: (1) Do có tính oxi hoá mạnh, nitric acid thường được sử dụng để phá mẫu quặng trong việc nghiên cứu, xác định hàm lượng các kim loại trong quặng. (2) Hiện tượng mưa acid là do không khí bị ô nhiễm bởi các khí SO_2, CO, NO_2. (3) Hiện tượng phú dưỡng là do sự dư thừa các chất dinh dưỡng, bao gồm cả hợp chất chứa nitơ và photpho. (4) Mưa acid gây ra rất nhiều tác hại cho đời sống và sản xuất, nước mưa acid có pH nằm trong khoảng dưới 5,6. Số phát biểu đúng là
4
3
2
1
Tinh thể chất rắn X không màu, vị ngọt, dễ tan trong nước. X có nhiều trong cây mía, củ cải đường và hoa thốt nốt. Trong công nghiệp, X được chuyển hóa thành chất Y dùng để tráng gương, tráng ruột phích. Tên gọi của X và Y lần lượt là
glucose và fructose
saccharose và glucose
glucose và saccharose
saccharose và tinh bột
Hydrocacbon no X có kết quả phổ MS như hình dưới. Phần trăm khối lượng carbon trong X là
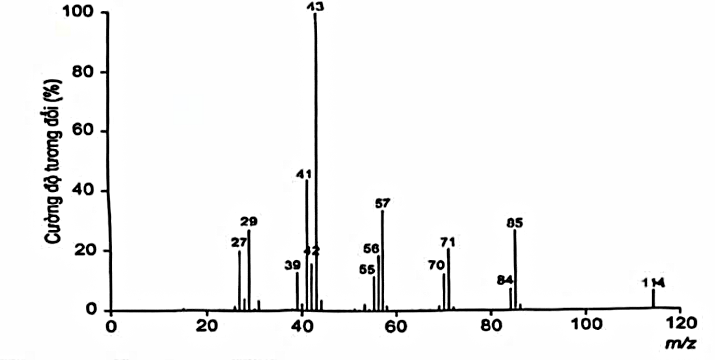
30,77%
84,21%
50%
15,79%
Hợp chất CH_2=CHCOOCH_3 có tên là
vinyl acetate
methyl acetate
methyl acrylate
methyl propionate
Ester no, đơn chức, mạch hở X là dung môi hữu cơ được sử dụng nhiều trong công nghiệp hoá chất. Phổ MS cho biết khối lượng phân tử X là 88. Trong đời sống, hợp chất X_2 được điều chế từ quá trình lên men tinh bột và là một thành phần của xăng E5. Cho các phương trình hoá học sau: (1) X + H_2O \xrightarrow{H_2SO_4, to} X_1 + X_2 ; (2) X_2 + CuO \rightarrow X_3 + Cu + H_2O ; (3) X_3 + 3I_2 + 4NaOH \rightarrow X_4 + CHI_3 + 3NaI + 3H_2O. Phát biểu nào sau đây là đúng?
Thứ tự nhiệt độ sôi được sắp xếp theo chiều X_2 < X_3 < X_1.
X_2 tan tốt trong nước hơn X_1 và X_2.
X_4 có thể tham gia phản ứng tráng bạc với thuốc thử Tollens.
Có thể thực hiện phản ứng theo sơ đồ chuyển hoá X_2 \rightarrow X_3 \rightarrow X_4.
Chất nào sau đây thuộc loại disaccharide?
Glucose
Cellulose
Saccharose
Fructose
Khi cho 100 kg một loại mỡ (giả sử có chứa 50% tristearin; 30% triolein và 20% tripalmitin về khối lượng) tác dụng với dung dịch potassium hydroxide vừa đủ thu được m kg muối (biết hiệu suất phản ứng đạt 100%). Giá trị m là
108,7
119,3
87,6
103,2
Điện phân là
Quá trình oxi hoá - khử xảy ra trên bề mặt các điện cực khi có dòng điện 1 chiều với hiệu điện thế đủ lớn đi qua chất điện li nóng chảy hoặc dung dịch chất điện li.
Quá trình oxi hoá - khử xảy ra trên bề mặt các điện cực khi có dòng điện 2 chiều với hiệu điện thế đủ lớn đi qua chất điện li nóng chảy hoặc dung dịch chất điện li.
Quá trình oxi hoá - khử xảy ra trên bề mặt các điện cực khi có dòng điện 1 chiều đi qua chất điện li rắn khô.
Quá trình oxi hoá - khử xảy ra trên bề mặt các điện cực khi có dòng điện đi qua chất điện li nóng chảy hoặc dung dịch chất điện li.
Phần II
Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Hai ống nghiệm (1) và (2) đều chứa 1 mL dung dịch copper(II) sulfate 0,5% màu xanh nhạt. Tiến hành hai thí nghiệm sau ở 20 ºC: Thí nghiệm 1: Thêm từ từ cho đến hết 2 mL dung dịch hydrochloric acid đặc không màu vào ống nghiệm (1), vừa nhỏ vừa lắc đều thì sau đó thu được dung dịch có màu vàng chanh, do có quá trình: [Cu(OH)_2(H_2O)_4]^{2+} + 4Cl^{-} \leftrightarrow [CuCl_4]^{2-} + 6H_2O (K_c = 4,18.10^5). Thí nghiệm 2: Thêm từ từ cho đến hết 2 mL dung dịch sodium chloride không màu vào ống nghiệm (2), vừa nhỏ vừa lắc đều thì sau đó thu được dung dịch có màu xanh nhạt hơn so với ban đầu. Phát biểu sau đây đúng hay sai?
Phát biểu
Đúng
Sai
a
Thí nghiệm 2, không có dấu hiệu của phản ứng hình thành phức chất.
b
Trong thí nghiệm 1 có sự thay đổi màu sắc dung dịch, chứng tỏ có phản ứng thay thế phối tử H_2O trong phức chất [Cu(OH_2)_6]^{2+} bởi các phối tử Cl^{-}.
c
Liên kết trong phức [Cu(OH_2)_6]^{2+} là liên kết cho – nhận, trong đó mỗi phân tử H_2O đã cho 2 cặp electron liên kết vào các orbital trống của ion trung tâm Cu^{2+} tạo nên phức có dạng hình học bát diện.
d
Thí nghiệm 1 chứng minh phức [Cu(OH_2)_6]^{2+} bền hơn phức [CuCl_4]^{2-}.
Vị tanh của cá, đặc biệt là cá mè, là do các amine gây ra, trong đó có amine X. Phân tích nguyên tố cho kết quả: %C = 61,02%; %H = 15,25%; %N = 23,73%. Từ phổ khối lượng xác định được phân tử khối của X là 59. Bằng phương pháp khác, thấy phân tử X có cấu trúc đối xứng cao. Mỗi phát biểu sau đây là đúng hay sai.
Phát biểu
Đúng
Sai
a
pH của dung dịch X 0,1M ở 20 ºC khoảng 11,4 (biết hằng số K_b ở nhiệt độ này là 6,5.10^{-5}).
b
Để loại bỏ 5,9 gam X bằng dung dịch giấm ăn (acetic acid) 5% thì cần tối thiểu 100 mL dung dịch giấm ăn, biết D_\text{giấm ăn} = 1002,5 g/L.
c
Danh pháp thay thế của X là trimethylamine.
d
Ở điều kiện thường, X là chất khí, tan tốt trong nước.
Cho biết giá trị thế điện cực của các cặp oxi hoá khử . Phát biểu sau đây đúng hay sai?

Phát biểu
Đúng
Sai
a
Pin Galvani Z–X có suất điện động lớn nhất trong các pin Galvani tạo từ 4 kim loại trên.
b
Kim loại Z có tính khử mạnh nhất nên có thể đẩy các kim loại còn lại ra khỏi dung dịch muối của chúng.
c
Pin Galvani được thiết lập bởi 2 cặp điện cực: Y^{2+}/Y và T^{2+}/T với anode là T^{2+}/T và cathode là Y^{2+}/Y.
d
Trình tự oxi hoá được xếp theo thứ tự: Z^{2+} > Y^{2+} > T^{2+} > X^{+}.
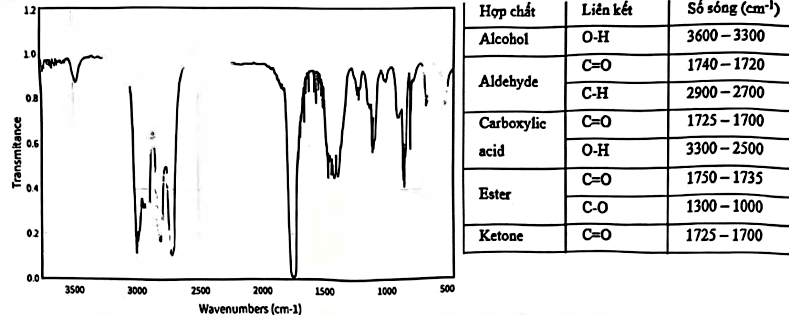
Hợp chất hữu cơ X no, mạch hở, công thức phân tử là C_3H_6O và phổ IR của chất X như hình. Mối quan hệ các hợp chất X, Y, Z, T được biểu diễn bằng các phương trình: (1) X + 2[H] \xrightarrow{LiAlH_4} alcohol Y ; (2) X + Br_2 + H_2O \rightarrow acid Z + 2HBr ; (3) Y + acid Z \xrightarrow{H_2SO_4,\ to} ester T + H_2O. Phát biểu sau đây đúng hay sai?
Phát biểu
Đúng
Sai
a
Dựa trên phổ IR có thể xác định X là acetone.
b
Ester T có danh pháp thay thế là propyl propionate.
c
Hợp chất X thể hiện tính oxi hoá ở phản ứng (1) và tính khử ở phản ứng (2).
d
Hợp chất X, Y, Z tan được trong nước vì đều có khả năng tạo liên kết hydrogen với nước.
Phần III
Thí sinh trả lời từ câu 1 đến câu 6.
Ngành công nghiệp sản xuất nhiên liệu sinh học để phát triển bền vững cần áp dụng các công nghệ mới theo hướng thân thiện môi trường, rơm rạ là một loại phế phẩm nông nghiệp có thể dùng làm một nguồn nguyên liệu để sản xuất ethanol tạo xăng sinh học thay vì đốt gây ô nhiễm môi trường. Để sản xuất 100,0 L xăng E5 (ethanol chiếm 5% về thể tích) thì cần m kg rơm rạ. Biết cellulose chiếm 35% khối lượng khô của rơm rạ, việc tách cellulose ra khỏi rơm rạ thường đạt hiệu suất 40%. Trong khi đó, hiệu suất của quá trình chuyển hoá cellulose thành ethanol đạt 60%. Khối lượng riêng của ethanol là 0,8 g/mL. Giá trị của m là bao nhiêu? (Kết quả làm tròn đến hàng phần mười)

Hợp chất hữu cơ X (C_5H_{11}NO_2) tác dụng với dung dịch NaOH dư, đun nóng, thu được một muối chứa cả α-amino acid và ancol. Hợp chất hữu cơ X có bao nhiêu công thức cấu tạo thỏa mãn?
Muối ăn khi khai thác từ nước biển, mỏ muối, hồ muối thường có lẫn nhiều tạp chất như MgCl_2, CaCl_2, CaSO_4 làm cho muối có vị đắng chát và dễ bị chảy nước gây ảnh hưởng xấu tới chất lượng muối. Một trong những phương pháp loại bỏ tạp chất ở muối ăn là dùng hỗn hợp A gồm Na_2CO_3, NaOH, BaCl_2 tác dụng với dung dịch nước muối để loại tạp chất dưới dạng chất kết tủa CaCO_3, Mg(OH)_2, BaSO_4. Một mẫu muối thô thu được bằng phương pháp bay hơi nước biển có thành phần khối lượng như sau: 96,525% NaCl, 0,190% MgCl_2, 1,224% CaSO_4, 0,010% CaCl_2, 0,951% H_2O, còn lại là tạp chất trơ. Hỏi cần dùng bao nhiêu kilogram hỗn hợp A để loại bỏ hết tạp chất có trong 1 tấn muối nói trên (kết quả làm tròn đến hàng đơn vị).
Cho sơ đồ chuyển hóa sau: CH_4 \xrightarrow{+O_2, t^0} X \xrightarrow{+H_2, Ni} Y \xrightarrow{+CO, xt, t^0} Z \xleftrightarrow{Y(xt H-2SO_4)} T. Biết X, Y, Z, T là các hợp chất hữu cơ. Phân tử khối của T có giá trị là bao nhiêu?
Điểm chớp cháy là nhiệt độ thấp nhất ở áp suất xác định mà tại đó hơi của chất lỏng kết hợp với không khí tạo thành hỗn hợp hơi khí dễ cháy khi gặp nguồn lửa. Chất lỏng có điểm chớp cháy nhỏ hơn 37,8^{\circ}C gọi là chất lỏng dễ cháy. Có bao nhiêu chất lỏng dễ cháy trong bảng dưới?
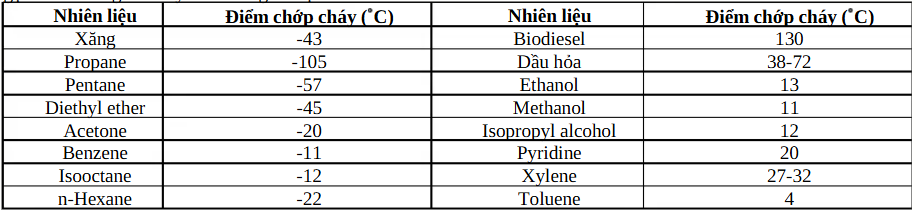
Một nhà máy sản xuất túi nylon từ HDPE, túi có dạng hình chữ nhật (kích thước 20 cm × 30 cm, bề dày của lớp nylon là 0,02 cm). Biết hiệu suất phản ứng trùng hợp ethylene để điều chế HDPE là 60%, quá trình chuyển nhựa thành túi có hiệu suất là 95% và khối lượng riêng của nhựa HDPE là 0,95 g/cm^3. Tính khối lượng (tấn) nguyên liệu ethylene cần dùng để sản xuất đơn hàng 10000 túi trên.
Xem đáp án và bài mẫu
Answer key
Cho sơ đồ các phản ứng hoá học sau: X_1 + H_2O \rightarrow X_2 + X_3 + H_2 ; X_2 + X_4 \rightarrow BaCO_3 \downarrow + Na_2CO_3 + H_2O ; X_4 + X_5 \rightarrow BaSO_4 \downarrow + K_2SO_4 + CO_2 \uparrow + H_2O (phương trình phản ứng chưa được cân bằng và chưa ghi điều kiện phản ứng). Nhận định nào sau đây đúng?
X_1 là KCl.
X_4 là NaHCO_3.
X_5 là KHSO_4.
X_2 là KOH.
Giải thích câu 1
Giải thích chi tiết
😎 Cùng DOL xem qua cách giải câu này nhé!
📃 Thông tin đề bài cho:
Phương trình 1: X_1 + H_2O \rightarrow X_2 + X_3 + H_2
Phương trình 2: X_2 + X_4 \rightarrow BaCO_3\downarrow + Na_2CO_3 + H_2O
Phương trình 3: X_4 + X_5 \rightarrow BaSO_4\downarrow + K_2SO_4 + CO_2\uparrow + H_2O
Các phương trình chưa cân bằng và chưa ghi điều kiện.
❓ Hiểu câu hỏi:
Yêu cầu xác định chất X₅.
Cần vận dụng tính chất phản ứng trao đổi ion và sự phân hủy của muối.
🔎 Hướng dẫn cách làm:
Bước 1: Xác định X₂ và X₄ từ phương trình 2 • Phương trình tổng quát: X_2+X_4\longrightarrow BaCO_3\downarrow+Na_2CO_3+H_2O. • Nếu chọn X_2 = NaOH và X_4 = Ba(HCO_3)_2, ta có (cân bằng): 2NaOH+Ba(HCO_3)_2\longrightarrow BaCO_3\downarrow+Na_2CO_3+2H_2O. ⇒ X₂ = NaOH, X₄ = Ba(HCO₃)₂.
Bước 2: Xác định X₅ từ phương trình 3 • Phương trình tổng quát: X_4 + X_5 \longrightarrow BaSO_4\downarrow + K_2SO_4 + CO_2 + H_2O. • Thay X_4 = Ba(HCO_3)_2. Đặt X_5 là muối có K⁺ và SO₄²⁻: KHSO₄. Ba(HCO_3)_2 + 2KHSO_4 \longrightarrow BaSO_4\downarrow + K_2SO_4 + 2CO_2 + 2H_2O. • Kết quả hoàn toàn trùng khớp với sản phẩm cho trước. ⇒ X₅ = KHSO₄.
✅ Đáp án: X_5 = KHSO_4
❌ Các đáp án khác:
A. X_1 = KCl: KCl không phản ứng với H₂O để sinh H₂, nên không phù hợp phương trình 1.
B. X_4 = NaHCO_3: nếu X₄ = NaHCO₃, phản ứng 2/3 không tạo được đúng BaCO₃ và BaSO₄ như đã cho.
D. X_2 = KOH: cần NaOH để tạo Na₂CO₃ ở phản ứng 2, không thể thay bằng KOH.
Bạn đang luyện đề THPTQG Môn Hoá thuộc chuyên mục luyện thi THPT Quốc gia. Để tiếp tục rèn luyện với nhiều đề thi khác, bạn học có thể xem thêm những đề thi liên quan khác bên dưới.


