Đáp án & giải thích đề môn Hoá k12
Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Yên Bái 2025 - Đề 02

DOL THPT
Mar 27, 2026
Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Yên Bái 2025 - Đề 02 được xây dựng dưới hình thức thi thử trắc nghiệm online, giúp bạn hiểu rõ bố cục đề thi. Hệ thống chấm điểm ngay sau khi bạn hoàn thành bài thi, đồng thời lưu lại lịch sử làm bài để bạn theo dõi hiệu quả quá trình ôn luyện, đi kèm lời giải chi tiết, dễ hiểu và tải PDF đề thi miễn phí HOÀN TOÀN MIỄN PHÍ.

Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Yên Bái 2025 - Đề 02
Download PDF
Miễn phí dowload
Câu hỏi đề bài
28 Câu hỏi
Phần I
Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Tên gọi của polymer (-CH_2-CH=CH-CH_2-)_n là :
cao su buna.
cao su buna-S.
cao su buna-N.
cao su isoprene.
Cho sơ đồ pin Galvani Zn-Cu ở điều kiện chuẩn như hình bên. Phát biểu nào sau đây đúng ?
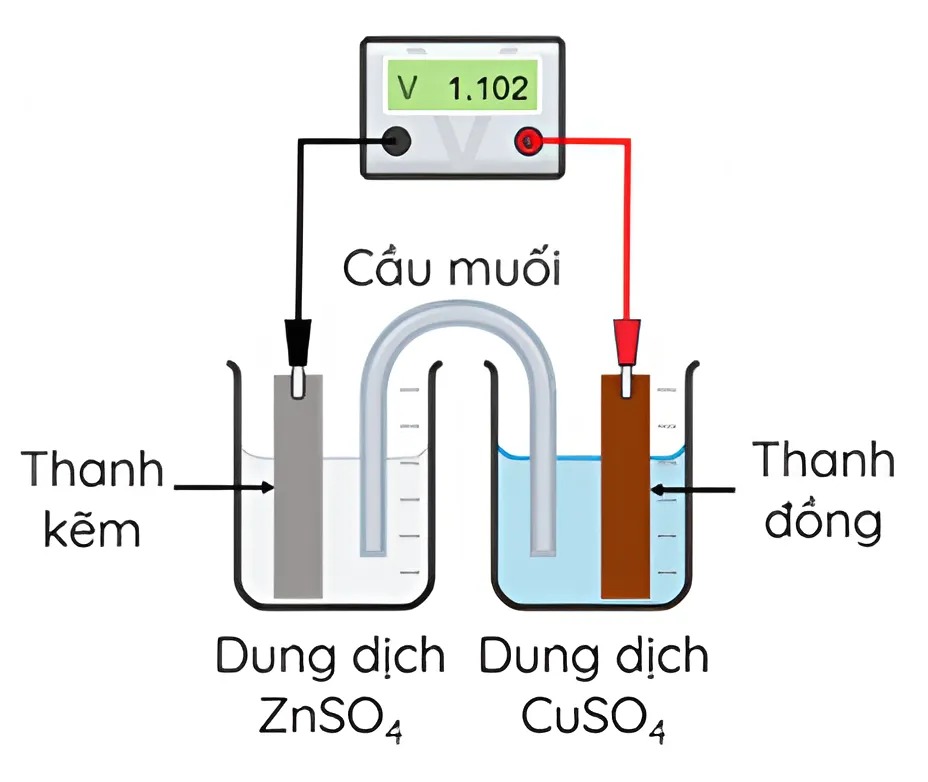
Thế điện cực chuẩn của cặp Cu^{2+}/Cu có giá trị bằng 1{,}102\ V.
Tại cathode của pin xảy ra quá trình oxi hóa Cu \to Cu^{2+} + 2e^-.
Phản ứng xảy ra trong pin là Zn + Cu^{2+} \to Zn^{2+} + Cu.
Electron chuyển từ điện cực Cu sang điện cực Zn thông qua dây dẫn điện.
Cho phản ứng nhiệt phân polystyrene: [-CH_2-CH(C_6H_5)-]_n\,(t^\circ) \to nCH_2=CH-C_6H_5. Phản ứng trên thuộc loại :
phản ứng trùng hợp polymer.
phản ứng tăng mạch polymer.
phản ứng cắt mạch polymer.
phản ứng giữ nguyên mạch polymer.
Điểm chớp cháy của chất cháy là nhiệt độ thấp nhất ở áp suất khí quyển mà chất cháy bị đốt nóng tới mức tạo ra lượng hơi đủ lớn để bốc cháy trong không khí khi gặp nguồn lửa. Điểm chớp cháy được sử dụng để phân biệt chất lỏng dễ cháy với chất lỏng có thể gây cháy. Chất lỏng có điểm chớp cháy nhỏ hơn 37{,}8^\circ C gọi là chất lỏng dễ cháy, chất lỏng có điểm chớp cháy lớn hơn 37{,}8^\circ C gọi là chất lỏng có thể gây cháy. Cho số liệu về điểm chớp cháy của một số chất trong bảng sau: (Có bảng số liệu). Trong bảng trên, số chất lỏng dễ cháy là :
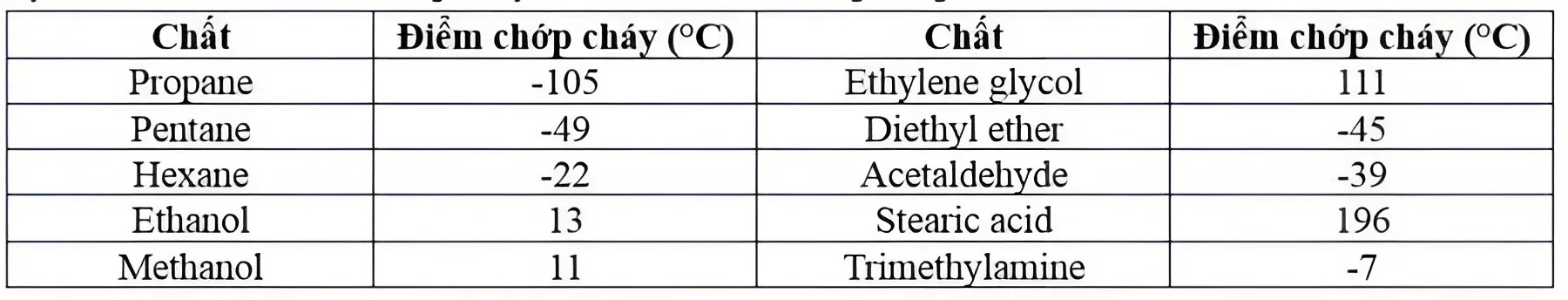
7
8
6
9
Cho các phát biểu sau về đơn chất và hợp chất của kim loại nhóm IA: (1) Trong công nghiệp, baking soda và soda được sản xuất bằng phương pháp Solvay. (2) Lithium là kim loại nhẹ nhất trong các kim loại. (3) Kim loại sodium thường được bảo quản bằng cách ngâm trong dầu hỏa khan. (4) Trong hợp chất, tất cả nguyên tố kim loại nhóm IA đều có số oxi hóa là +1. Số phát biểu đúng là :
1
2
4
3
Cho phương trình nhiệt hóa học: CO(g) + \dfrac{1}{2}O_2(g) \rightarrow CO_2(g)\ \Delta H^{\circ}_{298} = -283{,}0\ \text{kJ}. Biết nhiệt tạo thành chuẩn của CO_2(g) là \Delta H^{\circ}_{f\ 298} = -393{,}5\ \text{kJ/mol}. Nhiệt tạo thành chuẩn của CO(g) là :
-110{,}5\ \text{kJ/mol}.
-141{,}5\ \text{kJ/mol}.
-221{,}0\ \text{kJ/mol}.
+110{,}5\ \text{kJ/mol}.
Để bảo vệ vỏ tàu biển làm bằng thép, người ta thường gắn vào vỏ tàu (phần chìm dưới nước) tấm kim loại nào sau đây ?
Ag.
Cu.
Zn.
Na.
Trong hợp chất SO_3, số oxi hóa của sulfur là :
+6.
+2.
+3.
+5.
Arachidonic acid (ARA) là một acid béo thiết yếu có vai trò quan trọng trong việc kích hoạt các dây thần kinh trong não và hỗ trợ cho nhiều chức năng khác như hệ miễn dịch, tạo mạch máu, phát triển xương và hoạt động của tim. ARA có công thức cấu tạo như bên. Cho các phát biểu sau : (1) ARA thuộc loại acid béo omega-6. (2) Trong một phân tử ARA có 11 nhóm methylene. (3) Triester của glycerol với ARA có công thức phân tử C_{63}H_{92}O_6. (4) a mol ARA tác dụng tối đa với 4a mol H_2 (xt, t^\circ, p). Số phát biểu đúng là :
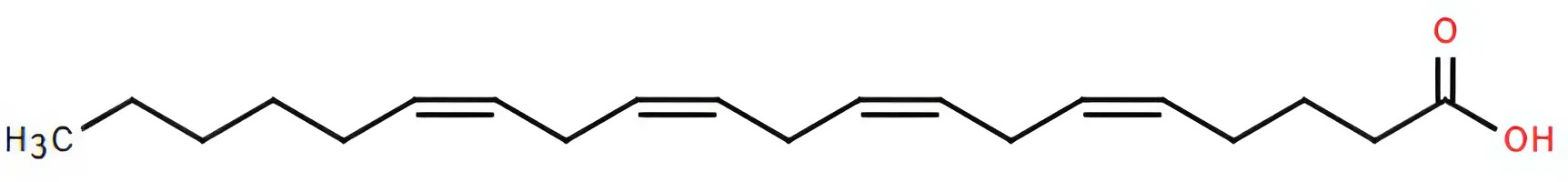
2
4
1
3
Thả một đinh sắt nặng $$m_1$$ gam đã được đánh sạch bề mặt vào cốc chứa dung dịch copper (II) sulfate màu xanh. Sau một thời gian thấy toàn bộ lượng đồng sinh ra đã bám vào
đinh sắt
thực chất là phần đinh sắt chưa phản ứng
. Lấy “đinh sắt” ra khỏi cốc dung dịch, sấy khô, đem cân được $$m_2$$ gam. Phát biểu nào sau đây đúng ?
Màu xanh của dung dịch copper (II) sulfate nhạt dần.
Phản ứng xảy ra là 2Fe(s) + 3Cu^{2+}(aq) \rightarrow 2Fe^{3+}(aq) + 3Cu(s).
Fe vô hóa ion Cu^{2+} trong dung dịch.
So sánh, thu được kết quả m_2 < m_1.
Hợp chất nào sau đây là ester ?
CH₃CH₂COOH.
CH₃CH₂OH.
CH₃CH₂COOCH₃.
CH₃CH₂CHO.
Cho hệ cân bằng trong một bình kín: N_2(g) + O_2(g) \rightleftharpoons 2NO(g)\ \Delta H^{\circ}_{298} > 0. Cân bằng trên chuyển dịch theo chiều thuận khi
thêm khí NO vào hệ.
giảm áp suất của hệ.
tăng nhiệt độ của hệ.
thêm chất xúc tác vào hệ.
Ester X có công thức phân tử C_5H_{10}O_2. Thủy phân X trong dung dịch H_2SO_4 loãng, đun nóng, thu được ethyl alcohol và chất hữu cơ Y. Công thức của Y là
HCOOH.
C_3H_7COOH.
C_2H_5COOH.
CH₃COOH.
Carbohydrate nào sau đây thuộc loại disaccharide?
Tinh bột.
Glucose.
Saccharose.
Cellulose.
Công thức phân tử của dimethylamine là
C_2H_8N_2.
C_4H_{11}N.
C_2H_6N_2.
C_2H_7N.
Nước muối sinh lí là dung dịch của chất X với nồng độ 0,9% được dùng trong việc ngăn ngừa nguy cơ mất muối do đổ quá nhiều mồ hôi, sau phẫu thuật, do tiêu chảy hay các nguyên nhân khác. X là muối nào sau đây?
Na₂SO₄.
NaNO₃.
NaClO.
NaCl.
Cho thế điện cực chuẩn của một số cặp oxi hoá - khử ở bảng sau: (Có bảng dữ liệu). Trong số các kim loại Fe, Cu, Mg, Zn, Ag, có bao nhiêu kim loại tác dụng với dung dịch Fe(NO_3)_3 ở điều kiện chuẩn?

2
4
3
5
Công thức chung của alkane là
C_nH_{2n}\ (n \geq 2).
C_nH_{2n-6}\ (n \geq 6).
C_nH_{2n+2}\ (n \geq 1).
C_nH_{2n-2}\ (n \geq 2).
Phần II
Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Nấm men là chất xúc tác cho phản ứng lên men rượu trong điều kiện không có khí oxygen. Quá trình lên men là một quá trình tỏa nhiệt. Từ 250 gam glucose, thực hiện quá trình lên men rượu trong phòng thí nghiệm, kết quả biểu thị theo đồ thị bên.
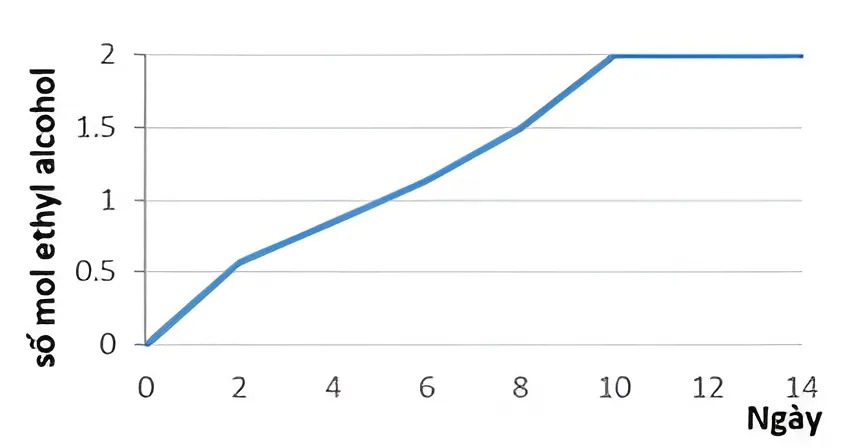
Phát biểu
Đúng
Sai
a
Trong quá trình lên men, ngoài ethyl alcohol thì còn có thể tạo thành một số sản phẩm như CH₃CHO, CH₃COOH.
b
Phương trình lên men glucose là C_6H_{12}O_6 \rightarrow 2C_2H_5OH + 2CO_2.
c
Glucose thuộc loại disaccharide.
d
Đến ngày thứ 10, hiệu suất quá trình lên men rượu là 78%.
Dipeptide Phe-Tyr có cấu trúc như hình. Hỗn hợp của dipeptide Phe-Tyr và hai amino acid thành phần (Phe và Tyr) đã được tiến hành điện di trong dung dịch đệm pH = 12. Tại điều kiện này, thông tin của ba chất được cung cấp như sau (bảng dữ liệu). Vào cuối thí nghiệm thu được những kết quả sau: Ba chấm P, R, S là đại diện cho ba chất Phe hoặc Tyr hoặc Phe-Tyr (không theo thứ tự). Các chấm R và S vẫn nằm rất gần nhau.
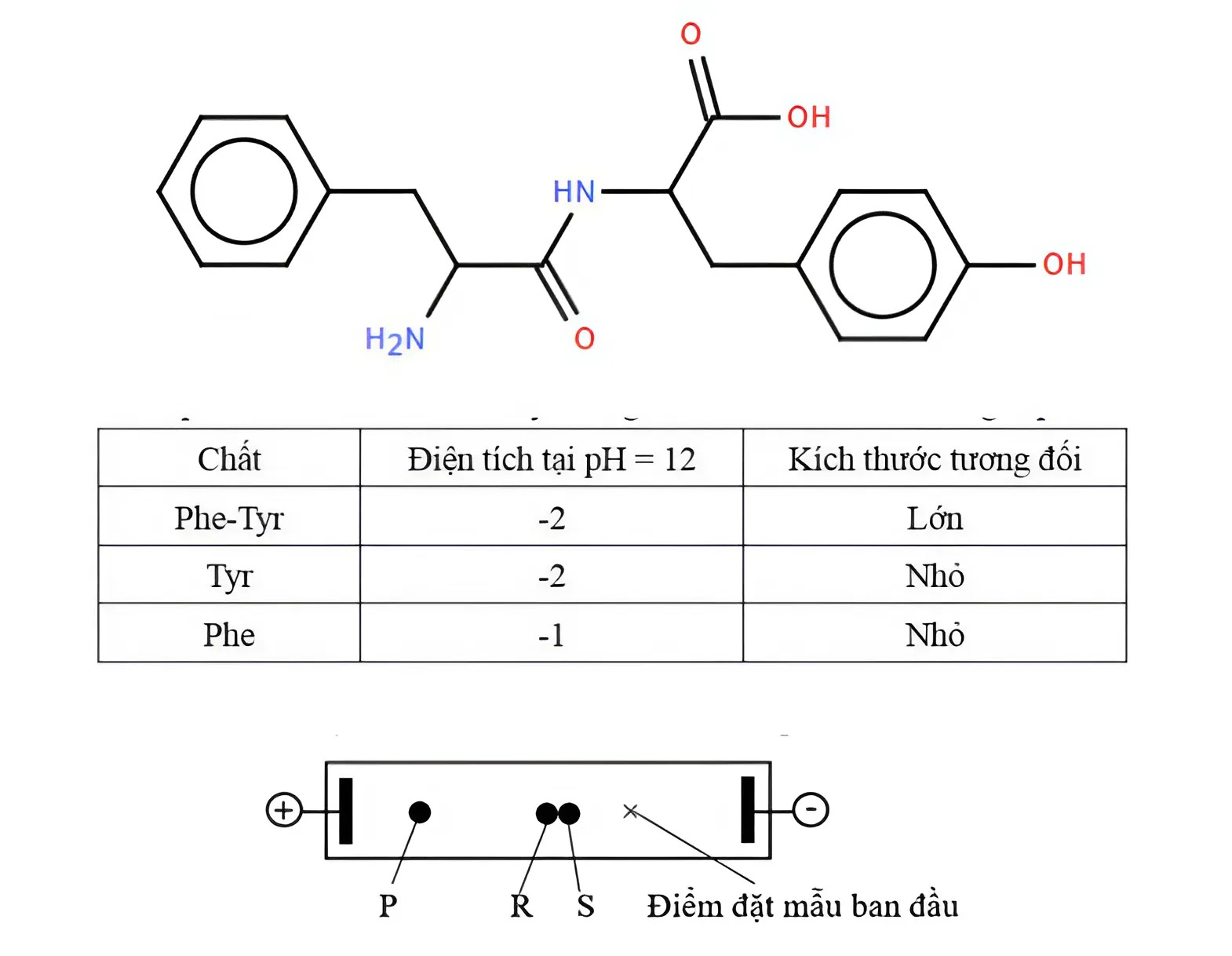
Phát biểu
Đúng
Sai
a
Kích thước phân tử càng lớn thì khả năng di chuyển về phía điện cực càng kém.
b
Chất có giá trị điện tích càng nhỏ thì khả năng di chuyển về phía điện cực càng tốt.
c
Chất P là Tyr.
d
Amino acid Phe có khả năng di chuyển với tốc độ gần như dipeptide Phe-Tyr trong điện trường.
Tiến hành thí nghiệm điện phân dung dịch CuSO_4 theo các bước: (Bước 1, Bước 2, Bước 3 như hình bên). Sau một khoảng thời gian thu được 0,0025 mol khí ở anode. Sau thời gian 3t giây thu được 0,0125 mol khí thoát ra ở cả hai điện cực và dung dịch X.
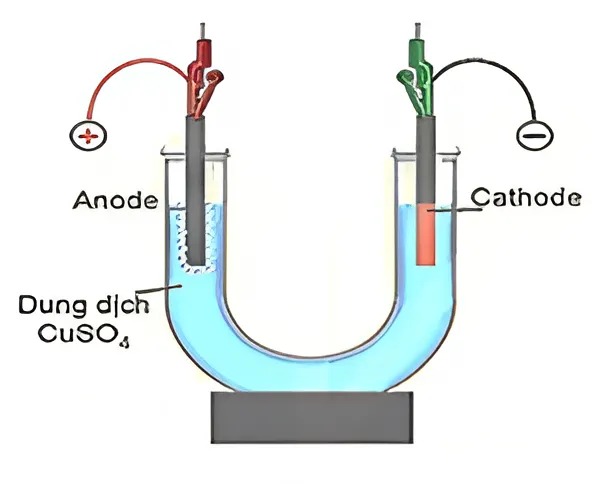
Phát biểu
Đúng
Sai
a
Phản ứng trong bình điện phân là 2CuSO_4 + 2H_2O \rightarrow 2Cu + O_2 + 2H_2SO_4.
b
Tại anode, xuất hiện bọt khí hydrogen trên bề mặt điện cực.
c
Khối lượng dung dịch X giảm 0,89 gam so với dung dịch CuSO_4 ban đầu.
d
Để mạ đồng lên chiếc chìa khóa bằng sắt theo phương pháp điện phân thì trong sơ đồ thí nghiệm trên phải sử dụng anode là thanh đồng, cathode là chìa khóa và dung dịch điện phân là dung dịch CuSO_4.
Năm 1965, trong quá trình tổng hợp thuốc chống loét dạ dày, nhà hóa học James M. Schlatter đã vô tình phát hiện một chất làm ngọt nhân tạo với tên thương mại gọi là “Aspartame” có cấu tạo như hình bên. Aspartame ngọt hơn khoảng 200 lần so với đường ăn thông thường và thường được sử dụng trong đồ uống, thực phẩm ăn kiêng. Tổ chức Y tế Thế giới (WHO) khuyến nghị giới hạn hằng ngày của aspartame.
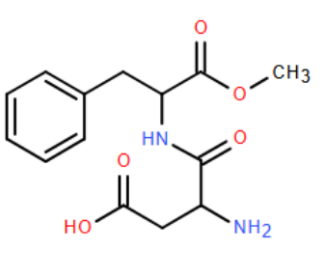
Phát biểu
Đúng
Sai
a
Aspartame là ester của methanol với dipeptide (tạo bởi amino acid HOOCCH(NH₂)CH₂COOH và C₆H₅CH₂CH(NH₂)COOH).
b
Không nên sử dụng quá nhiều đồ uống có chất làm ngọt nhân tạo aspartame liên tục trong thời gian dài.
c
Tổng số cặp electron hóa trị chưa tham gia liên kết của nguyên tử N trong một phân tử aspartame là 2.
d
Một phân tử aspartame có 39 liên kết \sigma.
Phần III
Thí sinh trả lời từ câu 1 đến câu 6.
Trong công nghiệp, kim loại sắt được sản xuất bằng phương pháp nhiệt luyện quặng hematite với hiệu suất phản ứng là 80%. Để sản xuất được 8,4 tấn sắt cần dùng bao nhiêu tấn quặng hematite, biết quặng hematite có chứa 60% Fe_2O_3?
Khảo sát một số tính chất của ba chất X, Y, Z được ghi lại trong bảng sau: (nhiệt độ nóng chảy và quỳ tím). Biết X, Y, Z là một trong ba chất glycine, alanine, glutamic acid. Thủy phân hoàn toàn 1 mol peptide A thu được 2 mol X, 1 mol Y và 2 mol Z. Mặt khác, nếu thủy phân không hoàn toàn A thu được hỗn hợp các peptide và các α-amino acid, trong đó có tripeptide X–Z–Z. Có bao nhiêu công thức cấu tạo của A với amino acid đầu N là alanine thỏa mãn tính chất trên?
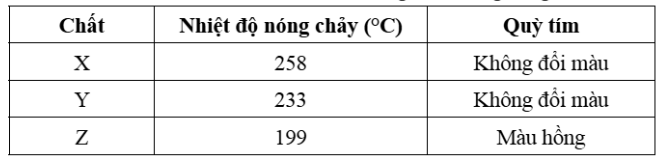
Trong phòng thí nghiệm, soda (Na_2CO_3) khi để lâu ngày bị chuyển hóa và hút ẩm tạo thành hỗn hợp X gồm Na_2CO_3, NaHCO_3 và H_2O. Hòa tan hoàn toàn một lượng X trong nước thu được 100 mL dung dịch Y. Tiến hành các thí nghiệm như sau: Thí nghiệm 1: Cho 50 mL dung dịch HCl 1M vào 10 mL dung dịch Y, sau đó đun nhẹ. Để trung hòa dung dịch thu được cần dùng 50 mL dung dịch NaOH 0,2M. Thí nghiệm 2: Cho 20 mL dung dịch NaOH 1M vào 10 mL dung dịch Y, sau đó thêm tiếp dung dịch BaCl₂ đến dư và lọc bỏ kết tủa. Để trung hòa nước lọc cần dùng 30 mL dung dịch HCl 0,2M. Biết các phản ứng xảy ra hoàn toàn. Phần trăm Na_2CO_3 đã bị chuyển hóa thành NaHCO_3 là bao nhiêu?
Điện phân dung dịch NaCl bão hòa là một phương pháp thu được những sản phẩm có tính ứng dụng rất cao trong ngành công nghiệp sản xuất. – Để điều chế chlorine và xút thì trong quá trình điện phân dùng màng ngăn giữa các điện cực. – Để điều chế nước Javel thì trong quá trình điện phân không dùng màng ngăn giữa các điện cực. Cho các phát biểu sau: (1) Theo thời gian, trong hai quá trình điện phân trên, nồng độ ion Na+ không thay đổi. (2) Trong quá trình điện phân để điều chế nước Javel, số mol NaCl và NaClO luôn bằng nhau. (3) Trong hai quá trình điện phân trên, pH của dung dịch đều tăng lên. (4) Trong hai quá trình điện phân trên, tại cathode đều xảy ra bán phản ứng khử H2O. Liệt kê theo thứ tự tăng dần các phát biểu đúng?
Cho các nguyên liệu sau: CH₃[CH₂]₁₆COONa, CH₃[CH₂]₁₄COOK, dịch đun từ quả bồ hòn, CH₃COOH, CH₃[CH₂]₁₁C₆H₄SO₃Na, CH₃COONa. Có bao nhiêu nguyên liệu có tính giặt rửa?
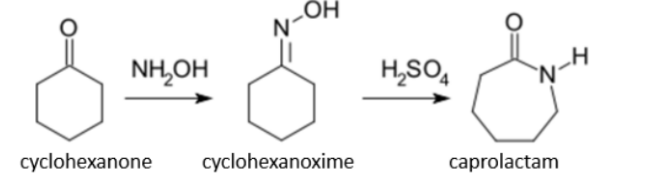
Caprolactam được tổng hợp từ cuối thế kỷ XIX. Hiện nay, nhu cầu sản xuất caprolactam trên thế giới khoảng 10 triệu tấn/năm; 90% trong đó dùng để tổng hợp to capron. Trong công nghiệp, caprolactam được điều chế theo sơ đồ sau (có hình). Giả sử hiệu suất trung bình của cả quá trình trên là 65%. Mỗi năm, cần bao nhiêu triệu tấn cyclohexanone để đáp ứng nhu cầu sản xuất caprolactam trên thế giới (làm tròn đến hàng phần mười)?
Xem đáp án và bài mẫu
Answer key
Tên gọi của polymer (-CH_2-CH=CH-CH_2-)_n là :
cao su buna.
cao su buna-S.
cao su buna-N.
cao su isoprene.
Giải thích câu 1
Giải thích chi tiết
😎 Cùng DOL xem qua cách giải câu này nhé!
📃 Thông tin đề bài cho:
Công thức cấu tạo của polymer: (-CH_2-CH=CH-CH_2-)_n
❓ Hiểu câu hỏi:
Câu hỏi yêu cầu đặt tên cho polymer có công thức lặp lại như trên.
Cần nhận diện monomer và tên thương mại tương ứng của polymer.
🔎 Hướng dẫn cách làm:
Xác định monomer:
Mạch lặp là -CH_2-CH=CH-CH_2-, tương ứng đơn vị monomer là buta-1,3-diene (CH₂=CH–CH=CH₂).
Nhận biết polymer:
Khi trùng hợp buta-1,3-diene, ta được polybutadiene.
Tên thương mại:
Polybutadiene còn gọi là “cao su Buna” hay “butadiene rubber.”
Đối chiếu với các lựa chọn:
“cao su Buna-S” là copolymer giữa butadiene và styrene.
“cao su Buna-N” là copolymer giữa butadiene và acrylonitrile.
“cao su isoprene” là polymer hóa isoprene (monomer khác).
✅ Đáp án: \text{cao su buna.}
❌ Các đáp án khác:
B. cao su buna-S: là copolymer butadiene–styrene, không phải polybutadiene thuần.
C. cao su buna-N: là copolymer butadiene–acrylonitrile, không đúng.
D. cao su isoprene: polymer của isoprene (không phải butadiene).
Hiện bạn đang luyện đề THPTQG Môn Hoá thuộc chuyên mục luyện thi THPT Quốc gia. Để tiếp tục rèn luyện với nhiều đề thi khác, bạn có thể tham khảo những đề liên quan khác bên dưới.


