Đáp án & giải thích đề môn Hoá k12
Đề thi thử môn Hóa Lớp 12 Sở GD&ĐT Bắc Ninh - năm học 2025-2026 - Mã đề 01

DOL THPT
Mar 27, 2026
Đề thi thử môn Hóa Lớp 12 Sở GD&ĐT Bắc Ninh - năm học 2025-2026 - Mã đề 01 được thiết kế dưới hình thức thi thử trắc nghiệm online, giúp bạn hiểu rõ cấu trúc đề thi. Nền tảng chấm điểm tự động sau khi bạn nộp bài, đồng thời lưu kết quả bài làm để bạn dễ theo dõi tiến độ luyện thi, đi kèm đáp án giải thích rõ ràng và tải PDF đề thi miễn phí HOÀN TOÀN MIỄN PHÍ.

Đề thi thử môn Hóa Lớp 12 Sở GD&ĐT Bắc Ninh - năm học 2025-2026 - Mã đề 01
Download PDF
Miễn phí dowload
Câu hỏi đề bài
28 Câu hỏi
Phần I
Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Cho các phát biểu sau: (1) Độ dinh dưỡng của phân đạm, phân lân và phân kali tính theo phần trăm khối lượng tương ứng của N_2O_5; P_2O_5 và K_2O. (2) Người ta không bón phân urea kèm với vôi. (3) Phân lân chứa nhiều phospho nhất là superphosphate kép. (4) Bón nhiều phân đạm ammonium sẽ làm đất chua. (5) Quặng phosphorite có thành phần chính là Ca_3(PO_4)_2. Trong các phát biểu trên, số phát biểu đúng là
4
2
5
3
Có thể tạo ra một hợp chất ester X có mùi thơm giống quả táo từ sự kết hợp của methanol và butanoic acid. Công thức phân tử của ester X là
C_3H_6O_2
C_4H_{10}O_2
C_5H_{10}O_2
C_2H_4O_2
Cho đồ thị. Khi sử dụng đồ uống có đường, nồng độ glucose trong máu tăng cao nhất sau khi
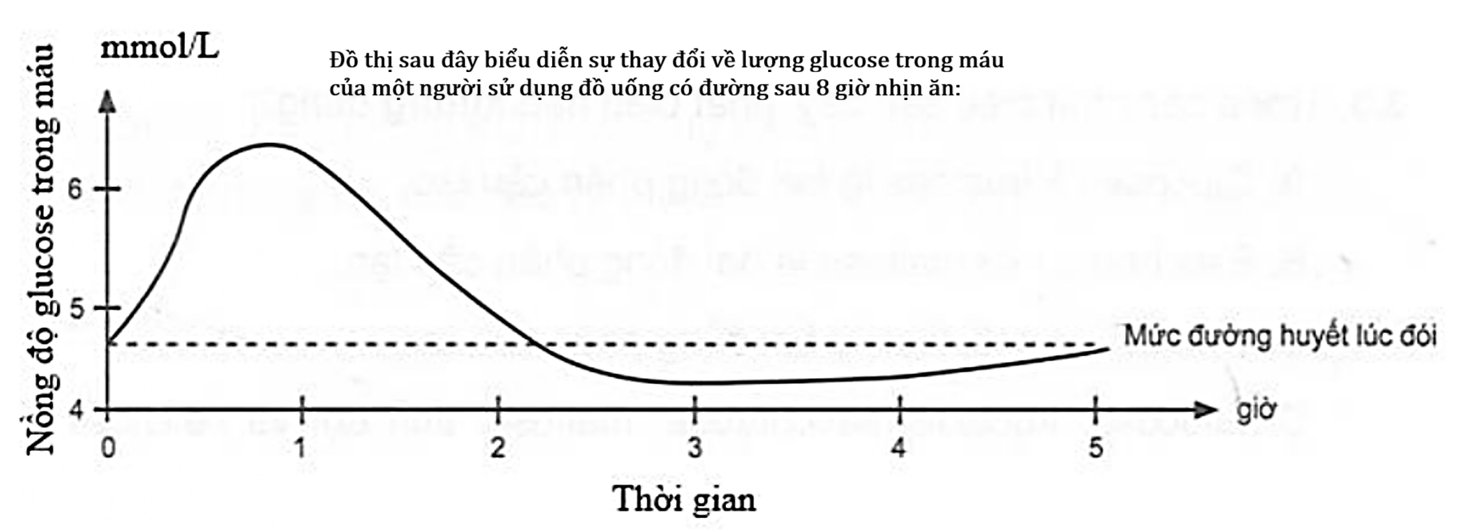
sử dụng khoảng 50 phút
sử dụng khoảng 2 giờ
sử dụng khoảng 20 phút
sử dụng khoảng 3 giờ
Nước Javel là sản phẩm của quá trình
sục khí chlorine vào vôi sữa
điện phân dung dịch NaOH không có màng ngăn
điện phân dung dịch NaCl có màng ngăn giữa hai điện cực
điện phân dung dịch NaCl không có màng ngăn giữa hai điện cực
Khi thủy phân saccharose, sản phẩm thu được là
fructose
glucose và fructose
tinh bột
glucose
Trong dung dịch K_2Cr_2O_7 tồn tại cân bằng: Cr_2O_7^{2-} + H_2O \rightleftharpoons 2CrO_4^{2-} + 2H^+. Cho vài giọt dung dịch chất X vào dung dịch K_2Cr_2O_7 thì dung dịch chuyển dần từ màu da cam sang màu vàng. X có thể là chất nào sau đây?
KCl
KOH
H_2SO_4
K_2SO_4
Cho các alcohol sau: CH_3OH; C_2H_5OH; HOCH_2CH_2OH; CH_2OHCHOHCH_2OH; CH_2OHCH_2CH_2OH. Số alcohol không hòa tan được Cu(OH)_2 là
1
3
4
2
Có một loại quặng pyrite chứa 96% FeS_2. Nếu mỗi ngày nhà máy sản xuất 100 tấn dung dịch sulfuric acid 98% thì cần m tấn quặng pyrite trên và biết hiệu suất của cả quá trình sản xuất H_2SO_4 là 90%. Giá trị của m là
69,44
68,44
70,44
67,44
Cho 5,6 gam CO và 5,4 gam H_2O vào một bình kín dung tích không đổi 10 L. Nung nóng bình ở 830°C để hệ đạt đến trạng thái cân bằng. Phản ứng xảy ra: CO(g) + H_2O(g) \rightleftharpoons CO_2(g) + H_2(g). Biết K_c = 1. Nồng độ H_2O (M) ở trạng thái cân bằng là
0,18
0,018
0,12
12
Cho cân bằng hóa học: PCl_5(g) \rightleftharpoons PCl_3(g) + Cl_2(g), \Delta_rH^\circ_{298} > 0. Yếu tố không ảnh hưởng đến cân bằng hóa học này là
Chất xúc tác
Nhiệt độ
Nồng độ
Áp suất
Cho các chất sau: H_2O (1), C_2H_5OH (2), C_6H_5OH (3), CH_3COOH (4). Độ linh động của nguyên tử hydrogen trong nhóm –OH tăng dần theo thứ tự là
(1) < (2) < (4) < (3)
(2) < (1) < (3) < (4)
(1) < (2) < (3) < (4)
(2) < (1) < (4) < (3)
Tên gọi của CH_2=CHCOOC_6H_5 là
Benzyl acrylate
Phenyl methacrylate
Phenyl acrylate
Phenyl propionate
“Saccharose và …(1)… là hai disaccharide, có cùng công thức phân tử là …(2)…”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
maltose, C_6H_{12}O_6
maltose, C_{12}H_{22}O_{11}
cellulose, (C_6H_{10}O_5)_n
glucose, C_6H_{12}O_6
Ester X được tạo bởi methyl alcohol và acetic acid. Công thức của X là
HCOOCH_3
CH_3COOCH_3
CH_3COOC_2H_5
HCOOC_2H_5
Ammonia được tạo ra bằng cách cho nitrogen phản ứng với hydrogen với sự có mặt của chất xúc tác iron. Phương trình phản ứng tạo ammonia diễn ra như sau: N_2(g) + 3H_2(g) \rightleftharpoons 2NH_3(g). Biết năng lượng liên kết (kJ/mol) ở 25°C của một số liên kết được cho trong bảng:

-80
-959
1476
993
Nhiệt độ ngọn lửa là nhiệt độ cao nhất có thể tạo ra bởi phản ứng cháy của chất cháy trong không khí ở áp suất khí quyển. Nhiệt độ ngọn lửa cao nhất khi cháy trong không khí của methane khoảng 1963°C. Methane trong khí gas trộn với oxygen không khí gây nổ rất mạnh do phản ứng: CH_4(g) + 2O_2(g) \rightarrow CO_2(g) + 2H_2O(g) (*); \Delta_rH^\circ_{298}=-571,6 \text{kJ} Phản ứng này tỏa rẩt nhiều nhiệt, các sản phẩm bị đốt nóng mạnh. Cho các phát biểu sau: (a) Tổng số mol khí trước và sau phản ứng không thay đổi. (b) Sự nổ xảy ra là do phản ứng (*) tỏa nhiệt nhiệt, thể tích tăng đột ngột. (c) CH_4 kết hợp với O_2 theo tỉ lệ khối lượng 1 : 2 sẽ tạo ra hỗn hợp nổ. (d) Việc sử dụng nước để chữa cháy nhằm mục đích hạ nhiệt độ của hỗn hợp. Các phát biểu đúng là
(a), (d)
(a), (b), (d)
(a), (b), (c)
(a), (c), (d)
Phản ứng giữa ethylene với HBr : CH_2 = CH_2 + HBr \rightarrow CH_3CH_2Br .
Giai đoạn 1 của phản ứng là quá trình H^+ (tác nhân electrophile ()) phản ứng với C=C tạo carbocation trung gian (Như hình). () tác nhân electrophile là những chất "yêu thích" electron, chúng thường là các chất mang điện tích dương hoặc có trung tâm mang một phần điện tích dương.
Giai đoạn 2 là quá trình kết hợp giữa carbocation với tác nhân X (như hình). Trong các phát biểu sau, phát biểu nào đúng?
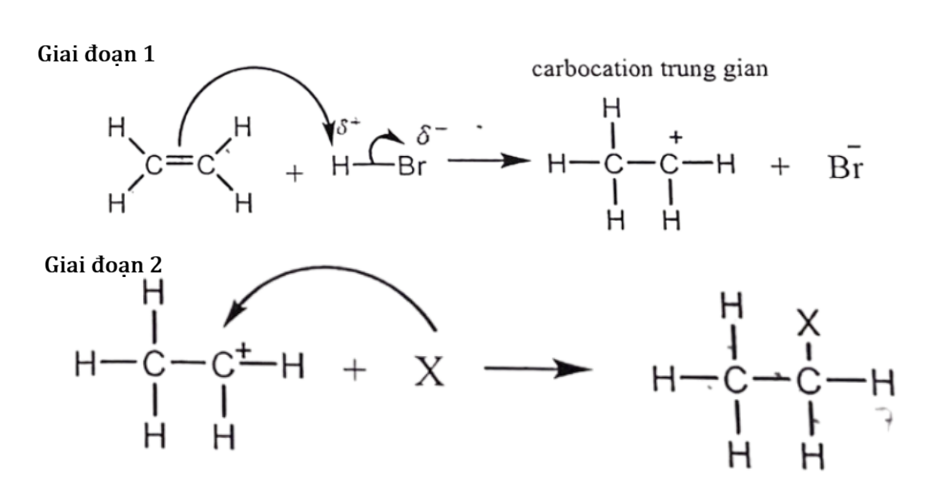
Hướng mũi tên cong biểu diễn sự chuyển dịch của electron
Giai đoạn 2, tác nhân X phản ứng với carbocation là cation Br^+
Giai đoạn 1 có sự hình thành liên kết \pi
Sản phẩm CH_3CH_2Br nhiều hơn chất ban đầu 1 liên kết \sigma
Số liên kết \sigma và liên kết \pi trong phân tử acetylene (C_2H_2) lần lượt là
3 và 2
2 và 1
1 và 1
3 và 1
Phần II
Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Đun hỗn hợp ethylene glycol và carboxylic acid X (phân tử chỉ có nhóm –COOH) với xúc tác H_2SO_4 đặc, thu được hỗn hợp sản phẩm hữu cơ, trong đó có chất hữu cơ Y mạch hở. Đốt cháy hoàn toàn 3,95 gam Y cần 4,00 gam O_2, thu được CO_2 và H_2O theo tỉ lệ mol tương ứng 2 : 1. Biết Y có công thức phân tử trùng với công thức đơn giản nhất, Y phản ứng được với NaOH theo tỉ lệ mol tương ứng 1 : 2. Cho các phát biểu sau:
Phát biểu
Đúng
Sai
a
X có đồng phân hình học.
b
Y tham gia được phản ứng cộng với Br_2 theo tỉ lệ mol tương ứng 1 : 2.
c
Y không có phản ứng tráng bạc.
d
Tổng số nguyên tử hydrogen trong hai phân tử X, Y bằng 8.
Muối Mohr có công thức (NH_4)_2Fe(SO_4)_2.6H_2O. Để xác định độ tinh khiết của một loại muối Mohr (cho rằng trong muối Mohr chỉ có muối kép ngậm nước nêu trên và tạp chất trơ), một học sinh tiến hành các thí nghiệm sau: Cân chính xác 7,237 gam muối Mohr, pha thành 100 mL dung dịch X. Lấy chính xác 10 mL dung dịch X, thêm 10 mL dung dịch H_2SO_4 10%, được dung dịch Y. Chuẩn độ dung dịch Y bằng dung dịch chuẩn KMnO_4 0,023 M. Thực hiện chuẩn độ 3 lần. Kết quả đạt được như bảng. Những phát biểu sau là đúng hay sai?

Phát biểu
Đúng
Sai
a
Theo kết quả chuẩn độ ở trên, trong số các giá trị: 93,32; 98,45; 97,36; 99,87, độ tinh khiết (% khối lượng) của muối Mohr có giá trị gần nhất với 98,45.
b
Trong mỗi lần chuẩn độ, dung dịch KMnO_4 được xem là phản ứng vừa đủ với muối Mohr (điểm dừng) khi giọt dung dịch KMnO_4 cuối cùng nhỏ vào dung dịch Y không mất màu.
c
Dung dịch H_2SO_4 được thêm vào dung dịch chuẩn độ để tạo môi trường acid, giúp phản ứng xảy ra theo hướng tạo thành Mn^{2+}.
d
Có thể thay dung dịch H_2SO_4 đã dùng bằng dung dịch acid mạnh như HCl, HNO_3 nhưng phải đảm bảo lượng H^+ dư sau phản ứng.
Trong nước mưa acid thường có pH = 4 đến 5. pH thấp trong nước mưa acid chủ yếu là do có chứa các acid như HNO_3, H_2SO_4. Trong tự nhiên, HNO_3 còn được tạo ra từ N_2 theo sơ đồ chuyển hóa:
N_2 \xrightarrow{+O_2} NO \xrightarrow{+O_2} NO_2 \xrightarrow{+O_2 + H_2O} HNO_3.
Phát biểu
Đúng
Sai
a
Một cơn mưa acid, nước mưa có pH = 4 thì nồng độ HNO_3 có trong nước mưa đó là 10^{-4}\ M.
b
Trong thực tế để điều chế ester từ acid và alcohol tương ứng người ta sử dụng HNO_3 làm chất xúc tác.
c
HNO_3 sinh ra từ quá trình trên sẽ cung cấp một lượng phân đạm cho cây trồng ở dạng NO_3^-.
d
Dung dịch HNO_3 có pH = 3 cần phải pha loãng 20 lần để thu được dung dịch HNO_3 có pH = 5.
Một học sinh tiến hành tổng hợp isoamyl acetate (thành phần chính của dầu chuối) từ acetic acid và isoamyl alcohol theo phương trình hóa học đã cho. Sau thí nghiệm, tiến hành phân tách sản phẩm. Ghi phổ hồng ngoại của acetic acid, isoamyl alcohol và isoamyl acetate. Cho biết số sóng hấp thụ đặc trưng của một số liên kết trên phổ hồng ngoại như bảng.
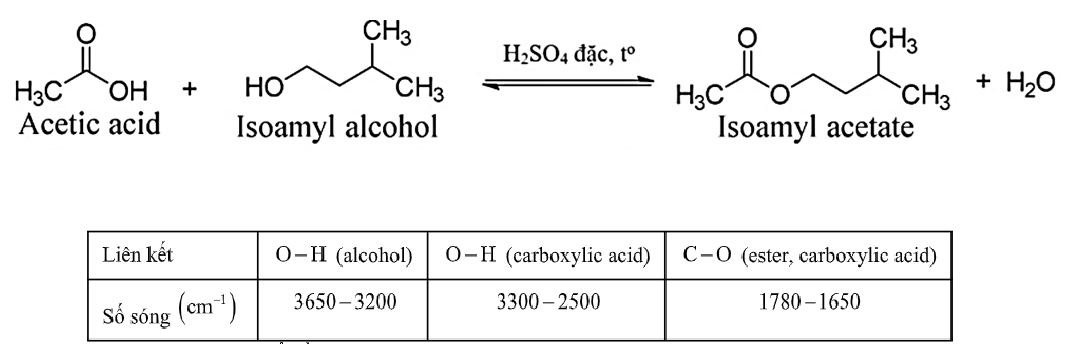
Phát biểu
Đúng
Sai
a
Dựa vào phổ hồng ngoại, phân biệt được acetic acid, isoamyl alcohol và isoamyl acetate.
b
Phổ hồng ngoại có số sóng hấp thụ ở khoảng 1750 cm^{-1} mà không có số sóng hấp thụ đặc trưng của liên kết H là phổ của isoamyl acetate.
c
Phổ hồng ngoại có số sóng hấp thụ ở khoảng 3350 cm^{-1} là phổ của isoamyl alcohol.
d
Phản ứng tổng hợp trong thí nghiệm này là phản ứng thủy phân ester.
Phần III
Thí sinh trả lời từ câu 1 đến câu 6.
Một hộ gia đình mua than đá làm nhiên liệu đun nấu và trung bình mỗi ngày dùng hết 2,0 kg than đá. Giả thiết loại than đá này chứa 90% carbon và 1,2% sulfur về khối lượng, còn lại là các tạp chất trơ không cháy. Cho các phản ứng: C(s)+O_2(g)\xrightarrow{t^\circ}CO_2(g), \Delta_rH^\circ_{298}=-393,5\text{ kJ/mol}; S(s)+O_2(g)\xrightarrow{t^\circ}SO_2(g), \Delta_rH^\circ_{298}=-296,8\text{ kJ/mol}. Nhiệt lượng cung cấp cho hộ gia đình từ quá trình đốt than trong một ngày tương đương bao nhiêu số điện? (Biết cứ 1 số điện = 1kWh = 3600 kJ?) Biết rằng hiệu suất sử dụng nhiệt là 37,5%. (Kết quả làm tròn đến hàng đơn vị).
Một mẫu nước thải của nhà máy sản xuất có pH=3. Để thải ra ngoài môi trường thì cần phải tăng pH lên từ 5,8 đến 8,6 (theo đúng quy định), nhà máy phải dùng vôi sống thả vào nước thải. Để nâng pH của 5 m^3 nước thải từ 3 lên 7 cần dùng m gam vôi sống. Tính giá trị m? (Bỏ qua sự thủy phân của các muối, kết quả làm tròn đến hàng đơn vị).
Một nhà hóa học trẻ quyết định nghiên cứu về sự nhiệt phân muối cobalt(II) sulfate pentahydrate (CoSO_4.5H_2O) để phục vụ cho dự án khoa học của mình. Để tiến hành, anh ta đặt một mẫu muối màu hồng tươi vào thiết bị phân tích nhiệt trọng (TGA) và bắt đầu quá trình đun nóng đến 950°C. Kết quả là anh ta nhận được đồ thị về sự phụ thuộc của khối lượng mẫu vào nhiệt độ như trong hình bên. Số nguyên tử trong một phân tử mẫu ở 520°C là bao nhiêu?
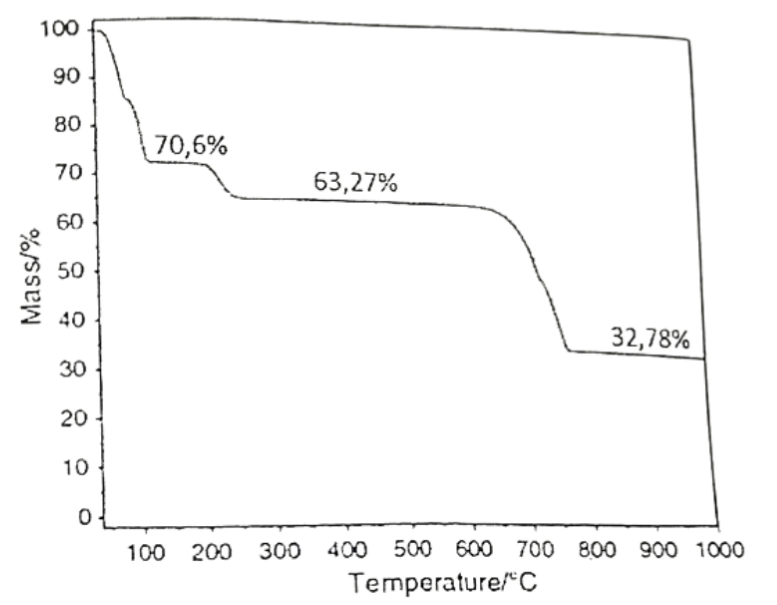
Cho salixylic acid (o-hitroxibenzoic acid) phản ứng với anhidrit acetic, thu được axetylsalixylic acid (o-CH_3COO-C_6H_4-COOH) dùng làm thuốc cảm (aspirin). Để phản ứng hoàn toàn với 43,2 gam axetylsalixylic acid cần vừa đủ V lít dung dịch NaOH 1 M. Giá trị của V là bao nhiêu? (Kết quả làm tròn đến hàng phần trăm).
Thủy phân hoàn toàn chất béo X trong dung dịch NaOH dư, thu được glycerol, sodium stearate và oleate. Có bao nhiêu đồng phân cấu tạo của chất béo X?.
Carboxylic acid X hai chức (có phần trăm khối lượng của oxygen nhỏ hơn 70%), Y và Z là hai alcohol đồng đẳng kế tiếp (M_Y
Xem đáp án và bài mẫu
Answer key
Cho các phát biểu sau: (1) Độ dinh dưỡng của phân đạm, phân lân và phân kali tính theo phần trăm khối lượng tương ứng của N_2O_5; P_2O_5 và K_2O. (2) Người ta không bón phân urea kèm với vôi. (3) Phân lân chứa nhiều phospho nhất là superphosphate kép. (4) Bón nhiều phân đạm ammonium sẽ làm đất chua. (5) Quặng phosphorite có thành phần chính là Ca_3(PO_4)_2. Trong các phát biểu trên, số phát biểu đúng là
4
2
5
3
Giải thích câu 1
Giải thích chi tiết
😎 Cùng DOL xem qua cách giải câu này nhé!
📃 Thông tin đề bài cho:
Các phát biểu liên quan đến:
cách đánh giá độ dinh dưỡng của phân bón
cách sử dụng phân bón
thành phần hóa học của quặng và phân lân
Yêu cầu: xác định số phát biểu đúng.
❓ Hiểu câu hỏi:
Cần kiểm tra từng phát biểu đúng/sai theo kiến thức Hóa học – Công nghệ nông nghiệp phổ thông, sau đó đếm số phát biểu đúng.
🔎 Hướng dẫn cách làm:
(1) Độ dinh dưỡng của phân đạm, phân lân và phân kali tính theo phần trăm khối lượng tương ứng của N_2O_5; P_2O_5 và K_2O. → Sai.
Phân đạm được tính theo %N, không phải N_2O_5.
P_2O_5 và K_2O chỉ dùng cho phân lân và phân kali.
(2) Người ta không bón phân urea kèm với vôi. → Đúng. Vôi làm urea bị phân hủy nhanh, giải phóng NH_3 gây thất thoát đạm.
(3) Phân lân chứa nhiều phospho nhất là superphosphate kép. → Đúng. Superphosphate kép có hàm lượng P_2O_5 cao hơn superphosphate đơn.
(4) Bón nhiều phân đạm ammonium sẽ làm đất chua. → Đúng. Ion NH_4^+ bị oxi hóa sinh ra H^+ làm tăng độ chua của đất.
(5) Quặng phosphorite có thành phần chính là Ca_3(PO_4)_2. → Đúng. Đây là thành phần hóa học chính của quặng phosphat tự nhiên.
Các phát biểu đúng: (2), (3), (4), (5) → 4 phát biểu.
✅ Đáp án: 4
Bạn đang luyện đề THPTQG Môn Hoá thuộc chuyên mục luyện thi THPT Quốc gia. Để tiếp tục với nhiều đề thi khác, bạn có thể luyện tập thêm những đề thi liên quan khác bên dưới.


