Đáp án & giải thích đề môn Hoá k12
Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Bắc Ninh 2025 - Đề 06

DOL THPT
Mar 27, 2026
Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Bắc Ninh 2025 - Đề 06 được thiết kế dưới mô hình thi thử trắc nghiệm online, giúp người học nắm rõ format đề thi. Hệ thống chấm điểm ngay sau khi bạn làm xong bài, đồng thời lưu kết quả bài làm để bạn theo dõi hiệu quả tiến độ luyện thi, đi kèm lời giải chi tiết, dễ hiểu và tải file PDF đề thi HOÀN TOÀN MIỄN PHÍ.

Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Bắc Ninh 2025 - Đề 06
Download PDF
Miễn phí dowload
Câu hỏi đề bài
28 Câu hỏi
Phần I
Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Chất lỏng X không làm nhạt màu dung dịch KMnO_{4} ở điều kiện thường nhưng làm mất màu dung dịch KMnO_{4} khi đun nóng. X là chất nào trong các chất sau đây?
Vinylbenzene.
1,2-Dimethylbenzene.
Benzen.
Naphtalene.
Chất nào sau đây thuộc loại chất điện li yếu?
HCl.
CH_{3}COOH.
NaCl.
C_{2}H_{5}OH.
Chất nào sau đây thuộc loại hợp chất ion?
CH_{4}.
CH_{3}NH_{2}.
NaCl.
H_{2}O.
Dung dịch acetic acid phản ứng được với tất cả các chất trong dãy nào sau đây?
Zn, CuO, NaCl.
Cu, NaOH, NaCl.
Zn, NaOH, CaCO_{3}.
Cu, CuO, HCl.
rong công nghiệp hóa dầu, các alkane thường được loại bỏ hydrogen trong các phản ứng dehydrogen hóa để tạo ra các hydrocarbon không no có nhiều ứng dụng hơn như phản ứng sau: CH_{3}–CH_{2}–CH_{2}–CH_{3}\ (t^{\circ}) \rightarrow CH_{2}=CH–CH=CH_{2} + 2H_{2} Cho các liên kết và giá trị năng lượng liên kết của một số liên kết cộng hóa trị như bảng dưới. Biến thiên enthalpy chuẩn của phản ứng ở trên là:
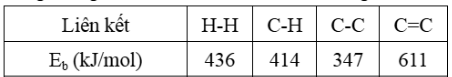
+1056 kJ.
–166 kJ.
–432 kJ.
+256 kJ.
Hợp chất E được điều chế từ alcohol X và acid Y (biết Y là hợp chất tạp chức chứa vòng benzen). E có trong thành phần của một số thuốc giảm đau, xoa bóp, cao dán., dùng để điều trị đau lưng, căng cơ, bong gân,. Thành phần về khối lượng các nguyên tố trong E như sau: 63,16%C, 5,26%H và 31,58%O. Phổ IR của E ngoài vùng hấp thụ với peak đặc trưng của liên kết C=O (số sóng 1750-1735 cm^{-1}), liên kết C–O (số sóng 1300-1000 cm^{-1}) còn có peak đặc trưng của liên kết O–H (số sóng 3650-3200 cm^{-1}). Từ phổ MS, xác định được E có phân tử khối là 152. Cho các phát biểu sau: (1) X là methyl alcohol. (2) Tổng số nguyên tử trong phân tử E là 20. (3) Y có nhóm –OH và –COOH. (4) 1 mol Y tác dụng vừa đủ với 2 mol NaOH. Số phát biểu đúng là:
2
1
4
3
Chất nào sau đây có thể hòa tan được Cu(OH)_{2}/NaOH ở nhiệt độ thường tạo ra dung dịch màu xanh lam?
Acetone.
Acetaldehyde.
Glycerol.
Propyl alcohol.
Hợp chất CH_{2}=CH_{2} có tên gọi là:
propene.
ethane.
methane.
ethene.
Chất nào sau đây tác dụng được với NaOH theo tỉ lệ số mol 1 : 1?
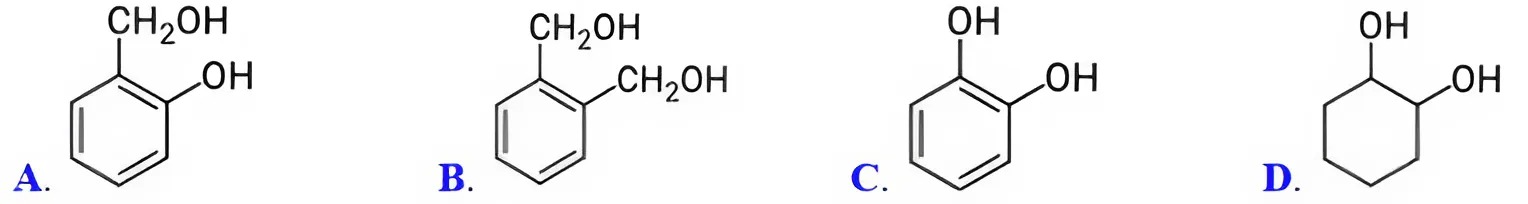
A
B
C
D
Cho phản ứng sau: 2NO(g) + O_{2}(g) \rightleftharpoons 2NO_{2}(g) \quad \Delta H^{\circ}_{298} = -115\ kJ Nhận xét nào sau đây sai?
Nếu tăng áp suất thì cân bằng trên chuyển dịch theo chiều thuận.
Nếu tăng nhiệt độ thì cân bằng trên chuyển dịch theo chiều thuận.
Phản ứng thuận là phản ứng toả nhiệt.
Hằng số cân bằng của phản ứng trên phụ thuộc vào nhiệt độ.
Đun nóng hỗn hợp gồm CH_{3}CH_{2}CH_{2}Cl và dung dịch NaOH, sau đó gạn lấy lớp dung dịch và acid hoá bằng dung dịch HNO_{3}, nhỏ tiếp vào đó dung dịch AgNO_{3}. Hiện tượng quan sát được là
có kết tủa màu trắng.
có kết tủa trắng, lắc nhẹ thì thấy tan dần.
có khí không màu, không mùi.
có khí màu nâu đỏ.
Cho phản ứng sau: Propene + H_{2}O (xt, t^{\circ}) → X. Công thức hóa học của sản phẩm chính là
CH_{3}COCH_{3}.
CH_{3}CH_{2}COOH.
CH_{3}CHOHCH_{3}.
CH_{3}CH_{2}CH_{2}OH.
Nhỏ nước bromine vào dung dịch nào sau đây thì xuất hiện kết tủa trắng?
Ethylene glycol.
Methylamine.
Phenol.
Allyl alcohol.
Để loại bỏ lớp cặn màu trắng (thành phần chính là CaCO_{3} và MgCO_{3}) trong ấm đun nước, vòi nước, thiết bị vệ sinh., trong gia đình, ta cho dùng dung dịch nào sau đây?
Muối ăn.
Dầu ăn.
Rượu uống.
Giấm ăn.
Cho X và Y là hai hợp chất hữu cơ có cùng công thức đơn giản nhất. Phân tích định lượng các nguyên tố trong Y thì có phần trăm khối lượng các nguyên tố là: 85,71%C; 14,29%H. Phổ MS của hai hợp chất này được cho trong hình dưới. Biết mảnh [M⁺] của chất X có cường độ tương đối lớn nhất, mảnh [M⁺] của chất Y có giá trị m/z lớn nhất. Công thức phân tử của X và Y lần lượt là
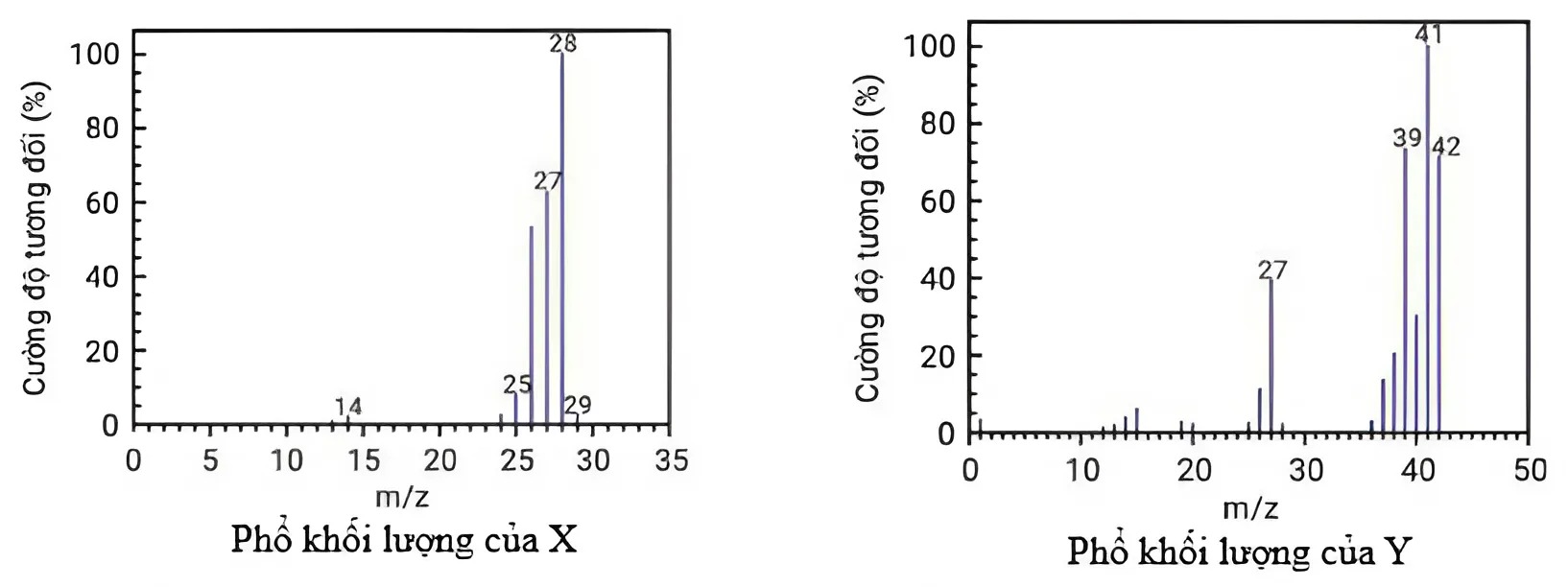
C_{2}H_{4} và C_{3}H_{6}.
C_{2}H_{4} và C_{3}H_{6}.
C_{3}H_{6} và C_{2}H_{4}.
C_{2}H_{2} và C_{6}H_{6}.
Bảng dưới đây cho biết nhiệt lượng toả ra khi đốt cháy hoàn toàn 1 mol alkane ở bảng dưới. Đốt cháy 100 gam alkane nào trong số các alkane ở trên toả ra nhiều nhiệt lượng nhất?
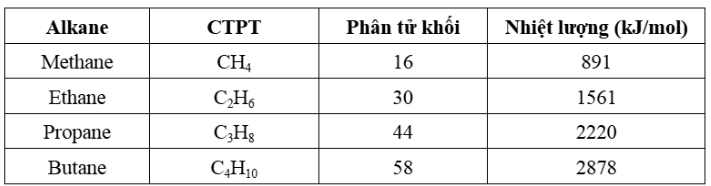
Propane.
Butane.
Ethane.
Methane.
Trong các chất sau, chất nào có nhiệt độ sôi thấp nhất?
C_{3}H_{8}.
C_{2}H_{5}OH.
CH_{3}CHO.
CH_{3}COOH.
Nhận xét nào sau đây đúng?
Acetaldehyde đóng vai trò chất oxi hóa khi tác dụng với nước bromine.
Benzaldehyde bị khử bởi NaBH_{4}, tạo ra benzyl alcohol.
Formaldehyde phản ứng với I_{2} trong môi trường kiềm, tạo ra iodoform.
Acetone bị oxi hóa bởi thuốc thử Tollens, tạo ra Ag.
Phần II
Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Khí sulfur dioxide (SO_{2}) do các nhà máy thải ra là nguyên nhân chính trong việc gây ô nhiễm môi trường. Theo quy chuẩn kỹ thuật quốc gia về chất lượng không khí (QCVN 05:2013/ BTNMT) nếu nồng độ SO_{2} vượt quá 350 \mug/m³ không khí (được đo trong 1 giờ) ở thành phố thì không khí bị ô nhiễm.
Phát biểu
Đúng
Sai
a
Số oxi hóa của sulfur trong SO_{2} là +6.
b
Khi SO_{2} tác dụng với NO_{2} (ở điều kiện thích hợp) thì SO_{2} đóng vai trò chất khử.
c
Lấy 50 L không khí trong 1 giờ ở một thành phố và phân tích thấy có 0,012 mg SO_{2} thì có thể kết luận không khí ở đó bị ô nhiễm.
d
SO_{2} là nguyên nhân chính gây ra hiện tượng mưa acid.
Đun nóng hỗn hợp gồm ethyl alcohol, acetic acid và sulfuric acid đặc ở điều kiện thích hợp để tổng hợp ra ester E. Sau một thời gian phản ứng thì thu được hỗn hợp X. Tiến hành tách được chất E từ X. Cho các thông số tính chất vật lý sau:

Phát biểu
Đúng
Sai
a
Phản ứng ester hoá giữa ethyl alcohol và acetic acid là phản ứng một chiều.
b
Để tách E ra khỏi X, sử dụng phương pháp chưng cất sẽ phù hợp hơn phương pháp chiết.
c
Phổ IR của E có peak hấp thụ đặc trưng của liên kết C=O và C–O.
d
Ở phản ứng trên có sự tách OH từ phân tử acetic acid và H từ phân tử ethyl alcohol.
Dẫn xuất monohalogen X có phần trăm khối lượng của C và H lần lượt là 35,05% và 6,75%, còn lại là bromine. Trong phân tử X, nguyên tử bromine liên kết với nguyên tử carbon bậc II.
Phát biểu
Đúng
Sai
a
Tổng số nguyên tử trong phân tử X là 14.
b
Đun nóng X với NaOH trong ethanol, thu được tối đa 3 alkene.
c
Trong phân tử X có 1 liên kết đôi C=C.
d
Chất X có mạch carbon không phân nhánh.
Hằng số phân li acid K_{a} (trong H_{2}O ở 25°C) của một số hợp chất được thể hiện trong bảng dưới đây. Giá trị của K_{a} càng lớn, tính acid càng mạnh.

Phát biểu
Đúng
Sai
a
Khi cho vào nước, acetic acid và phenol đều ít tan trong nước.
b
Nếu cho quỳ tím vào dung dịch picric acid, quỳ tím không chuyển màu.
c
Nếu cho picric acid vào dung dịch muối sodium carbonate, có bọt khí thoát ra từ dung dịch.
d
Nếu sục khí CO_{2} vào dung dịch muối sodium phenolate trong suốt, dung dịch bị đục trở lại.
Phần III
Thí sinh trả lời từ câu 1 đến câu 6.
Tiến hành chuẩn độ dung dịch NaOH chưa biết nồng độ bằng dung dịch chuẩn HCl 0,10M với chất chỉ thị phenolphthalein như sau: Bước 1: Dùng pipette lấy 10 mL dung dịch HCl 0,10M vào bình tam giác, thêm 1-2 giọt chất chỉ thị phenolphthalein. Bước 2: Cho dung dịch NaOH vào burette, điều chỉnh dung dịch trong burette về mức 0. Bước 3: Mở khóa burette, nhỏ từng giọt dung dịch NaOH xuống bình tam giác (lắc đều trong quá trình chuẩn độ) cho đến khi dung dịch xuất hiện màu hồng nhạt (bền trong khoảng 10 giây) thì dừng chuẩn độ. Bước 4: Ghi lại thể tích dung dịch NaOH đã dùng. Nếu thể tích dung dịch NaOH đã dùng là 12 mL thì nồng độ mol/L của dung dịch NaOH ban đầu là bao nhiêu? (Làm tròn kết quả đến hàng phần trăm)
Aspirin là một chất được sử dụng làm giảm đau, hạ sốt được điều chế theo phản ứng sau: o-HO-C_{6}H_{4}-COOH + (CH_{3}CO)_{2}O \rightarrow o-CH_{3}COO-C_{6}H_{4}-COOH + CH_{3}COOH Để sản xuất một lô thuốc aspirin gồm 2,7 triệu viên nén (mỗi viên chứa 500 mg aspirin) cần tối thiểu m kg salicylic acid, biết hiệu suất phản ứng là 90% tính theo salicylic acid. Tính giá trị của m. (Làm tròn kết quả đến hàng đơn vị)
Cho sơ đồ chuyển hoá sau: CH_{3}CH_{2}Br \xrightarrow{NaOH} X \xrightarrow{O_{2}, xúc\ tác} Y \xrightarrow{AgNO_{3}, NH_{3}} Z Các chất X, Y, Z đều là chất hữu cơ và đều là sản phẩm chính của các phản ứng. (1) Công thức cấu tạo của X là CH_{3}CHBrCH_{3}. (2) Tên gọi của Y là propan-1-ol. (3) Độ tan trong nước của X lớn hơn Y. (4) Chất Z tham gia phản ứng tráng bạc. (5) Khi cho hơi Y đi qua bột Al_{2}O_{3} đun nóng, thu được propene. (6) Chất Z phản ứng với I_{2} trong môi trường kiềm, tạo ra iodoform. Hãy liệt kê các phát biểu đúng. (Theo số thứ tự tăng dần)
Bromine có thể được tạo thành từ phản ứng sau: BrO_{3}^{-}(aq) + 5Br^{-}(aq) + 6H^{+}(aq) \rightarrow 3Br_{2}(aq) + 3H_{2}O(l) Tốc độ của phản ứng có dạng v = k[BrO_{3}^{-}][Br^{-}][H^{+}]^{2}. Giữ nguyên nhiệt độ, để tăng tốc độ sinh ra Br_{2} người ta tăng nồng độ H^{+} lên gấp đôi và nồng độ Br^{-} lên gấp ba (giữ nguyên nồng độ BrO_{3}^{-}). Cho biết tốc độ phản ứng điều chế Br_{2} tăng lên bao nhiêu lần?
Ethanol có thể được sản xuất từ cellulose hoặc tinh bột, loại ethanol này được dùng trong xăng E_{5} (xăng chứa 5% ethanol về thể tích). Lượng ethanol thu được từ 1,62 tấn mùn cưa (chứa 50% cellulose, còn lại là chất trơ) được dùng để pha chế V m³ xăng E_{5}. Biết hiệu suất quá trình sản xuất ethanol từ cellulose là 60%, ethanol có khối lượng riêng là 0,8 g/mL. Tính giá trị của V. (Làm tròn kết quả đến hàng phần mười)
Cho dãy các chất sau: (1) but-2-yne, (2) propanal, (3) benzaldehyde, (4) acetone, (5) propene, (6) acetylene. Hãy liệt kê các chất tạo được kết tủa khi tác dụng với dung dịch thuốc thử Tollens. (Theo số thứ tự tăng dần)
Xem đáp án và bài mẫu
Answer key
Chất lỏng X không làm nhạt màu dung dịch KMnO_{4} ở điều kiện thường nhưng làm mất màu dung dịch KMnO_{4} khi đun nóng. X là chất nào trong các chất sau đây?
Vinylbenzene.
1,2-Dimethylbenzene.
Benzen.
Naphtalene.
Giải thích câu 1
Giải thích chi tiết
😎 Cùng DOL xem qua cách giải câu này nhé!
📃 Thông tin đề bài cho:
Chất lỏng X không làm nhạt màu dung dịch KMnO_4 ở điều kiện thường.
X làm mất màu dung dịch KMnO_4 khi đun nóng.
Các chất lựa chọn: Vinylbenzene (styrene), 1,2-Dimethylbenzene (o-xylene), Benzen, Naphtalene.
❓ Hiểu câu hỏi:
Cần xác định chất có nhóm chức chỉ bị oxi hóa bởi KMnO_4 khi đun nóng, còn ở nhiệt độ thường không phản ứng.
Áp dụng kiến thức về phản ứng oxi hóa nhóm alkyl (–CH₃) gắn vào vòng thơm và phản ứng thử lên liên kết đôi (C=C).
🔎 Hướng dẫn cách làm:
Vinylbenzene (styrene) có liên kết đôi C=C; phản ứng cộng và oxi hóa với KMnO_4 xảy ra ngay ở nhiệt độ thường ⇒ dung dịch KMnO_4 bị nhạt màu ngay ⇒ không thỏa mãn điều kiện.
Benzen và Naphtalene không có nhóm alkyl bên ngoài vòng thơm, chỉ có vòng thơm ⇒ rất khó bị oxi hóa bởi KMnO_4 ngay cả khi đun nóng ⇒ không mất màu.
1,2-Dimethylbenzene (o-xylene) có hai nhóm –CH₃ gắn lên vòng thơm. Phản ứng oxi hóa nhóm metyl trên vòng thơm chỉ xảy ra khi đun nóng:
\mathrm{C_6H_4(CH_3)_2 + 6\, [O] \xrightarrow{\text{đun nóng}} C_6H_4(COOH)_2 + 2H_2O}Do đó ở nhiệt độ thường không mất màu, khi đun nóng mới làm mất màu KMnO_4 ⇒ thỏa mãn.
✅ Đáp án: 1,2-Dimethylbenzene
Hiện bạn đang luyện đề THPTQG Môn Hoá thuộc chuyên mục luyện thi THPT Quốc gia. Để tiếp tục với nhiều đề thi khác, bạn có thể xem thêm các đề liên quan khác dưới đây.


