Đáp án & giải thích đề môn Hoá k12
Đề thi thử tốt nghiệp THPT môn Hóa Học Sở GD&ĐT Hà Nội năm 2025 - Mã đề 03

DOL THPT
Mar 31, 2026
Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Hà Nội 2025 - Đề 03 được xây dựng dưới mô hình thi thử trắc nghiệm online, giúp bạn làm quen format đề thi. Hệ thống chấm điểm ngay sau khi bạn nộp bài, đồng thời lưu lại lịch sử làm bài để bạn tiện theo dõi quá trình ôn luyện, đi kèm đáp án giải thích rõ ràng và tải file PDF đề thi HOÀN TOÀN MIỄN PHÍ.

Đề thi thử tốt nghiệp THPT môn Hóa Học Sở GD&ĐT Hà Nội năm 2025 - Mã đề 03
Download PDF
Miễn phí dowload
Câu hỏi đề bài
28 Câu hỏi
Phần I
Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Cho các phương pháp sau: (1) đun nóng, (2) dùng dung dịch K_2CO_3, (3) dùng nhựa trao đổi ion, (4) dùng dung dịch Ca(OH)_2. Số phương pháp có khả năng làm mềm nước có tính cứng tạm thời là:
1
2
3
4
Palmitic acid là một acid béo bão hòa phổ biến trong động vật và thực vật. Công thức của palmitic acid là:
C_{17}H_{35}COOH
C_{17}H_{33}COOH
C_{15}H_{31}COOH
C_{17}H_{31}COOH
Insulin là hormon có tác dụng điều tiết lượng đường trong máu. Thủy phân một phần insulin thu được heptapeptide X mạch hở. Khi thủy phân không hoàn toàn X, thu được hỗn hợp chứa các peptide gồm: Phe-Phe-Tyr, Pro-Lys-Thr, Tyr-Thr-Pro và Phe-Tyr-Thr. Nếu đánh số thứ tự đầu N là số 1, thì amino acid ở vị trí số 5 trong X có ký hiệu là:
Thr
Pro
Tyr
Lys
Ở một số quốc gia, khoáng vật Trona là nguyên liệu chính để sản xuất soda. Thành phần hóa học chính của Trona là:
3NaF \cdot AlF_3
NaCl \cdot KCl
NaNO_3
Na_2CO_3 \cdot NaHCO_3 \cdot 2H_2O
Thả một đinh sắt nặng $$m_1$$ gam đã được đánh sạch bề mặt vào cốc chứa dung dịch $$CuSO_4$$ màu xanh. Sau một thời gian, thấy toàn bộ lượng Cu sinh ra đã bám vào
đinh sắt. Lấy “đinh sắt” ra khỏi cốc dung dịch, sấy khô, đem cân được $$m_2$$ gam. Cho các phát biểu sau:
(a) Phản ứng diễn ra trong cốc là: $$2Fe(s) + 3Cu^{2+}(aq) \rightarrow 2Fe^{3+}(aq) + 3Cu(s)$$
(b) Màu xanh của dung dịch $$CuSO_4$$ nhạt dần.
(c) So sánh, thu được kết tủa $$m_2 > m_1$$.
(d) Nếu thay đinh sắt ban đầu bằng thanh kẽm thì màu xanh của dung dịch không thay đổi.
Số phát biểu đúng là:
1
2
3
4
Menthol là một hoạt chất được tìm thấy nhiều trong cây bạc hà. Menthol tạo ra cảm giác mát lạnh và có tác dụng kháng khuẩn, chống co thắt và làm giãn cơ. Công thức cấu tạo của Menthol như hình bên dưới. Những phát biểu nào sau đây đúng khi nói về Menthol? (1) Menthol là alcohol đa chức. (2) Công thức phân tử của Menthol có dạng C_nH_{2n+1}OH. (3) Tên thay thế của Menthol là 2-isopropyl-5-methylcyclohexandiol. (4) Menthol là alcohol thơm. (5) Oxi hóa Menthol bằng CuO, đun nóng thu được một ketone.
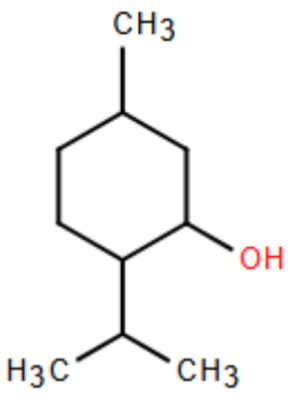
(1) và (2)
(2), (3) và (5)
(2) và (5)
(3), (4) và (5)
Trong các chất dưới đây chất nào là amine bậc một?
CH_3NHCH_3
CH_3CH_2NH_2
(CH_3)_3N
C_2H_5NHCH_3
Cao su buna-S (hay còn gọi là cao su SBR) là loại cao su tổng hợp được sử dụng rất phổ biến. Ước tính 50% lốp xe được làm từ SBR. Thực hiện phản ứng đồng trùng hợp các chất nào dưới đây thu được sản phẩm là cao su buna-S?
CH_2=CH{-}CH=CH_2 và CH_2=CH{-}Cl
CH_2=CH{-}CH=CH_2 và C_6H_5CH=CH_2
CH_2=CH{-}CH=CH_2 và CH_2=CH{-}CN
CH_2=CH{-}CH=CH_2 và sunfur
Khi cho muối X tác dụng với dung dịch NaOH, sinh khí mùi khai. X tác dụng với dung dịch BaCl_2 sinh ra kết tủa trắng không tan trong HNO_3. Vậy X là muối nào trong số các muối sau?
(NH_4)_2CO_3
(NH_4)_2SO_3
NH_4HSO_3
(NH_4)_2SO_4
Trong những năm 30 của thế kỉ XX, các nhà khoa học hãng DuPont (Mỹ) đã thông báo phát minh ra một loại vật liệu “mỏng hơn tơ nhện, bền hơn thép và đẹp hơn lụa”. Vật liệu này đã có mặt trong cuộc sống hàng ngày của con người, phổ biến trong sản phẩm như lốp xe, dù, quần áo, tất,... Một trong số vật liệu đó là nylon-6 dùng trong chỉ khâu phẫu thuật. Một hộp chỉ CARELON 7/10 có chứa 12 sợi chỉ, mỗi sợi chỉ nặng 0,1664 gam. To nylon-6 được tổng hợp từ ε-aminocaproic acid theo phản ứng: nNH_2-(CH_2)_5-COOH \rightarrow [-NH-(CH_2)_5-CO-]_n + nH_2O Biết hiệu suất quá trình tổng hợp nylon-6 là 80%. Khối lượng ε-aminocaproic acid cần dùng để sản xuất 2 triệu hộp chỉ CARELON 7/10 gần nhất với giá trị nào sau đây?
5137 kg
7578 kg
5787 kg
5807 kg
Cho thế điện cực chuẩn của các cặp oxi hóa – khử Fe^{3+}/Fe^{2+} và Cu^{2+}/Cu lần lượt là 0,771V và 0,340V. Nhận định nào sau đây đúng?
Tính khử của Cu yếu hơn tính khử của ion Fe^{2+}.
Tính oxi hóa của ion Cu^{2+} mạnh hơn tính oxi hóa của ion Fe^{3+}.
Ở điều kiện chuẩn, ion Fe^{2+} có thể khử ion Cu^{2+} thành Cu.
Ở điều kiện chuẩn, ion Fe có thể bị oxi hóa thành ion Fe^{2+} bởi kim loại Cu.
Một pin Galvani được cấu tạo bởi hai cặp oxi hóa – khử sau: (1) Ag^+ + 1e \rightarrow Ag\quad E^\circ_{Ag^+/Ag} = +0{,}799\ \text{V} (2) Ni^{2+} + 2e \rightarrow Ni\quad E^\circ_{Ni^{2+}/Ni} = -0{,}257\ \text{V} Khi pin làm việc ở điều kiện chuẩn, nhận định nào sau đây là đúng?
Ag được tạo ra ở cực dương, Ni được tạo ra ở cực âm.
Ag được tạo ra ở cực dương, Ni^{2+} được tạo ra ở cực âm.
Ag^+ được tạo ra ở cực âm và Ni được tạo ra ở cực dương.
Ag được tạo ra ở cực âm và Ni^{2+} được tạo ra ở cực dương.
Thực hiện phản ứng sau: 2[Fe(CN)_6]^{4-} (X) + Cl_2 \rightarrow 2[Fe(CN)_6]^{3-} (Y) + 2Cl^-. Phát biểu nào sau đây không đúng?
Phức X và Y có cùng phân tử khối.
Ion trung tâm của X và Y lần lượt là Fe^{2+} và Fe^{3+}.
X và Y đều có dạng hình học bát diện.
Phản ứng chuyển X thành Y thuộc loại phản ứng thế phối tử.
Ethylene là một trong những hóa chất quan trọng có nhiều ứng dụng trong đời sống. Phản ứng hóa học của ethylene với dung dịch Br_2 như sau: CH_2=CH_2 + Br_2 \rightarrow CH_2Br{-}CH_2Br. Cơ chế của phản ứng trên xảy ra như sau (có hình). Nhận định nào sau đây không đúng?
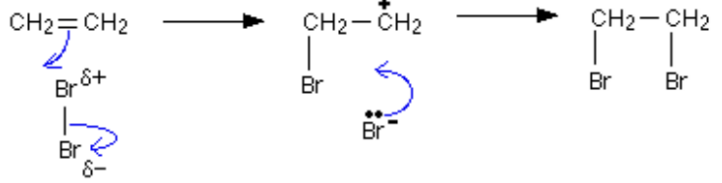
Phản ứng trên thuộc loại phản ứng cộng.
Giai đoạn 1, liên kết đôi phản ứng với tác nhân Br^+ tạo thành phần tử mang điện dương.
Giai đoạn 2, phần tử mang điện dương kết hợp với anion Br^- tạo thành sản phẩm.
Hiện tượng của phản ứng là dung dịch bromine bị nhạt màu.
Tính chất vật lý nào sau đây của kim loại không phải do các electron tự do gây ra?
Tính dẻo.
Ánh kim.
Tính cứng.
Tính dẫn điện và nhiệt.
Chất hữu cơ X có công thức phân tử là C_4H_8O và không tham gia phản ứng tráng bạc. Cho X tác dụng với iodine trong dung dịch NaOH, thu được kết tủa màu vàng. Khử X bằng NaBH_4 thu được chất hữu cơ Y. Tên gọi của chất Y là:
butan-2-ol.
butan-2-one.
2-methylpropanal.
butan-1-ol.
Thủy phân ester nào sau đây trong dung dịch NaOH thu được methyl alcohol?
CH_3COOCH_3
CH_3COOC_2H_5
HCOOC_2H_5
CH_3COOC_3H_7
Hợp chất X là dẫn xuất của benzene có công thức phân tử C_8H_{10}O_2 và tác dụng với NaOH theo tỉ lệ mol 1 : 1. Mặt khác, khi cho X tác dụng với Na dư thì số mol H_2 thu được đúng bằng số mol của X đã phản ứng. Khi tách một phân tử H_2O từ X trong điều kiện thích hợp, tạo ra sản phẩm Y có thể trùng hợp tạo polymer. Số công thức cấu tạo phù hợp với X là:
2
3
6
7
Phần II
Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Tiến hành thí nghiệm sau: • Bước 1: Rót vào ống nghiệm 1 và 2, mỗi ống khoảng 3 mL dung dịch H_2SO_4 loãng, sau đó cho vào mỗi ống một mẫu Zn giống nhau. • Bước 2: Nhỏ thêm 2–3 giọt dung dịch CuSO_4 vào ống 2. So sánh lượng bọt khí thoát ra ở 2 ống. Nhận định nào sau đây đúng?
Phát biểu
Đúng
Sai
a
Cả hai ống nghiệm, Zn đều bị oxi hóa thành Zn^{2+}.
b
Ống 1 xảy ra ăn mòn hóa học, còn ống 2 xảy ra ăn mòn điện hóa học.
c
Sau bước 2, tốc độ thoát khí ở hai ống là như nhau.
d
Ở ống 2, nếu thay dung dịch CuSO_4 bằng MgSO_4 vẫn xuất hiện pin điện hóa.
Cho hai chất hữu cơ mạch hở E và F đều chứa các nguyên tố C, H, O, đều có phân tử khối là 104 và không phải là đồng phân của nhau. Từ E và F thực hiện các phản ứng sau: (1) E + NaOH \xrightarrow{t^\circ} X + Y (2) F + 2NaOH \xrightarrow{t^\circ} Z + T + H_2O (3) X + NaOH \xrightarrow{CaO, t^\circ} CH_4 + Na_2CO_3 (4) Z + H_2SO_4 \rightarrow G + Na_2SO_4 Biết X, Y, Z, T, G, M là các chất hữu cơ, trong đó Y, T đều có chứa cùng một loại nhóm chức. Nhận định nào sau đây đúng?
Phát biểu
Đúng
Sai
a
E và F đều là các hợp chất hữu cơ tạp chức.
b
Từ chất T có thể điều chế trực tiếp được acetic acid.
c
Trong phân tử Z không còn nguyên tử hydrogen.
d
Sản phẩm của phản ứng este hóa giữa G với Y (xúc tác H_2SO_4 đặc) là các este đa chức mạch hở.
PETN (pentaerythritol tetranitrate, công thức hóa học: C(CH_2ONO_2)_4) là một trong số những chất nổ mạnh nhất đã biết, nổ nhạy nổ ma sát và chấn động hơn TNT, không bao giờ sử dụng một mình làm thuốc dẫn nổ. PETN ban đầu được dùng làm thuốc dẫn nổ và thuốc nổ chính của đạn nhỏ, nay nó được dùng làm thuốc nổ sau trong kíp nổ, được dùng làm thuốc lôi của dây truyền nổ. PETN cũng được sử dụng y học như một thuốc giãn mạch trong điều trị bệnh tim. Năng lượng nổ của PETN là 5,8 MJ/kg.
Phát biểu
Đúng
Sai
a
Trong phản ứng phân hủy nổ của PETN, cứ 1 gam PETN tạo ra 0,784 L hơi (CO_2, CO, N_2, H_2O) ở đktc.
b
Khi phân hủy nổ, 1 gam PETN tạo ra lượng nhiệt nhiều hơn lượng nhiệt tạo ra khi đốt cháy 1 gam butane (biết 30% năng lượng nổ của PETN chuyển thành nhiệt, còn lại là sóng xung kích; đốt cháy 1 mol butane tạo ra nhiệt lượng 2875 kJ).
c
Để sản xuất 1 kg PETN từ pentaerythritol (C(CH_2OH)_4) và HNO_3 đặc (H_2SO_4 đặc xúc tác), hiệu suất 80% cần 0,538 kg alcohol.
d
Thuốc tim Lentonitrat 7% chứa PETN và 7% sáp. Để sản xuất 100 gam thuốc Lentonitrat cần 7 gam PETN.
Năm 1965, trong quá trình tổng hợp thuốc chống loét dạ dày, nhà hóa học James M. Schlatter (Mỹ) đã vô tình phát hiện một chất ngọt nhân tạo với tên thường gọi là "Aspartame" có cấu tạo như hình vẽ. Aspartame ngọt hơn khoảng 200 lần so với đường ăn thông thường (sucrose) và được sử dụng trong đồ uống và thực phẩm dành cho người ăn kiêng vì có ít calo hơn đường ăn thông thường.
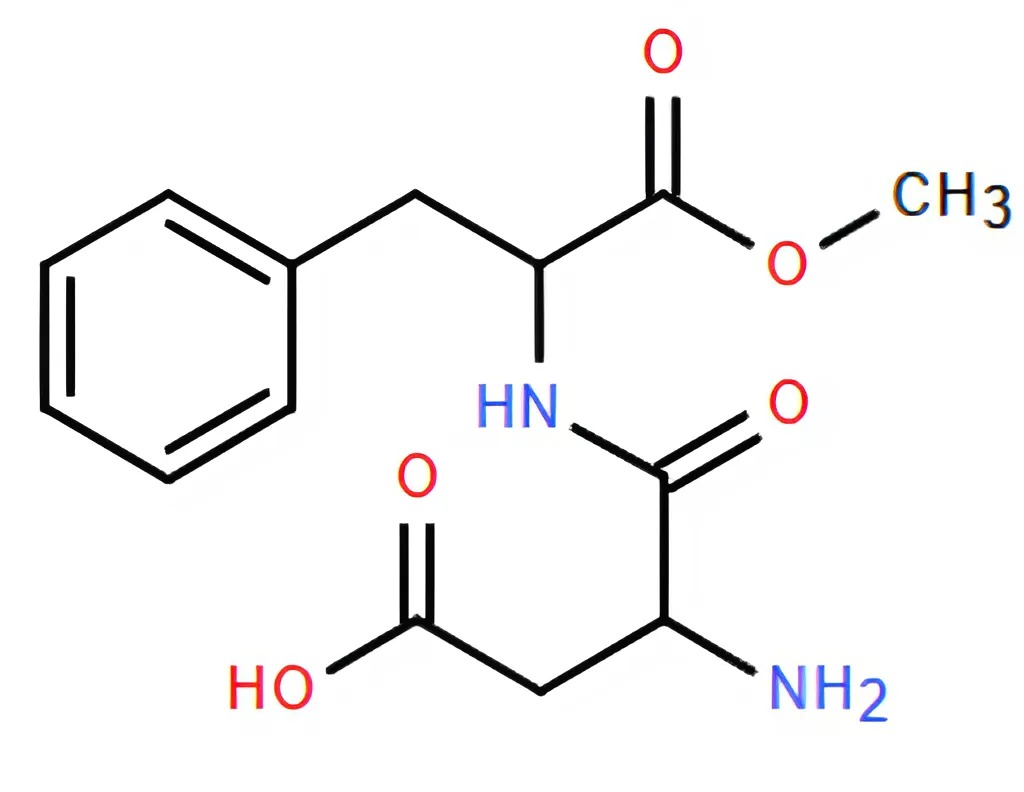
Phát biểu
Đúng
Sai
a
Aspartame là hợp chất hữu cơ tạp chức chứa đồng thời nhóm chức ester, amine, carboxylic acid và ketone.
b
Trong dung dịch, a mol Aspartame có thể phản ứng tối đa với 2a mol NaOH.
c
Công thức phân tử của Aspartame là C_{14}H_{18}N_2O_5.
d
Liên kết -CO-NH- trong phân tử Aspartame được gọi là liên kết peptide.
Phần III
Thí sinh trả lời từ câu 1 đến câu 6.
Thực hiện thí nghiệm điện phân dung dịch CuSO_4 với điện cực graphite (than chì). Cho các nhận định sau: (1) Tại cathode xảy ra sự khử Cu^{2+} trước, sau đó mới đến sự khử của nước. (2) Tại anode chỉ xảy ra sự oxi hóa của nước tạo khí hydrogen. (3) Sau điện phân, khối lượng cathode tăng lên. (4) Theo thời gian điện phân, pH của dung dịch giảm dần. (5) Khi vừa bắt đầu điện phân, cả hai điện cực đều có khí thoát ra. Có bao nhiêu nhận định đúng trong các nhận định trên?
Cho các polymer: (1) tơ tằm, (2) sợi bông, (3) sợi dây, (4) cellulose triacetate, (5) tinh bột. Có bao nhiêu polymer thiên nhiên trong số các polymer trên?
Sodium hydrogencarbonate được dùng để sản xuất thuốc giảm đau dạ dày. Giả sử 1 viên thuốc nặng 1 gam chứa 35% sodium hydrogencarbonate về khối lượng. Vậy để sản xuất được 2 triệu viên thuốc loại này cần bao nhiêu m^3 CO_2 ở đktc? (Làm tròn kết quả đến hàng đơn vị). Biết hiệu suất của phản ứng NaCl + NH_3 + CO_2 + H_2O \rightarrow NaHCO_3 + NH_4Cl là 75%.
Trong danh mục tiêu chuẩn chất lượng sản phẩm có chỉ tiêu về dư lượng chlorine không vượt quá 1 mg/L (ngưỡng cho phép). Phương pháp chuẩn độ iodine – thiosulfate được dùng để xác định dư lượng chlorine theo phương trình: Cl_2 + 2KI \rightarrow 2KCl + I_2 Sản phẩm I_2 tạo ra được nhận biết bằng hồ tinh bột và bị khử bởi dung dịch chuẩn sodium thiosulfate: I_2 + 2Na_2S_2O_3 \rightarrow 2NaI + Na_2S_4O_6 Dựa vào thể tích dung dịch Na_2S_2O_3 phản ứng, tính được dư lượng chlorine trong dung dịch mẫu. Tiến hành chuẩn độ 100 mL dung dịch mẫu A bằng dung dịch Na_2S_2O_3 0,01M, thấy thể tích Na_2S_2O_3 trung bình sau 3 lần chuẩn độ là 2,8 mL. Vậy dư lượng chlorine có trong mẫu A bằng bao nhiêu mg/L? (Làm tròn kết quả đến hàng phần trăm)
Cho sơ đồ phản ứng sau: CH_2=CH_2 \xrightarrow{KMnO_4 + H_2O} X \xrightarrow{+ CuO, t^\circ} Y \xrightarrow{+ O_2, xt, t^\circ} Z \xrightarrow{+ CH_3OH/H^+, t^\circ} T\ (C_3H_6O_4) Biết X, Y, Z, T là các hợp chất hữu cơ. Cho các phát biểu sau: (1) Chất T chỉ chứa một nhóm -CH_3. (2) Ở điều kiện thường, X và T hòa tan được Cu(OH)_2 tạo thành dung dịch phức màu xanh lam. (3) X, Z, T đều tác dụng với kim loại Na. (4) T tác dụng được với Na, NaHCO_3 và NaOH. (5) Khi đun nóng, Y và T phản ứng được với Cu(OH)_2 tạo kết tủa màu đỏ gạch. (6) Trong công nghiệp, X là nguyên liệu để sản xuất PE. Số phát biểu đúng là bao nhiêu?
Để xác định hàm lượng muối Fe(II) trong 1 mẫu dung dịch A có thể dùng dung dịch thuốc tím KMnO_4, phương trình ion như sau: MnO_4^- + 5Fe^{2+} + 8H^+ \rightarrow Mn^{2+} + 5Fe^{3+} + 4H_2O
Lấy 25,00 mL dung dịch A cho vào bình định mức, thêm nước cất cho đủ 100 mL, dung dịch thu được gọi là dung dịch X.
Lấy 10,00 mL dung dịch X chuyển vào bình tam giác sau đó thêm khoảng 5 mL dung dịch H_2SO_4 2M.
Tiến hành chuẩn độ 3 lần bằng dung dịch KMnO_4 0,02M. Kết quả thể tích KMnO_4 sau 3 lần chuẩn độ lần lượt là: 20,50 mL; 20,55 mL; 20,55 mL. Tính hàm lượng muối Fe^{2+} (g/L) trong dung dịch A với giả thiết lượng KMnO_4 chỉ phản ứng với Fe^{2+}. (Làm tròn kết quả đến hàng phần mười).
Xem đáp án và bài mẫu
Answer key
Cho các phương pháp sau: (1) đun nóng, (2) dùng dung dịch K_2CO_3, (3) dùng nhựa trao đổi ion, (4) dùng dung dịch Ca(OH)_2. Số phương pháp có khả năng làm mềm nước có tính cứng tạm thời là:
1
2
3
4
Giải thích câu 1
Giải thích chi tiết
😎 Cùng DOL xem qua cách giải câu này nhé!
📃 Thông tin đề bài cho:
Cho các phương pháp làm mềm nước: • đun nóng • dùng dung dịch K_2CO_3 • dùng nhựa trao đổi ion • dùng dung dịch Ca(OH)_2
Nước xét đến là nước có tính cứng tạm thời.
Hỏi: số phương pháp có khả năng làm mềm nước cứng tạm thời.
❓ Hiểu câu hỏi:
“Làm mềm nước cứng tạm thời” nghĩa là loại bỏ các ion Ca^{2+}, Mg^{2+} do muối bicacbonat (đặc trưng bởi Ca(HCO_3)_2, Mg(HCO_3)_2).
Cần xác định xem mỗi phương pháp có trung hòa hoặc kết tủa các muối bicacbonat này hay không.
🔎 Hướng dẫn cách làm:
Xác định bản chất cứng tạm thời: Các ion Ca^{2+}, Mg^{2+} liên kết với HCO_3^- ⇒ dễ phân hủy khi加 nhiệt hoặc khi có chất tạo kết tủa CO_3^{2-}.
Đánh giá từng phương pháp: • (1) Đun nóng: Ca(HCO_3)_2 ;\xrightarrow{\text{t° tăng}}; CaCO_3\downarrow + CO_2\uparrow + H_2O ⇒ kết tủa CaCO_3, loại bỏ Ca^{2+}. • (2) Dùng dung dịch K_2CO_3: Ca^{2+} + CO_3^{2-} ;\longrightarrow; CaCO_3\downarrow ⇒ kết tủa CaCO_3. • (3) Dùng nhựa trao đổi ion (cation): Nhựa trao đổi cation loại Ca^{2+}, Mg^{2+} thành Na^+ ⇒ loại bỏ hoàn toàn ion gây cứng. • (4) Dùng dung dịch Ca(OH)_2 (phương pháp vôi hóa): Ca(OH)_2 + Ca(HCO_3)_2 ;\longrightarrow; 2CaCO_3\downarrow + 2H_2O ⇒ kết tủa CaCO_3.
Tất cả bốn phương pháp đều có thể làm mất tính cứng tạm thời.
✅ Đáp án: 4
❌ Các đáp án khác:
A. 1: Chỉ tính phương pháp đun nóng, bỏ qua ba phương pháp còn lại.
B. 2: Chỉ liệt kê hai phương pháp, chưa đủ để loại bỏ hết ion Ca^{2+}, Mg^{2+} bicacbonat.
C. 3: Bỏ sót một trong các phương pháp hiệu quả (ví dụ nhựa trao đổi ion hoặc vôi hóa).
Bạn đang luyện đề THPTQG Môn Hoá thuộc chuyên mục luyện thi THPT Quốc gia. Để tiếp tục rèn luyện với nhiều đề thi khác, bạn học có thể luyện tập thêm các đề thi liên quan khác dưới đây.


