Đáp án & giải thích đề môn Hoá k12
Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Hà Nội 2025 - Đề 02

DOL THPT
Mar 27, 2026
Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Hà Nội 2025 - Đề 02 được thiết kế dưới mô hình thi thử trắc nghiệm online, giúp bạn hiểu rõ format đề thi. Nền tảng chấm điểm tự động sau khi bạn hoàn thành bài thi, đồng thời lưu lại lịch sử làm bài để bạn theo dõi hiệu quả tiến độ luyện thi, đi kèm lời giải chi tiết, dễ hiểu và tải file PDF đề thi HOÀN TOÀN MIỄN PHÍ.

Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Hà Nội 2025 - Đề 02
Download PDF
Miễn phí dowload
Câu hỏi đề bài
28 Câu hỏi
Phần I
Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Trong công nghiệp, kim loại nào sau đây được điều chế bằng phương pháp nhiệt luyện?
Fe
Na
Ca
Al
Tính chất nào sau đây không phải là tính chất vật lý chung của kim loại?
Tính cứng
Tính dẻo
Tính dẫn nhiệt
Tính dẫn điện
Chất X được tổng hợp bởi thực vật và chiếm khoảng 90% khối lượng sợi bông. X là:
tinh bột
cellulose
saccharose
maltose
Số nguyên tử nitrogen có trong phân tử peptide Lys-Gly-Ala là:
3
5
4
2
Tơ tằm, sợi bông, len thuộc loại tơ nào sau đây?
Tơ nhân tạo
Tơ tổng hợp
Tơ tự nhiên
Tơ bán tổng hợp
Phản ứng hóa học đặc trưng của chất béo là:
phản ứng trùng hợp
phản ứng thủy phân
phản ứng cộng
phản ứng thế
Dung dịch nào sau đây không làm đổi màu quỳ tím?
Methylamine
Glycine
Glutamic acid
Lysine
Trong môi trường base, protein có phản ứng màu biuret với:
HNO_3
NaCl
Cu(OH)_2
Mg(OH)_2
Chất nào sau đây là ester?
Oleic acid
Ethanol
Methyl formate
Glycerol
Chất nào sau đây là amine bậc ba?
(CH_3)_2NH
C_2H_5NH_2
CH_3NH_2
(CH_3)_3N
Cho các kim loại kim: Fe–Cu, Fe–C, Fe–Zn, Fe–Mg. Khi để lâu trong không khí ẩm, số hợp kim trong đó Fe bị ăn mòn điện hóa là:
3
4
1
2
Cho các cặp oxi hóa – khử của các kim loại và thế điện cực chuẩn tương ứng theo bảng dưới. Trong số các kim loại trên, kim loại có tính khử mạnh nhất là:
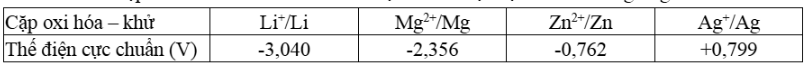
Mg
Zn
Li
Ag
Trong máu người trưởng thành, khỏe mạnh vào lúc đói (8 giờ sau ăn) có lượng đường huyết từ 4{,}4 đến 7{,}2\ \text{mmol/L}. Biết 1 L = 10 dL. Kết quả xét nghiệm của anh A là 152 mg/dL. Cho các nhận định: a) Lượng đường huyết là lượng glucose trong máu. b) Anh A có đường huyết thấp hơn mức giới hạn bình thường. c) Lúc đói, nếu ăn tinh bột thì lượng đường huyết sẽ tăng. d) Khi bị hạ đường huyết nên uống nước đường ấm. Số nhận định đúng là:
2
3
4
1
Kim loại Zn phản ứng được với dung dịch nào trong các dung dịch sau?
MgCl_2
NaCl
CuCl_2
AlCl_3
Ấm đun nước sau một thời gian sử dụng thường có lớp cặn bám ở đáy ấm (thành phần chính là CaCO_3). Để loại bỏ lớp cặn này có thể dùng chất nào sau đây?
Giấm ăn.
Đường mía.
Rượu uống.
Muối ăn.
Phản ứng clo hóa methane khi chiếu sáng xảy ra theo cơ chế gốc tự do gồm ba giai đoạn: khơi mào, phát triển mạch, và kết thúc. Trong đó giai đoạn phát triển mạch có: Cl\cdot + CH_4 \rightarrow HCl + \cdot CH_3, \cdot CH_3 + Cl_2 \rightarrow CH_3Cl + Cl\cdot. Nhận định nào sau đây không đúng về giai đoạn này?
Có sự hình thành liên kết H-Cl.
Có sự hình thành liên kết C-Cl.
Có sự phân cắt liên kết C-H.
Có sự hình thành liên kết Cl-Cl.
Cho nhiệt độ sôi của các chất thể hiện ở bảng dưới. Trong các chất trên, chất nào là chất khí ở điều kiện thường?
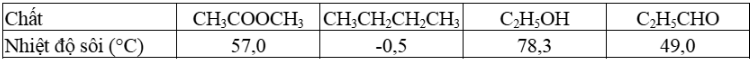
CH_3COOCH_3
CH_3CH_2CH_2CH_3
C_2H_5CHO
C_2H_5OH
Dưới đây một chai nhựa có kí hiệu như hình dưới.
PP là kí hiệu của polymer nào sau đây?

Polystyrene
Polypropylene
Poly(vinyl chloride)
Polyethylene
Phần II
Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
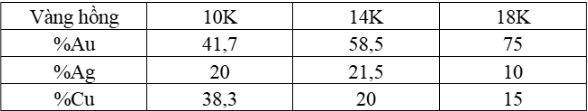
Vàng hồng là một hợp kim quý được sử dụng chủ yếu trong chế tác trang sức. Trên thị trường có các loại vàng hồng 10K, 14K, 18K với thành phần như bảng: Vàng hồng 10K thường bị xỉn màu nhanh do hàm lượng đồng cao. Một nhóm học sinh khi được giao dự án làm tăng hàm lượng vàng, bạc trong một mảnh hợp kim thu hồi từ chiếc nhẫn vàng hồng 10K đã đề xuất sử dụng phương pháp điện phân để loại đồng ra khỏi mảnh nhẫn, với giả thuyết “Nếu kim loại đồng trong mảnh nhẫn tan hết thì khối lượng mảnh nhẫn không giảm nữa”. Để kiểm tra giả thuyết này, nhóm học sinh đã làm thí nghiệm như sau:
Cân để xác định khối lượng ban đầu của mảnh nhẫn (1,125 gam) và thanh đồng tinh khiết (2,255 gam).
Nối mảnh nhẫn với một điện cực và thanh đồng tinh khiết với điện cực còn lại của nguồn điện một chiều, rồi nhúng vào bình điện phân chứa dung dịch copper(II) sulfate.
Điện phân ở hiệu điện thế phù hợp.
Sau thời gian điện phân, làm khô, rồi cân để xác định lại khối lượng của mảnh nhẫn và thanh đồng tinh khiết, thấy khối lượng của mảnh nhẫn là 0,515 gam và của thanh đồng là 2,740 gam. Trong quá trình điện phân nước bay hơi không đáng kể.
Phát biểu
Đúng
Sai
a
Có một lượng kim loại bị rơi xuống đáy bình điện phân.
b
Mảnh nhẫn chứa Au và Ag có thế điện cực lớn hơn Cu nên nối vào cực dương.
c
Nồng độ ion Cu^{2+} trong dung dịch không đổi trong quá trình điện phân.
d
Kết quả trên cho thấy giả thuyết học sinh đưa ra là sai.
Biodiesel (diesel sinh học) là nhiên liệu lỏng, thân thiện hơn với môi trường so với diesel truyền thống. Biodiesel được sản xuất thông qua phản ứng giữa chất béo với các alcohol mạch ngắn (thường là methanol), với xúc tác là kiềm, thu được biodiesel (ester của acid béo) và glycerol. Một nhà máy tái chế dầu ăn đã qua sử dụng để sản xuất biodiesel theo phương trình phản ứng tổng quát sau: (RCOO)_3C_3H_5 + 3CH_3OH \xrightarrow{NaOH} 3RCOOCH_3 + C_3H_5(OH)_3.
Phát biểu
Đúng
Sai
a
Biodiesel có thành phần nguyên tố giống dầu diesel truyền thống.
b
Phương pháp này giúp tận dụng dầu ăn đã qua sử dụng, giảm ô nhiễm môi trường.
c
Phản ứng (1) là thủy phân ester trong môi trường kiềm.
d
Từ 500 kg dầu ăn có thể tạo tối đa 432 kg biodiesel dạng methyl ester với hiệu suất 90%.
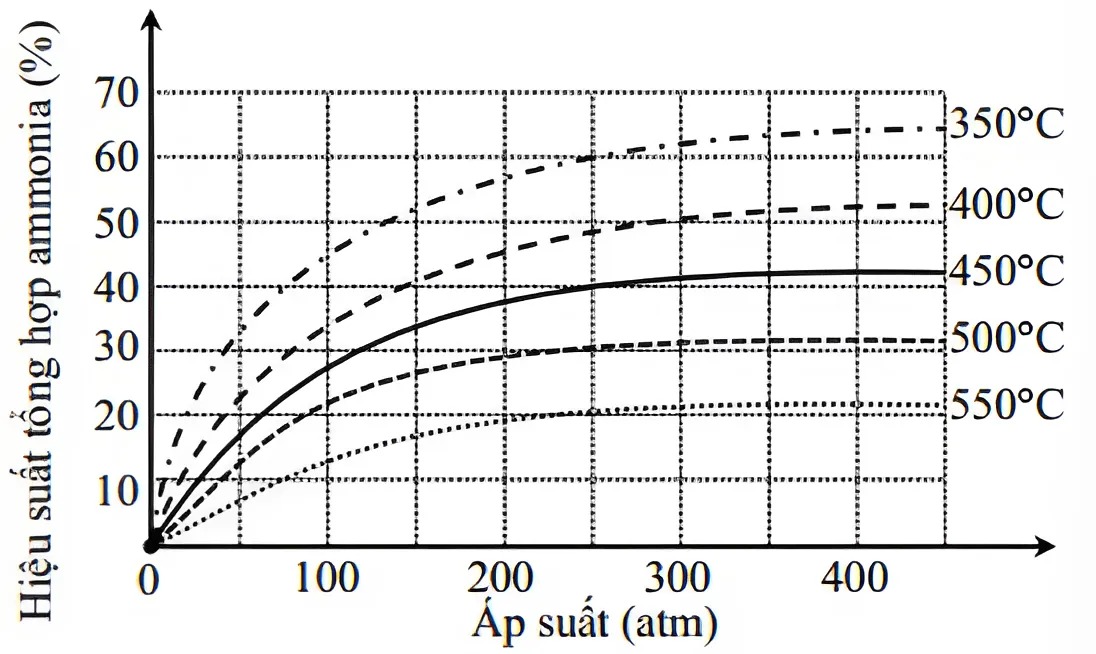
Ammonia được tổng hợp theo phản ứng: N_2(g) + 3H_2(g) \rightleftharpoons 2NH_3(g) (*). Kết quả nghiên cứu hiệu suất phản ứng phụ thuộc áp suất và nhiệt độ được cho theo đồ thị.
Phát biểu
Đúng
Sai
a
Phản ứng (*) xảy ra ở nhiệt độ cao nên là phản ứng thu nhiệt (\Delta H > 0).
b
Hiệu suất phản ứng ở 550^\circ C, 300 atm cao hơn hiệu suất ở 500^\circ C, 200 atm.
c
Khi tăng áp suất thì cân bằng phản ứng chuyển dịch theo chiều thuận.
d
Ở 450^\circ C, 250 atm, 2 mol N_2 trộn với 4,5 mol H_2 thu được 1,2 mol NH_3.
Mẻ là một loại gia vị truyền thống tạo nên hương vị đặc trưng cho nhiều món ăn của ẩm thực Viện Nam. Người ta thường làm mẻ bằng cách lên men bún hoặc cơm nát để nguội. Quá trình lên men diễn ra nhờ vi khuẩn kị khí, biến tinh bột và đường thành lactic acid. Chính acid này đã tạo nên vị chua của mẻ, sữa chua,…Một học sinh tiến hành thử nghiệm làm ba lọ mẻ theo các cách sau:
Lọ 1: Cho 100 gam cơm nát để nguội vào lọ thủy tinh sạch có sẵn nước cơm (là phần nước được chắt ra khi cơm đã sôi), rồi đậy kín.
Lọ 2: Cho 100 gam cơm nát để nguội vào lọ thủy tinh sạch có sẵn một ít nước đường glucose, rồi đậy kín.
Lọ 3: Cho 100 gam cơm nát để nguội vào lọ thủy tinh sạch có sẵn một ít mẻ, rồi đậy kín. Giả sử các điều kiện thực hiện phản ứng lên men đều giống nhau
Phát biểu
Đúng
Sai
a
Trong ba lọ đều xảy ra các phản ứng hóa học: (C_6H_{10}O_5)_n + nH_2O \xrightarrow{enzyme} nC_6H_{12}O_6 và C_6H_{12}O_6 \xrightarrow{enzyme} 2CH_3CH(OH)COOH.
b
Nước cơm, nước đường, mè là xúc tác có sẵn trong cả ba lọ.
c
Thứ tự bắt đầu thu được mè: lọ 3, lọ 1, lọ 2.
d
Nếu không có sẵn mè ở lọ 3 thì có thể thay thế bằng sữa chua không đường.
Phần III
Thí sinh trả lời từ câu 1 đến câu 6.
Trong công nghiệp, xút (NaOH) và chlorine (Cl_2) được sản xuất bằng phương pháp điện phân dung dịch muối ăn bão hòa. Biết hiệu suất chuyển hóa NaCl thành NaOH là 46,28%. Để sản xuất 2,0 tấn NaOH, cần bao nhiêu tấn nguyên liệu NaCl? (Làm tròn đến hàng phần mười)
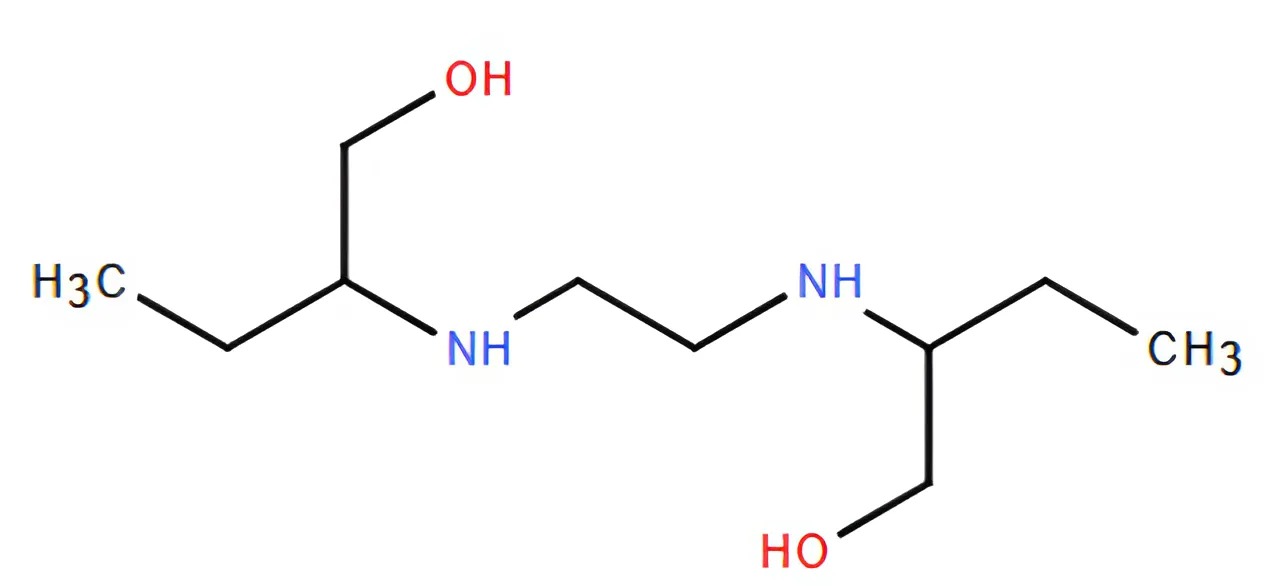
Ethambutol (có công thức cấu tạo như hình bên dưới) là một loại thuốc kháng sinh, có tác dụng trong điều trị các bệnh nhiễm trùng do vi khuẩn. Ethambutol thường được sử dụng kết hợp với các loại thuốc khác để điều trị bệnh lao.
Ethambutol có công thức phân tử là C_{10}H_{24}N_2O_2.
Có 2 nhóm amine bậc hai.
Phản ứng với NaOH theo tỉ lệ mol 1:2.
Phản ứng với CuO cho sản phẩm chứa nhóm chức aldehyde.
Là hợp chất hữu cơ tạp chức. Viết các phát biểu đúng theo thứ tự tăng dần.
Để đánh giá mức độ tự diễn biến của một phản ứng tại nhiệt độ T, người ta dựa vào đại lượng biến thiên năng lượng tự do Gibbs (\Delta G_T^\circ). Nếu \Delta G_T^\circ > 0: phản ứng không tự xảy ra; \Delta G_T^\circ < 0: phản ứng tự xảy ra. Giá trị của đại lượng này được tính theo biểu thức: \Delta G_T^\circ = \Delta H_T^\circ - T \cdot \Delta S_T^\circ. Trong đó:
T: nhiệt độ tính theo thang Kelvin (K);
\Delta H_T^\circ: Biến thiên enthalpy của phản ứng;
\Delta S_T^\circ: Biến thiên entropy của phản ứng (đại lượng đặc trưng cho độ mất trật tự của hệ ở một trạng thái và điều kiện xác định). Tính giá trị thấp nhất của T (làm tròn đến hàng đơn vị) để phản ứng sau tự xảy ra: CaCO_3(s) \rightarrow CaO(s) + CO_2(g). Cho biết: \Delta S_T^\circ = 159{,}26\ \text{J/mol.K} và nhiệt tạo thành chuẩn của các chất như bảng dưới. Giả sử \Delta H_T^\circ và \Delta S_T^\circ không phụ thuộc vào nhiệt độ.

Để bảo vệ vật bằng thép khỏi bị ăn mòn, người ta có thể:
Sơn kín bề mặt cánh cửa bằng thép;
Tráng kẽm lên tấm thép mỏng khi sản xuất tôn;
Gắn một số tấm kẽm lên vỏ tàu làm bằng thép;
Cho dầu mỡ lên các đinh ốc vít trên đường ray. Có bao nhiêu cách trong các cách trên thuộc phương pháp bảo vệ bề mặt?
Amine C_3H_9N có bao nhiêu đồng phân?
Poly(hexamethylene adipamide) còn gọi là nylon-6,6 là polymer được tạo từ phản ứng trùng ngưng giữa acid adipic và hexamethylenediamine. Biết mỗi mắt xích gồm: (-NH-(CH_2)_6-NH-CO-(CH_2)_4-CO-). Tính khối lượng của một mắt xích nylon-6,6 (đơn vị amu)?
Xem đáp án và bài mẫu
Answer key
Trong công nghiệp, kim loại nào sau đây được điều chế bằng phương pháp nhiệt luyện?
Fe
Na
Ca
Al
Giải thích câu 1
Giải thích chi tiết
😎 Cùng DOL xem qua cách giải câu này nhé!
📃 Thông tin đề bài cho:
Đề bài yêu cầu xác định kim loại được điều chế bằng phương pháp nhiệt luyện.
Các kim loại cần xét: sắt (Fe), natri (Na), canxi (Ca), nhôm (Al).
❓ Hiểu câu hỏi:
Câu hỏi: “Trong công nghiệp, kim loại nào được điều chế bằng phương pháp nhiệt luyện?”
Khái niệm cần vận dụng: phương pháp nhiệt luyện (còn gọi là phương pháp aluminothermy).
🔎 Hướng dẫn cách làm:
Phương pháp nhiệt luyện là quá trình dùng bột nhôm (Al) làm chất khử để khử oxit của kim loại khác ở nhiệt độ rất cao mà không cần dùng lò điện.
Phương trình điển hình của phản ứng nhiệt luyện là:
- \text{Fe}_2\text{O}_3 + 2\,\text{Al} \;\longrightarrow\; 2\,\text{Fe} + \text{Al}_2\text{O}_3 + \text{nhiệt lượng lớn}
✅ Đáp án: \text{Fe}
❌ Các đáp án khác:
Natri (Na): điều chế qua điện phân NaCl, không thuộc nhiệt luyện.
Canxi (Ca): điều chế qua điện phân CaCl₂ nóng chảy, không dùng Al làm khử.
Nhôm (Al): chính bản thân Al là chất khử trong phản ứng nhiệt luyện, không được điều chế theo phương pháp này.
Hiện bạn đang luyện đề THPTQG Môn Hoá thuộc chuyên mục luyện thi THPT Quốc gia. Để tiếp tục rèn luyện với nhiều đề thi khác, bạn học có thể tham khảo những đề liên quan khác bên dưới.


