Đáp án & giải thích đề môn Hoá k12
Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Hà Tĩnh 2025 - Đề 04

DOL THPT
Mar 27, 2026
Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Hà Tĩnh 2025 - Đề 04 được xây dựng dưới mô hình thi thử trắc nghiệm online, giúp người học hiểu rõ bố cục đề thi. Nền tảng chấm điểm tự động sau khi bạn hoàn thành bài thi, đồng thời lưu lại lịch sử làm bài để bạn theo dõi hiệu quả lộ trình ôn tập, đi kèm đáp án giải thích chi tiết và tải file PDF đề thi HOÀN TOÀN MIỄN PHÍ.

Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Hà Tĩnh 2025 - Đề 04
Download PDF
Miễn phí dowload
Câu hỏi đề bài
28 Câu hỏi
Phần I
Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Biết X là một amine bậc 3 có phân tử khối bằng 59. Tên gọi của X là:
Propylamine.
N-Methylethanamine.
Triethylamine.
Trimethylamine.
Methadone là một loại thuốc dùng trong cai nghiện ma túy, thực chất nó cũng là một loại chất gây nghiện nhưng “nhẹ” hơn các loại ma túy thông thường và dễ kiểm soát hơn. Công thức cấu tạo methadone như hình dưới. Công thức phân tử của methadone là:
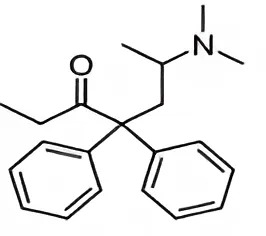
C_{21}H_{27}NO
C_{17}H_{22}NO
C_{17}H_{27}NO
C_{21}H_{29}NO
Phương trình hoá học của phản ứng ethanal với HCN là: CH_3CH=O + HCN \to CH_3CHOH–CN. Giai đoạn (1) trong cơ chế của phản ứng trên xảy ra như sau: (hình). Giai đoạn (2) trong cơ chế của phản ứng trên xảy ra như sau: (hình). Nhận định nào sau đây không đúng?
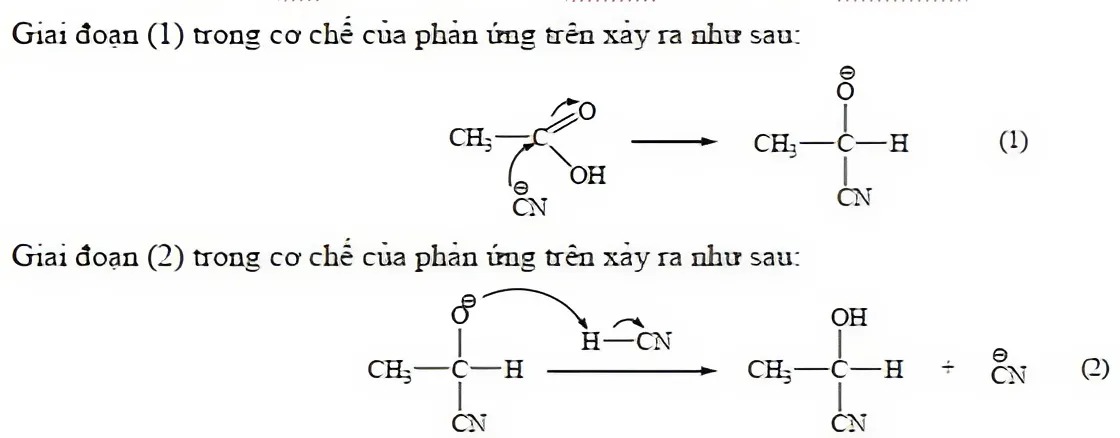
Trong giai đoạn (1) có sự hình thành liên kết σ.
Trong giai đoạn (2) có sự phân cắt liên kết π.
Trong giai đoạn (2) có sự hình thành liên kết σ.
Trong giai đoạn (1) có sự phân cắt liên kết π.
Ở nhiệt độ thường, kim loại nào sau đây đều tác dụng với nước ở nhiệt độ thường?
Na, Mg, Fe.
Cu, Na, Ag.
Na, K, Ba.
Au, K, Al.
Tơ nylon-6,6 được điều chế bằng phản ứng …(1)… từ hexamethylenediamine và …(2)…. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là:
trùng hợp, acetic acid.
trùng ngưng, adipic acid.
trùng ngưng, acrylic acid.
trùng hợp, formic acid.
Nổ bụi là vụ nổ gây ra bởi quá trình bốc cháy nhanh hơn các hạt bụi mịn phân tán trong không khí bên trong một không gian hạn chế, tạo ra sóng nổ. Nổ bụi xảy ra khi có đủ năm yếu tố: nguồn oxygen, nguồn nhiệt, nhiên liệu (bụi có thể cháy được), nồng độ bụi đủ lớn và không gian đủ kín. Một vụ nổ khủng khiếp từng xảy ra tại công viên ở Đài Loan. Cụ thể là một loại bột màu tạo hiệu ứng sân khấu được phun vào đám đông khi họ đang nhảy trong tiếng nhạc rất lớn. Đám mây bụi đột nhiên bốc cháy và phát nổ ngay lúc đó khiến cho 10 người chết và 500 bị thương. Bột màu gồm bột ngô, bột mì có thành phần chính là tinh bột. Cho các phát biểu sau: (a) Nổ bụi là một vụ nổ vật lí. (b) Nhiên liệu trong vụ nổ bụi tại công viên ở Đài Loan là bột ngô, bột mì. (c) Tốc độ của các phản ứng hóa học càng nhanh khi kích thước của các hạt vật chất tham gia phản ứng càng nhỏ. (d) Tinh bột do 3 nguyên tố carbon, hydrogen, oxygen tạo thành. Các phát biểu đúng là
(a), (b), (c).
(a), (b), (d).
(a), (c), (d).
(b), (c), (d).
X và Y là các hợp chất vô cơ của một kim loại kiềm, có nhiều ứng dụng trong thực tế và khi đốt nóng ở nhiệt độ cao trên đèn khí cho ngọn lửa màu vàng. Biết chúng hóa mãn các sơ đồ phản ứng sau: (1) X + NaOH → Y + H_2O; (2) X → Y + …. Y là chất nào sau đây?
K_2CO_3
Na_2CO_3
NaOH
NaHCO_3
Cho bảng giá trị thế điện cực chuẩn của các cặp oxi hóa – khử như dưới. Sức điện động chuẩn lớn nhất của pin Galvani thiết lập từ hai cặp oxi hóa – khử trong số các cặp trên là:
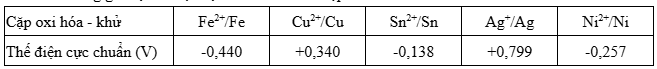
0,459\ \mathrm{V}
1,239\ \mathrm{V}
0,780\ \mathrm{V}
1,056\ \mathrm{V}
Ứng với công thức phân tử C_3H_6O_2 có bao nhiêu đồng phân là ester?
3
4
2
1
Chất nào sau đây được tạo thành từ sự liên kết của một đơn vị glucose với một đơn vị fructose?
Maltose
Tinh bột
Saccharose
Cellulose
Quặng có chứa khoáng vật sphalerite là nguyên liệu dùng để sản xuất kim loại nào sau đây?
Iron (Fe)
Copper (Cu)
Aluminium (Al)
Zinc (Zn)
Kim loại nào sau đây có nhiệt độ nóng chảy cao nhất?
Al
Fe
Na
W
Điểm đẳng điện (kí hiệu pI) là giá trị pH của dung dịch mà tại đó amino acid tồn tại ion lưỡng cực và tổng điện tích dương bằng tổng điện tích âm. Giá trị pH của dung dịch thay đổi làm cho amino acid tích điện khác nhau và có khả năng dịch chuyển về các hướng khác nhau dưới tác dụng của điện trường. Tính chất này được gọi là tính điện di của amino acid và có thể dùng để tách, tinh chế amino acid ra khỏi hỗn hợp của chúng. Trong quá trình điện di, ion sẽ di chuyển về phía điện cực trái dấu với ion đó. Cho ba amino acid gồm valine, glutamic acid, lysine có điểm đẳng điện như bảng dưới. Cho các phát biểu sau: (a) Với pH = 6,0 tách được ba amino acid ra khỏi dung dịch hỗn hợp của chúng. (b) Với pH = 1,0 cả ba amino acid sẽ di chuyển về cực dương. (c) Với pH = 9,7 chỉ tách được lysine ra khỏi dung dịch hỗn hợp của chúng. (d) Với pH = 13,0 cả ba amino acid sẽ di chuyển về cực âm. Số phát biểu đúng là
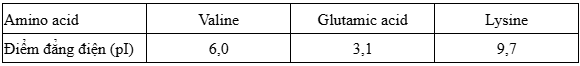
4
3
1
2
Cho dãy các nguyên tố: Mg, K, Fe, Na, Al, Cs. Số nguyên tố thuộc nhóm IA là
1
3
4
2
Ở trạng thái cơ bản, nguyên tử nào sau có 3 electron ở phân lớp 2p?
_{8}O
_{17}Cl
_{20}Ca
_{7}N
Chất béo là các triester (ester ba chức) của …(1)… với các …(2)… gọi chung là các triglyceride. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
ethylene glycol, acid béo.
glycerol, acid béo.
glycerol, carboxylic acid.
ethylene glycol, carboxylic acid.
Cho peptide X có công thức cấu tạo như hình bên. Số liên kết peptide trong X là
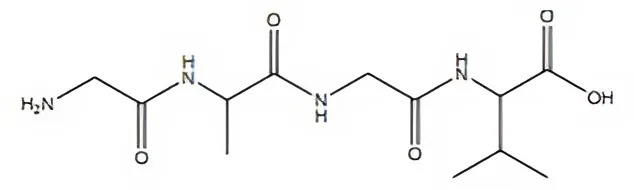
5
2
3
4
Cách làm nào sau đây là đúng trong việc khử chua bằng vôi sống (CaO) và bón phân superphosphate (Ca(H_2PO_4)_2) cho lúa?
Bón superphosphate và vôi cùng lúc.
Bón superphosphate trước rồi vài ngày sau mới bón vôi khử chua.
Bón vôi khử chua trước rồi vài ngày sau mới bón superphosphate.
Bón vôi khử chua trước rồi bón superphosphate ngay sau khi bón vôi.
Phần II
Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Quá trình nấu rượu gạo thủ công được thực hiện như sau: Bước 1: Gạo được nấu chín, để nguội, rắc men, ủ kín 3–5 ngày, thu được một hỗn hợp chủ yếu gồm nước, ethanol và bã rượu. Bước 2: Đun nóng hỗn hợp trên đến nhiệt độ sôi, hơi bay ra đi vào đường ống dẫn. Hỗn hợp hơi trong đường ống được làm lạnh, bị ngưng và chảy vào bình hứng.
Phát biểu
Đúng
Sai
a
Ở bước 1, có sinh ra khí CO_2.
b
Trong quy trình trên nấu rượu gạo đã sử dụng phương pháp chung cất lôi cuốn hơi nước.
c
Quá trình C_2H_5OH(g)\rightleftharpoons C_2H_5OH(l) có chiều thuận thu nhiệt, khi làm lạnh là tỏa nhiệt của hệ nên cân bằng chuyển dịch theo chiều thuận, kết quả thu được ethanol lỏng từ ethanol hơi thoát ra từ nồi cất.
d
Trong quá trình chưng cất hỗn hợp ethanol và nước, tỉ lệ thể tích ethanol/nước giảm dần do nhiệt độ sôi của ethanol thấp hơn của nước.
Khi phân tích thành phần nguyên tố của ester X, thấy trong phân tử X có tỷ lệ số nguyên tử C và H tương ứng 1:2. Thủy phân X trong môi trường acid, thu được alcohol Y (có M_Y = 46) và carboxylic acid Z (số nguyên tử carbon bằng bội số số nguyên tử carbon trong phân tử X).
Phát biểu
Đúng
Sai
a
Khả năng tan trong nước của X kém hơn Y và Z
b
Phân tử X có 60\% carbon về khối lượng.
c
Ứng với công thức phân tử của X có nắm ester là đồng phân cấu tạo của nhau.
d
Từ Y có thể điều chế trực tiếp được Z bằng xúc tác enzyme.
Một nhóm học sinh nghiên cứu về tinh chế kim loại đồng (copper) bằng phương pháp điện phân từ một thanh đồng không tinh khiết (chứa tạp chất không tham gia vào quá trình điện phân). Nhóm học sinh đã thực hiện thí nghiệm theo các bước sau:
Bước 1: Cân để xác định khối lượng ban đầu của thanh đồng nguyên chất (3,21 gam) và thanh đồng không tinh khiết (3,30 gam).
Bước 2: Nối thanh đồng nguyên chất với một điện cực và thanh đồng không tinh khiết với điện cực còn lại của nguồn điện một chiều, rồi nhúng vào bình điện phân chứa dung dịch copper (II) sulfate đã acid hóa bằng dung dịch sulfuric acid.
Bước 3: Điện phân ở hiệu điện thế phù hợp. Sau thời gian điện phân t giây, các điện cực được lấy ra, làm khô cẩn thận, rồi cân để xác định lại khối lượng của thanh đồng nguyên chất và thanh đồng không tinh khiết. Kết quả: khối lượng của thanh đồng nguyên chất tăng lên thành 3,51 gam và khối lượng thanh đồng không tinh khiết là 2,98 gam.
Phát biểu
Đúng
Sai
a
Ở cực dương xảy ra quá trình: Cu^{2+} + 2e^- \to Cu.
b
Màu của dung dịch CuSO_4 không thay đổi.
c
Trong thí nghiệm trên, thanh đồng nguyên chất được nối với điện cực âm, thanh đồng không tinh khiết được nối với điện cực dương của nguồn điện.
d
Sau thời gian điện phân t giây, khối lượng đồng trong thanh đồng không tinh khiết tan ra là 0,32 gam.
Cho công thức cấu tạo các hợp chất hữu cơ sau: (1) CH_4; (2) CH_3OH; (3) CH_2=CH_2; (4) HOCH_2-CHOH-CH_2OH; (5) CH\equiv CH; (6) CH_3CHO; (7) CH_3COOH; (8) HOOC(CH_2)_2COOH; (9) C_6H_6; (10) NH_2CH_2COOH; (11) HOCH_2(CHOH)_4CHO.
Phát biểu
Đúng
Sai
a
Có bảy hợp chất thuộc loại dẫn xuất hydrocarbon, trong đó có ba chất đơn chức.
b
Có hai hợp chất thuộc loại alcohol và ba hợp chất thuộc loại carboxylic acid.
c
Có bốn hợp chất thuộc loại hydrocarbon, trong đó có hai hydrocarbon không no.
d
Có hai hợp chất đa chức và hai hợp chất tạp chức.
Phần III
Thí sinh trả lời từ câu 1 đến câu 6.
Cho các chất sau: tinh bột và cellulose; glucose và fructose; acetic acid và methyl formate; saccharose và maltose. Có bao nhiêu cặp chất là đồng phân của nhau?
Cho biết Li (lithium) là kim loại quan trọng trong các ngành công nghiệp như pin điện, chế tạo các hợp kim,… Kim loại Li được điều chế bằng phương pháp điện phân nóng chảy hỗn hợp LiCl–KCl với tỉ lệ khối lượng tương ứng 3 : 2, ở nhiệt độ 425–500 °C. Hiệu suất điện phân đạt 75 %. Tính khối lượng kim loại Li thu được từ 1 tấn hỗn hợp LiCl–KCl ban đầu (làm tròn kết quả đến hàng phần mười).
Cho phương trình hóa học của các phản ứng được đánh số thứ tự từ (1) đến (4) dưới đây: (1)\;H_2NCH(CH_3)COOH + C_2H_5OH ⇔ H_2NCH(CH_3)COOC_2H_5 + H_2O\;(Xúc tác HCl); (2)\;H_2N(CH_2)_2COOH \xrightarrow{t^\circ} [-NH(CH_2)_2CO-]_n + nH_2O; (3)\;\text{Gly–Ala} + 2NaOH → H_2NCH_2COONa + H_2NCH(CH_3)COONa + H_2O; (4)\;\text{Lòng trắng trứng} + CuSO_4\;2\% + NaOH\;30\% → \text{Tạo thành phức chất màu tím đặc trưng}. Gán số thứ tự phương trình hóa học của các phản ứng theo tên gọi: thủy phân, este hóa, màu biuret, trứng ngưng và sắp xếp theo thứ tự thành dãy số (ví dụ: 1234, 4321, …).
Khi bảo quản trong phòng thí nghiệm, muối Mohr FeSO_4\cdot(NH_4)_2SO_4\cdot6H_2O hút ẩm và bị oxi hóa một phần bởi O_2 trong không khí thành hỗn hợp X. Để xác định phần trăm khối lượng muối Mohr trong X, tiến hành thí nghiệm theo các bước sau:
Bước 1: Cân chính xác 3,0\;\mathrm{gam} X, cho vào bình định mức 100\;\mathrm{mL}, thêm nước cất và khuấy tan, thêm tiếp nước cất đến vạch, thu được 100\;\mathrm{mL} dung dịch Y.
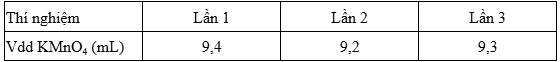
Bước 2: Lấy 10,00\;\mathrm{mL} dung dịch Y cho vào bình tam giác, thêm 5\;\mathrm{mL} H_2SO_4\;(1M); chuẩn độ bằng dung dịch KMnO_4\;(0,015M) đến điểm tương đương (màu tím nhạt bền trong 20\;\mathrm{s}). Lặp lại 2 lần nữa. Kết quả thể tích KMnO_4\;(0,015M) được ghi ở bảng dưới. Phần trăm khối lượng muối Mohr trong X là a\%. Tính a (làm tròn đến hàng phần mười).
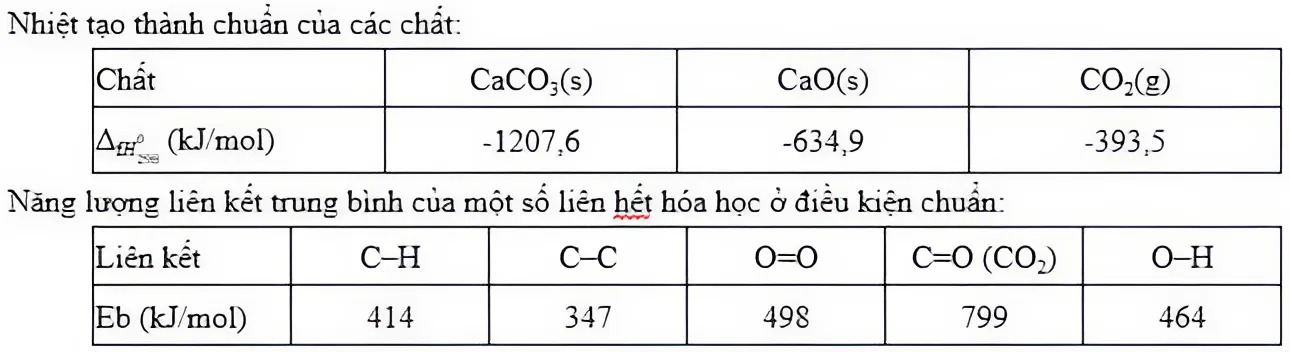
Sản phẩm của quá trình nung vôi có nhiều ứng dụng trong thực tế, CaO sinh ra được sử dụng trong công nghiệp luyện kim và làm nguyên liệu cho công nghiệp hóa học, được dùng để khử chua đất trồng trọt, xử lí nước thải công nghiệp, khử độc môi trường. Còn CO_2 được dùng sản xuất CO_2 lỏng phục vụ cho nhu cầu công nghiệp và dân sinh. Quá trình nung vôi xảy ra theo phương trình hóa học (1)\;CaCO_3(s) → CaO(s) + CO_2(g). Phản ứng (1) là phản ứng thu nhiệt mạnh. Lượng nhiệt này được cung cấp từ quá trình đốt cháy hoàn toàn khí thiên nhiên hóa lỏng (chứa 96\% methane, 4\% ethane về thể tích) theo phương trình hóa học (2)\;CH_4(g) + 2O_2(g) → CO_2(g) + 2H_2O(g) (3)\;C_2H_6(g) + 3,5O_2(g) → 2CO_2(g) + 3H_2O(g). Xét các phản ứng ở điều kiện chuẩn và hiệu suất chuyển hóa của CaO là 100\%. Khối lượng khí thiên nhiên hóa lỏng là m tấn cần thiết để sản xuất 280\;\mathrm{tấn} CaO(s) trong giai đoạn trên. Biết 95\% tổng lượng nhiệt tỏa ra từ phản ứng (2) và (3) được cung cấp cho phản ứng (1) và các giá trị nhiệt tạo thành của các chất, năng lượng liên kết trung bình của một số liên kết hóa học ở điều kiện chuẩn được cho trong bảng sau. Giá trị của m (theo tấn) là bao nhiêu (làm tròn đến hàng phần mười)?
Xà phòng hóa hoàn toàn triglyceride X trong dung dịch \mathrm{NaOH} (vừa đủ), thu được sodium oleate và sodium palmitate theo tỉ lệ mol tương ứng 1:2. Phân tử khối của X là bao nhiêu?
Xem đáp án và bài mẫu
Answer key
Biết X là một amine bậc 3 có phân tử khối bằng 59. Tên gọi của X là:
Propylamine.
N-Methylethanamine.
Triethylamine.
Trimethylamine.
Giải thích câu 1
Giải thích chi tiết
😎 Cùng DOL xem qua cách giải câu này nhé!
📃 Thông tin đề bài cho:
X là một amine bậc 3.
Phân tử khối của X bằng 59.
❓ Hiểu câu hỏi:
Đề yêu cầu tìm tên gọi của X, một amine bậc 3 (tức có 3 nhóm alkyl liên kết với nitơ).
Phân tử khối biết trước để xác định công thức phân tử phù hợp.
Cần vận dụng cách tính khối lượng phân tử và phân loại amine theo bậc.
🔎 Hướng dẫn cách làm:
Amine bậc 3 có công thức tổng quát \mathrm{N}(\mathrm{R_1})(\mathrm{R_2})(\mathrm{R_3}), không có nguyên tử H nào liên kết trực tiếp với N.
Khối lượng nguyên tử cơ bản: \mathrm{C}=12,\;\mathrm{H}=1,\;\mathrm{N}=14.
Tính khối lượng phân tử cho các ứng viên:
Trimethylamine \mathrm{N}(\mathrm{CH_3})_3: M = 14 + 3 \times (12 + 3 \times 1) = 14 + 3 \times 15 = 59 → thỏa yêu cầu cả bậc và khối lượng.
Triethylamine \mathrm{N}(\mathrm{C_2H_5})_3: M = 14 + 3 \times (2\times12 + 5\times1) = 14 + 3 \times 29 = 101 → không bằng 59.
✅ Đáp án: Trimethylamine
❌ Các đáp án khác:
Propylamine: là amine bậc 1, không đáp ứng điều kiện bậc.
N-Methylethanamine: amine bậc 2, không đúng.
Triethylamine: mặc dù là amine bậc 3 nhưng có khối lượng phân tử 101, không khớp 59.
Hiện bạn đang luyện đề THPTQG Môn Hoá thuộc chuyên mục luyện thi THPT Quốc gia. Để tiếp tục rèn luyện với nhiều đề thi khác, bạn học có thể tham khảo các đề liên quan trực tiếp khác dưới đây.


