Đáp án & giải thích đề môn Hoá k12
Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh TP.HCM 2025 - Đề 04

DOL THPT
Mar 27, 2026
Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh TP.HCM 2025 - Đề 04 được thiết kế dưới dạng thi thử trắc nghiệm online, giúp người học làm quen cấu trúc đề thi. Nền tảng chấm điểm ngay sau khi bạn nộp bài, đồng thời lưu lại lịch sử làm bài để bạn tiện theo dõi quá trình ôn luyện, đi kèm đáp án giải thích chi tiết và download PDF đề thi miễn phí HOÀN TOÀN MIỄN PHÍ.

Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh TP.HCM 2025 - Đề 04
Download PDF
Miễn phí dowload
Câu hỏi đề bài
28 Câu hỏi
Phần I
Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Điện phân nóng chảy potassium chloride với các điện cực trơ để điều chế kim loại potassium (K). Quá trình xảy ra ở cathode là:
Oxi hóa ion K⁺.
Khử ion Cl⁻.
Khử ion K⁺.
Oxi hóa ion Cl⁻.
Hoá chất nào sau đây làm mềm được nước cứng vĩnh cửu?
NaCl.
Na₂SO₄.
Na₂CO₃.
HCl.
Trong công nghiệp thực phẩm, để tạo hương dứa cho bánh kẹo người ta dùng ester X có công thức cấu tạo CH_3CH_2COOC_2H_5. Tên gọi của X là:
methyl propionate.
ethyl propionate.
methyl acetate.
propyl acetate.
Tính bột chứa hỗn hợp chất nào sau đây?
Glucose và fructose.
Amylose và amylopectin.
Glucose và galactose.
Amylose và cellulose.
Có thể dùng tối đa bao nhiêu cách trong các cách sau đây để dập tắt đám cháy xăng dầu? (a) Dùng chăn thấm ướt; (b) Dùng cát; (c) Dùng bình carbon dioxide; (d) Dùng nước; (e) Dùng bình chữa cháy dạng bọt.
2
4
5
3
Thí nghiệm nào sau đây thu được kết tủa sau phản ứng?
TN₁: Cho vào ống nghiệm (1) 1 ml ethylamine 5%, thêm 0,5–1 ml HCl 5%. Vừa thêm vừa lắc.
TN₂: Cho vào ống nghiệm (2) 5 giọt FeCl₃ 3%, thêm đến hết 2 ml ethylamine 5%, vừa thêm vừa lắc.
TN₃: Cho vào ống nghiệm (3) 5 giọt CuSO₄ 5%, thêm đến hết 4 ml ethylamine 5%, vừa thêm vừa lắc.
TN₄: Cho vào ống nghiệm (4) 1 ml benzylamine, thêm 0,5–1 ml nước bromine, vừa thêm vừa lắc.
Một mẫu nước được thử nghiệm định tính để xác định sự có mặt của một số ion. Ghi nhận hiện tượng như bảng. mẫu nước trên có thể chứa những ion nào trong số các ion sau đây: (1) H⁺; (2) Ca²⁺; (3) Cl⁻; (4) HCO₃⁻; (5) CO₃²⁻

(1), (2), (3)
(3), (4), (5)
(2), (3), (5)
(2), (3), (4)
Phát biểu nào sau đây sai khi nói về enzyme?
Phần lớn enzyme là những protein xúc tác cho các phản ứng hóa học và sinh hóa.
Tốc độ phản ứng có xúc tác enzyme thường nhanh hơn nhiều lần so với với xúc tác hóa học.
Tốc độ phản ứng có xúc tác enzyme thường chậm hơn nhiều lần so với với xúc tác hóa học.
Enzyme có tính chọn lọc cao, mỗi enzyme chỉ xúc tác cho một hoặc một số phản ứng nhất định.
Nguyên tử nguyên tố R có số electron là 25, vị trí của R trong bảng tuần hoàn là:
Chu kì 4, phân nhóm VIIA.
Chu kì 4, phân nhóm VIIB.
Chu kì 4, phân nhóm VB.
Chu kì 4, phân nhóm IIA.
Độ tan trong nước của các hydroxide nhóm IIA ở 20°C theo bảng. Phát biểu nào sau đây là sai?

Mức độ phản ứng với nước của kim loại nhóm IIA có xu hướng tăng dần từ Be tới Ba.
Độ tan của các hydroxide nhóm IIA tăng dần từ Be(OH)₂ tới Ba(OH)₂.
Các kim loại nhóm IIA đều phản ứng mãnh liệt với nước ở 20°C theo phản ứng: M + 2H₂O → M(OH)₂ + H₂.
Ba(OH)₂ có độ tan lớn nhất nên dễ tách khỏi bề mặt kim loại, do đó Ba sẽ phản ứng với nước ngay điều kiện thường.
Cho phản ứng hóa học: Fe + CuSO_4 → FeSO_4 + Cu. Trong phản ứng trên xảy ra:
Sự oxi hóa Fe và sự khử Cu²⁺.
Sự khử Fe²⁺ và sự khử Cu²⁺.
Sự oxi hóa Fe và sự oxi hóa Cu.
Sự khử Fe và sự oxi hóa Cu.
Trong điều trị bệnh, sodium hydrogencarbonate còn được gọi là sodium bicarbonate được sử dụng dạng viên uống hoặc dung dịch truyền tĩnh mạch. Công thức của sodium hydrogencarbonate là:
NaHCO_3
Na_2CO_3
NaHSO_4
Na_2SO_4
Cho các phát biểu sau: (1) Tơ viscose, tơ acetate đều thuộc loại tơ tổng hợp. (2) Polyethylene và poly(vinyl chloride) là sản phẩm của phản ứng trùng hợp. (3) Tơ nylon-6,6 được điều chế từ hexamethylenediamine và stearic acid. (4) Cao su thiên nhiên không tan trong nước cũng như trong xăng, benzene. (5) Tơ nitron (olon) được trùng hợp từ vinyl cyanide (acrylonitrile). Số phát biểu đúng là:
1
3
5
2
Đặt hỗn hợp các amino acid gồm lysine, glycine và glutamic acid ở pH = 6,0 vào trong một điện trường thấy sự di chuyển như hình vẽ sau: Cho các phát biểu sau:
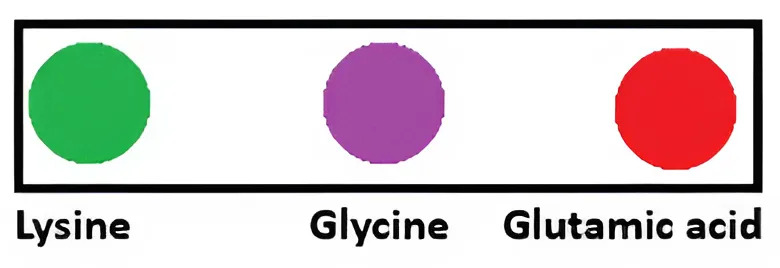
Glycine hầu như không dịch chuyển
Lysine dịch chuyển về phía cực âm
Glutamic acid dịch chuyển về phía cực dương
Cả 3 amino acid đều không di chuyển
Acquy chì là một loại acquy đơn giản, gồm bản cực dương bằng PbO2, bản cực âm bằng Pb, cả hai điện cực được đặt vào dung dịch H2SO4 loãng. Loại acquy này có thể sạc lại nhiều lần. Đây cũng là loại acquy được sử dụng phổ biến trên các dòng xe máy hiện nay với nhiều ưu điểm vượt trội. Acquy chì có các đặc điểm sau: (1) dễ sản xuất, giá thành thấp; (2) gây ô nhiễm môi trường; (3) có khả năng trữ một lượng điện lớn trong bình ắc quy; (4) hoạt động tương đối ổn định. Những ưu điểm của acquy chì là
(1), (2), (3)
(1), (3), (4)
(1), (2), (4)
(2), (3), (4)
Cho các cặp oxi hoá-khử của kim loại và thế điện cực chuẩn tương ứng như bảng. Số kim loại tác dụng với dung dịch HCl ở điều kiện chuẩn, giải phóng khí H_2 là:

2
1
4
3
Giá trị thế điện cực chuẩn của một số cặp oxi hoá - khử được xếp theo thứ tự tăng dần như sau: Fe^{2+}/Fe, Cu^{2+}/Cu, Fe^{3+}/Fe^{2+}, Ag^+/Ag, Cl_2/2Cl^-. Trong các chất: Cu, AgNO_3, Cl_2, chất tác dụng được với dung dịch Fe(NO₃)_3 là:
chỉ có AgNO_3
AgNO_3 và Cl_2
chỉ có Cu
chỉ có Cl_2
Cho các phương trình hoá học đúng theo tỉ lệ mol sau: (1) X + 2NaOH \rightarrow X_1 + X_2 + H_2O (2) X_1 + H_2SO_4 \rightarrow X_3 + Na_2SO_4 (3) nX_3 + nY \rightarrow \text{Poly(ethylene terephthalate)} + 2nH_2O (4) nX_3 + nZ \rightarrow \text{nylon-6,6} + 2nH_2O Phần trăm số nguyên tử oxygen trong X gần nhất với giá trị nào sau đây?
42,1%
36,78%
33,33%
38,1%
Phần II
Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Ở 25°C, nhúng một thanh Zn vào cốc đựng dung dịch ZnSO_4 1M, nhúng một thanh Cu vào cốc đựng dung dịch CuSO_4 1M. Nối thanh Zn và thanh Cu bằng dây dẫn, lắp một vôn kế để đo hiệu điện thế. Đóng kín mạch bằng cầu muối chứa dung dịch bão hoà KNO_3. Biết E^\circ_{Zn^{2+}/Zn} = -0,672\ V
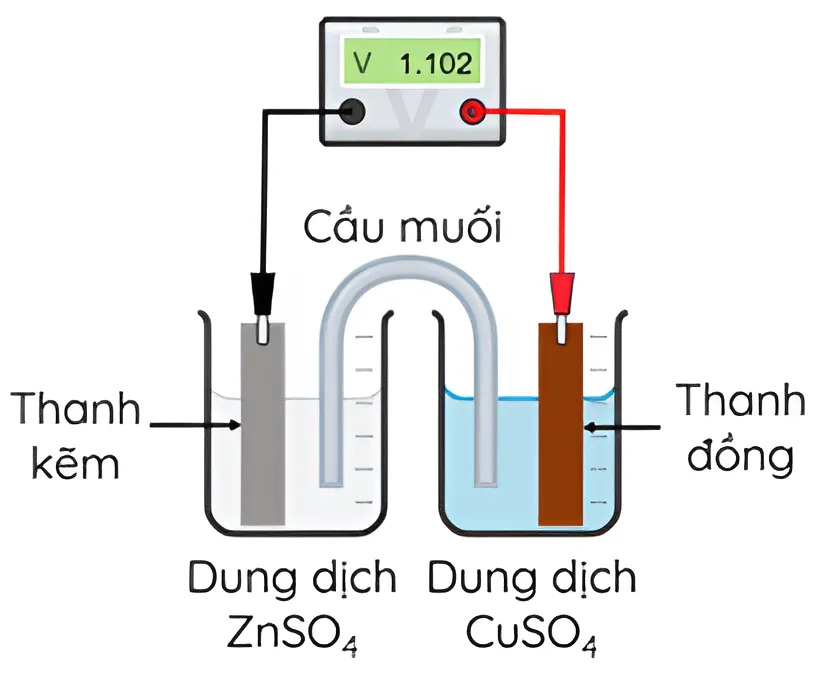
Phát biểu
Đúng
Sai
a
Tại cathode xảy ra quá trình oxi hoá: Cu \rightarrow Cu^{2+} + 2e
b
Khi pin hoạt động, electron theo dây dẫn đi từ thanh Zn sang thanh Cu
c
Thế điện cực chuẩn của Cu^{2+}/Cu là 1,774 V
d
Trong pin hoạt động, cation di chuyển từ bình ZnSO₄ sang CuSO₄ qua cầu muối; anion di chuyển ngược lại
Phân tích nguyên tố hợp chất hữu cơ E cho biết % khối lượng: C = 54,55%; H = 9,09%; O = 36,36%. Dựa vào phương pháp phân tích khối phổ (MS) xác định được phân tử khối của E là 88. Thuỷ phân hoàn toàn E trong dung dịch NaOH, thu được muối của carboxylic acid X và chất Y. Chất Y có nhiệt độ sôi 64,7°C < ethanol 78,3°C (nhiệt độ sôi đều đo ở áp suất 1 atm).
Phát biểu
Đúng
Sai
a
Công thức phân tử của E là C_4H_8O_2
b
Carboxylic acid X là propanoic acid
c
Chất Y được phối trộn với xăng RON 92 để tạo ra xăng sinh học
d
Chất E không thể được điều chế trực tiếp bằng phản ứng ester hoá
Trong phòng thí nghiệm, một nhóm học sinh tìm hiểu phản ứng giữa kim loại đồng (copper) và dung dịch silver nitrate (AgNO_3). Giả thuyết của nhóm học sinh là “khi nhúng lá đồng trong dung dịch silver nitrate, lá đồng tan bớt, có kim loại bạc (silver) bám trên lá đồng”. Để kiểm tra giả thuyết này, nhóm học sinh đã thực hiện thí nghiệm như sau:
Cân một lá đồng, xác định được khối lượng là đồng ban đầu là 5,24 gam.
Nhúng lá đồng vừa cân được vào dung dịch silver nitrate.
Sau một thời gian lấy lá đồng ra, làm khô, cân lại thấy khối lượng lá đồng là 5,39 gam.
Phát biểu
Đúng
Sai
a
Đã có 0,15 gam kim loại bạc bám trên lá đồng
b
Giả thuyết của nhóm học sinh là đúng
c
Dung dịch từ không màu chuyển sang màu xanh.
d
Thí nghiệm trên chứng minh tính oxi hóa của ion Ag+ mạnh hơn tính oxi hóa của ion Cu^{2+}.
Muối Mohr có công thức (NH_4)_2Fe(SO_4)_2.6H_2O. Để xác định độ tinh khiết của một loại muối Mohr (cho rằng trong muối Mohr chỉ có muối kép ngậm nước nêu trên và tạp chất trơ), một học sinh tiến hành các thí nghiệm sau: Cân chính xác 7,237 gam muối Mohr, pha thành 100 mL dung dịch X. Lấy chính xác 10 mL dung dịch X, thêm 10 mL dung dịch H_2SO_4 10%, được dung dịch Y. Chuẩn độ dung dịch Y bằng dung dịch chuẩn KMnO_4 0,023M. Thực hiện chuẩn độ 3 lần. Kết quả đạt được như bảng.

Phát biểu
Đúng
Sai
a
Dùng H_2SO_4 để tạo môi trường acid, giúp phản ứng tạo Mn^{2+}
b
Có thể thay bằng acid mạnh khác như HCl, HNO_3 nếu đảm bảo đủ ion H^+
c
Trong mỗi lần chuẩn độ, KMnO₄ được xem là phản ứng vừa đủ với muối Mohr khi giọt cuối không mất màu
d
Từ số liệu chuẩn độ, độ tinh khiết gần đúng của muối Mohr là 98,45%
Phần III
Thí sinh trả lời từ câu 1 đến câu 6.
Cho các polymer sau: polyethylene, poly(methyl methacrylate), poly(vinyl chloride), polyacrylonitrile. Có bao nhiêu polymer điều chế được bằng phản ứng trùng hợp?
Tiến hành các thí nghiệm: (1) Điện phân MgCl_2 nóng chảy (2) Cho CO qua Fe_2O_3 nung nóng (3) Nhiệt phân hoàn toàn CaCO_3 (4) Cho kim loại Na vào dung dịch CuSO_4 dư (5) Dẫn khí H_2 qua bột CuO nung nóng Sau khi các phản ứng kết thúc, các thí nghiệm thu được kim loại được sắp xếp theo trình tự từ nhỏ đến lớn là bao nhiêu?
Từ 500 tấn quặng hematite chứa 85% Fe_2O_3, sản xuất được x nghìn chiếc nồi gang 5 kg chứa 95% Fe. Biết rằng mỗi chiếc nồi gang nặng 5 kg và hiệu suất của toàn bộ quá trình là 80%. Giá trị của x là bao nhiêu (kết quả làm tròn đến chữ số hàng đơn vị)?
Thành phần chủ yếu của xà phòng thường là muối sodium của palmitic acid hoặc stearic acid. Ngoài ra, trong xà phòng còn có chất độn (làm tăng độ cứng để đúc thành bánh), chất tẩy màu, chất diệt khuẩn và chất tạo hương,.Từ 3,5 tấn chất béo chứa 80% khối lượng tristearin (còn 20% tạp chất trơ bị loại bỏ trong quá trình nấu xà phòng) để sản xuất được m tấn xà phòng chứa 70% khối lượng sodium stearate. Giả sử hiệu suất toàn bộ quá trình là 90%. Giá trị của m bằng bao nhiêu tấn (kết quả làm tròn đến chữ số hàng phần trăm)?
Độ tan của Ca(OH)_2 trong nước ở 25°C là 0,17 gam/100 gam nước. Dung dịch bão hòa Ca(OH)_2 có khối lượng riêng là 1,02 g/mL. Giá trị pH của dung dịch Ca(OH)_2 bão hòa bằng bao nhiêu (kết quả làm tròn đến chữ số hàng phần mười)?
Thực hiện các thí nghiệm sau:
Thí nghiệm 1: Rót khoảng 2 mL dung dịch HCl vào ống nghiệm có một viên Zn sạch.
Thí nghiệm 2: Rót khoảng 2 mL dung dịch HCl vào ống nghiệm có một viên Zn sạch, sau đó thêm vài giọt dung dịch CuSO_4.
Thí nghiệm 3: Rót khoảng 2 mL dung dịch HCl vào ống nghiệm có một mẩu dây đồng.
Thí nghiệm 4: Rót khoảng 2 mL dung dịch HCl vào ống nghiệm có một viên Zn và một mẩu dây Cu tiếp xúc với nhau. Số thí nghiệm xuất hiện ăn mòn điện hóa học trong 4 thí nghiệm trên?
Xem đáp án và bài mẫu
Answer key
Điện phân nóng chảy potassium chloride với các điện cực trơ để điều chế kim loại potassium (K). Quá trình xảy ra ở cathode là:
Oxi hóa ion K⁺.
Khử ion Cl⁻.
Khử ion K⁺.
Oxi hóa ion Cl⁻.
Giải thích câu 1
Giải thích chi tiết
😎 Cùng DOL xem qua cách giải câu này nhé!
📃 Thông tin đề bài cho:
Điện phân nóng chảy kali clorua (KCl)
Sử dụng điện cực trơ (không tác dụng với các sản phẩm điện phân)
Mục đích: điều chế kim loại potassium (K)
Câu hỏi: Quá trình xảy ra tại cathode là gì?
❓ Hiểu câu hỏi:
Xác định khái niệm cathode: nơi xảy ra sự khử trong quá trình điện phân.
Xác định các ion có trong dung dịch nóng chảy: K^+ và Cl^-.
Biết quy tắc: tại cathode, ion nhận electron (e⁻) → khử; tại anode, ion nhường electron → oxi hoá.
🔎 Hướng dẫn cách làm:
Quan sát hình minh hoạ: bình điện phân chứa KCl nóng chảy với hai điện cực trơ.
Ghi nhớ:
Cathode (cực âm) thu hút ion dương (K^+), nơi xảy ra quá trình khử.
Anode (cực dương) thu hút ion âm (Cl^-), nơi xảy ra quá trình oxi hoá.
Viết nửa phản ứng tại cathode:
K^+ + e^- \longrightarrow K\,(l)Đây là quá trình khử ion K^+.
Như vậy, quá trình chính xác tại cathode là khử ion K⁺.
✅ Đáp án: \text{Khử ion }K^+
❌ Các đáp án khác:
A. Oxi hóa ion K⁺: sai vì tại cathode xảy ra khử, không oxi hóa.
B. Khử ion Cl⁻: sai vì ion Cl⁻ bị oxi hóa tại anode chứ không bị khử tại cathode.
D. Oxi hóa ion Cl⁻: là quá trình đúng tại anode, nhưng câu hỏi hỏi về cathode.
Hiện bạn đang luyện đề THPTQG Môn Hoá thuộc chuyên mục luyện thi THPT Quốc gia. Để tiếp tục rèn luyện với nhiều đề thi khác, bạn có thể luyện tập thêm các đề liên quan khác dưới đây.


