Đáp án & giải thích đề môn Hoá k12
Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Tây Ninh 2025

DOL THPT
Mar 27, 2026
Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Tây Ninh 2025 được xây dựng dưới dạng thi thử trắc nghiệm online, giúp người học nắm rõ bố cục đề thi. Hệ thống chấm điểm ngay sau khi bạn hoàn thành bài thi, đồng thời lưu quá trình làm bài để bạn theo dõi hiệu quả quá trình ôn luyện, đi kèm lời giải chi tiết, dễ hiểu và tải file PDF đề thi HOÀN TOÀN MIỄN PHÍ.

Đề thi thử tốt nghiệp THPT môn Hóa Học tỉnh Tây Ninh 2025
Download PDF
Miễn phí dowload
Câu hỏi đề bài
28 Câu hỏi
Phần I
Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Cho bảng giá trị thế điện cực chuẩn của các cặp oxi hoá – khử như sau:... Pin Galvani X được thiết lập từ hai trong số các cặp oxi hoá – khử trên có sức điện động chuẩn là 2{,}475\,V. Pin Galvani X là pin gì?
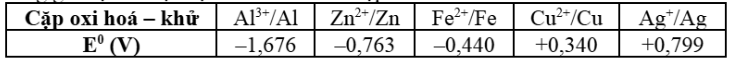
Fe-Cu.
Fe-Ag.
Al-Zn.
Al-Ag.
Trong pin điện hoá, quá trình oxi hoá
chỉ xảy ra ở cực dương.
xảy ra ở cả hai cực.
chỉ xảy ra ở cực âm.
không xảy ra ở cả hai cực.
Peptide nào sau đây không có phản ứng màu biuret?
Gly-Ala-Gly.
Ala-Ala-Gly-Gly.
Ala-Gly.
Ala-Gly-Gly.
Chất nào sau đây được dùng làm chất giặt rửa tổng hợp?
C_{15}H_{31}COONa
CH_{3}[CH_{2}]_{11}–C_{6}H_{4}–SO_{3}Na
C_{17}H_{35}COONa
CH_{3}–C_{6}H_{4}–ONa
Cho biết số thứ tự của Na trong bảng tuần hoàn là 11. Số electron ở lớp ngoài cùng của nguyên tử Na là
2
1
4
3
Phát biểu nào sau đây không đúng?
Nylon-6,6 thuộc loại tơ tổng hợp.
Thành phần của vật liệu composite chỉ chứa polymer.
Tơ tằm thuộc loại tơ thiên nhiên.
Cao su là những vật liệu polymer có tính đàn hồi.
Polystyrene (PS) là chất nhiệt dẻo... Monomer được dùng để điều chế PS là
C_{6}H_{5}CH=CH_{2}
CH_{2}=CH–CH=CH_{2}
CH_{2}=CH_{2}
CH_{2}=CH–CH_{3}
Dạng tồn tại chủ yếu của alanine trong môi trường acid mạnh (pH = 2) là
NH_{3}^{+}–CH(CH_{3})–COO^{-}
NH_{2}–CH(CH_{3})–COOH
NH_{3}^{+}–CH(CH_{3})–COOH
NH_{2}–CH(CH_{3})–COO^{-}
Số nguyên tử carbon trong 1 phân tử saccharose là
11
12
6
5
Phản ứng chứng tỏ glucose có dạng mạch vòng là phản ứng của glucose với
Cu(OH)_{2}
nước bromine
CH_{3}OH (xúc tác HCl)
dung dịch [Ag(NH_{3})_{2}]OH, t^{o}
Nguyên tắc tách kim loại là
oxi hoá ion kim loại thành nguyên tử.
thử ion kim loại thành nguyên tử.
oxi hoá nguyên tử kim loại thành ion.
khử nguyên tử kim loại thành ion.
Khi đun nóng chất X có công thức phân tử C_{3}H_{6}O_{2} với NaOH thu được CH_{3}COONa. Công thức cấu tạo của X là
CH_{3}COOC_{2}H_{5}
HCOOC_{2}H_{5}
C_{2}H_{5}COOH
CH_{3}COOCH_{3}
Dựa vào bảng thế điện cực chuẩn, kim loại có tính khử mạnh nhất là

Cu.
Fe.
Ag.
Al.
Ở nhiệt độ cao, CO khử được oxide nào sau đây?
Fe_{2}O_{3}
K_{2}O
CaO
Na_{2}O
Polymer nào sau đây không chứa nguyên tố nitrogen?
Polycaproamide.
Poly(hexamethylene adipamide).
Polyacrylonitrile.
Polyethylene.
Chất X có công thức cấu tạo CH_{3}–NH–C_{2}H_{5}. Tên gọi của X là
propylamine.
methylamine.
dimethylamine.
ethylmethylamine.
Phương pháp nào dưới đây được dùng để sản xuất bơ nhân tạo?
Hydrogen hóa acid béo không no.
Xà phòng hóa chất béo lỏng.
Trung hoà acid béo không no.
Hydrogen hóa chất béo lỏng.
Trong phân tử amylose, các gốc ...(1)... liên kết với nhau bằng liên kết ...(2)... Các cụm từ thích hợp là
β-glucose; β-1,6-glycoside.
β-glucose; β-1,4-glycoside.
α-glucose; α-1,4-glycoside.
α-glucose; α-1,6-glycoside.
Phần II
Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Một nhóm học sinh tiến hành thí nghiệm mạ đồng (copper) lên chiếc thìa kim loại. Giả thuyết được nhóm học sinh đưa ra là: “Nồng độ CuSO_4 trước và sau quá trình mạ là không đổi”. Để kiểm chứng giả thuyết, nhóm học sinh tiến hành quá trình mạ theo các bước như sau:
Bước 1: Cân để xác định khối lượng ban đầu của chiếc thìa là 10 gam và của thanh đồng nguyên chất là 15 gam.
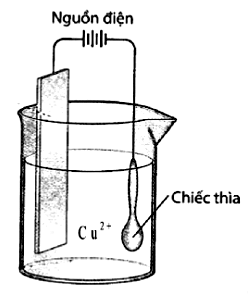
Bước 2: Nối chiếc thìa với 1 điện cực và thanh đồng với điện cực còn lại của nguồn điện một chiều rồi nhúng vào cốc chứa dung dịch CuSO_4 để tiến hành mạ với hiệu điện thế thích hợp (như hình vẽ):
Bước 3: Sau thời gian 15 phút điện phân, lấy chiếc thìa và thanh đồng ra khỏi cốc, làm khô cẩn thận, đem cân thì thấy khối lượng của chiếc thìa là 10,32 gam, của thanh đồng là 14,68 gam. Biết hiệu suất của quá trình đạt 100%.
Phát biểu
Đúng
Sai
a
Tại anode xảy ra quá trình khử ion Cu^{2+}, tại cathode xảy ra quá trình oxi hoá Cu.
b
Sau khi mạ xong, độ giảm khối lượng của thanh đồng bằng độ tăng khối lượng của chiếc thìa.
c
Do khối lượng của thanh đồng giảm nên giả thuyết ban đầu của nhóm học sinh là sai.
d
Thanh đồng được nối với cực dương, chiếc thìa được nối với cực âm của nguồn điện.
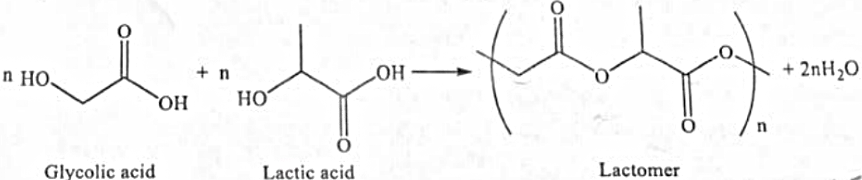
Lactomer là một loại polymer phân hủy sinh học, được ứng dụng nhiều trong ngành y tế. Lactomer có khả năng phân hủy một cách tự nhiên trong cơ thể mà không gây tác dụng phụ nên được sử dụng để sản xuất chỉ khâu tự tiêu. Loại chỉ khâu này có thể tan và phân hủy từ từ trong cơ thể tạo thành glycolic acid, lactic acid rồi bị đào thải nhờ các quá trình sinh hoá. Sau khoảng 2 tuần thì chỉ khâu hoàn thành nhiệm vụ của nó, lúc này các mô tổn thương đã kịp lành. Lactomer được tạo ra từ lactic acid và glycolic acid theo phương trình hoá học:
Phát biểu
Đúng
Sai
a
Glycolic acid và lactic acid đều thuộc loại carboxylic acid no, đơn chức.
b
Lactomer bị phân huỷ là do sự thuỷ phân các nhóm chức ester trong phân tử.
c
Phản ứng điều chế lactomer là phản ứng trùng hợp.
d
Mỗi mắt xích trong lactomer có 5 nguyên tử carbon.
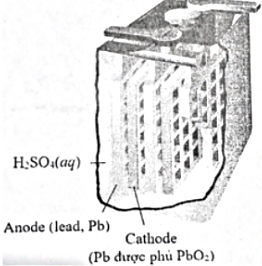
Ắc quy chì (Lead-acid Battery) là nguồn điện thông dụng, tạo ra dòng điện ổn định và đặc biệt có thể tái sử dụng. Cấu tạo của ắc quy chì như hình. Khi ắc quy phóng điện, quá trình xảy ra tại các điện cực như sau: Anode: Pb + HSO_4^{-} \rightarrow PbSO_4 + H^{+} + 2e. Cathode: PbO_2 + HSO_4^{-} + 3H^{+} + 2e \rightarrow PbSO_4 + 2H_2O. Khác với pin Galvani, ắc quy có thể tái sử dụng bằng cách áp dòng điện bên ngoài để các phản ứng ở điện cực xảy ra theo chiều ngược với khi phóng điện (gọi là quá trình nạp điện hay tích điện)
Phát biểu
Đúng
Sai
a
Khi nạp điện, ắc quy đóng vai trò như bình điện phân.
b
Khi ắc quy phóng điện cũng như nạp điện, nồng độ H_2SO_4 không đổi.
c
Khi ắc quy phóng điện, tại anode xảy ra quá trình oxi hoá chì.
d
Khi ắc quy phóng điện, tại cathode xảy ra quá trình khử PbO_2.
Quặng vàng (Gold) tồn tại trong tự nhiên thường có hàm lượng vàng thấp. Phương pháp tách vàng phù hợp hiện nay là phương pháp Cyanide. Theo phương pháp này, để thu hồi vàng từ quặng, người ta thường nghiền nhỏ quặng rồi hoà tan trong dung dịch KCN (potassium cyanide, rất độc) cùng với dòng không khí liên tục được thổi vào. Khi đó, vàng bị hoà tan tạo thành phức chất (các chất khác trong quặng không phản ứng với KCN): 4Au + 8KCN + O_2 + 2H_2O \rightarrow 4K[Au(CN)_2] + 4KOH (1). Tiếp theo cho bột kẽm đến dư vào dung dịch phức, thu được bột vàng (có lẫn một ít bột kẽm): Zn + 2K[Au(CN)_2] \rightarrow K_2[Zn(CN)_4] + 2Au (2)
Phát biểu
Đúng
Sai
a
Phương pháp tách vàng ở trên thân thiện với môi trường.
b
Phương pháp tách vàng ở trên là phương pháp thuỷ luyện.
c
Để loại bỏ Zn lẫn trong bột vàng, có thể dùng dung dịch HCl.
d
Để thu được 37,5 gam vàng cần 23,5 gam KCN (hiệu suất cả quá trình tách đạt 95%). Biết nguyên tử khối: C = 12; N = 14; K = 39; Au = 197.
Phần III
Thí sinh trả lời từ câu 1 đến câu 6.
Cho các phản ứng sau: (1) Mg^{2+}(aq) + Pb(s) \rightarrow Pb^{2+}(aq) + Mg(s); (2) 2H^{+}(aq) + Zn(s) \rightarrow Zn^{2+}(aq) + H_2(g); (3) Ni(s) + Pb^{2+}(aq) \rightarrow Ni^{2+}(aq) + Pb(s); (4) Fe(s) + Mn^{2+}(aq) \rightarrow Fe^{2+}(aq) + Mn(s). Biết E^\circ_{Mg^{2+}/Mg} = -2{,}356V, E^\circ_{Zn^{2+}/Zn} = -0{,}763V, E^\circ_{Fe^{2+}/Fe} = -0{,}440V, E^\circ_{Ni^{2+}/Ni} = -0{,}257V, E^\circ_{Pb^{2+}/Pb} = -0{,}126V, E^\circ_{H^{+}/H_2} = 0{,}000V. Liệt kê các phản ứng xảy ra ở điều kiện chuẩn theo thứ tự tăng dần số.
Cho các tính chất sau: tính dẻo, tính cứng, tính dẫn điện, ánh kim, khối lượng riêng. Có bao nhiêu tính chất vật lí chung của kim loại trong các tính chất trên?
Quặng sắt là khoáng vật chứa các hợp chất của sắt chủ yếu ở dạng các oxide. Hematite là một loại quặng chứa hàm lượng sắt cao và được dùng để sản xuất gang bằng cách nạp trực tiếp vào lò cao. Từ 100 tấn quặng hematite có thể sản xuất được bao nhiêu tấn gang chứa 96% Fe về khối lượng? Giả thiết quặng hematite chứa 69,9% Fe về khối lượng và có 90% lượng Fe trong quặng chuyển vào gang. (Kết quả làm tròn đến hàng phần mười)
Chất béo là nguồn cung cấp năng lượng đáng kể cho cơ thể. Trung bình 1 gam chất béo cung cấp 37,7 kJ. Mỗi ngày, một học sinh trung học phổ thông cần cung cấp 10000 kJ (trong đó năng lượng từ chất béo đóng góp 20%) thì học sinh đó phải ăn bao nhiêu gam chất béo cho phù hợp? (Kết quả làm tròn đến hàng đơn vị)
Thuỷ phân không hoàn toàn peptide: Gly-Ala-Lys-Val-Lys trong điều kiện thích hợp, có thể thu được tối đa bao nhiêu tripeptide?
Nhỏ dung dịch của mỗi chất: glycine, ethylamine, aniline, lysine, glutamic acid vào giấy quỳ tím. Có bao nhiêu dung dịch làm quỳ tím chuyển xanh?
Xem đáp án và bài mẫu
Answer key
Cho bảng giá trị thế điện cực chuẩn của các cặp oxi hoá – khử như sau:... Pin Galvani X được thiết lập từ hai trong số các cặp oxi hoá – khử trên có sức điện động chuẩn là 2{,}475\,V. Pin Galvani X là pin gì?
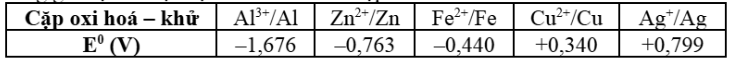
Fe-Cu.
Fe-Ag.
Al-Zn.
Al-Ag.
Giải thích câu 1
Giải thích chi tiết
😎 Cùng DOL xem qua cách giải câu này nhé!
📃 Thông tin đề bài cho:
Bảng giá trị thế điện cực chuẩn E° (V) của các cặp oxi hoá – khử từ ảnh đính kèm: • Al³⁺/Al: –1,676 • Zn²⁺/Zn: –0,763 • Fe²⁺/Fe: –0,440 • Cu²⁺/Cu: +0,340 • Ag⁺/Ag: +0,799
Pin Galvani X được ghép từ hai trong số các cặp trên.
Suất điện động chuẩn của pin X là 2{,}475\,\text{V}.
Các phương án trả lời ứng với các kiểu pin: Fe-Cu; Fe-Ag; Al-Zn; Al-Ag.
❓ Hiểu câu hỏi:
Xác định cặp oxi hoá – khử khi ghép lại cho suất điện động chuẩn E^\circ_\text{cell}=2{,}475\,\text{V}.
Áp dụng công thức tính suất điện động pin: E^\circ_\text{cell} = E^\circ_\text{cathode} - E^\circ_\text{anode}.
Chọn anode (bị oxi hoá) là cặp có E° nhỏ hơn, cathode (bị khử) là cặp có E° lớn hơn.
🔎 Hướng dẫn cách làm:
Ghi công thức chung: E^\circ_\text{cell} = E^\circ_\text{cathode} - E^\circ_\text{anode}.
Xác định thứ tự theo E° từ thấp đến cao: Al³⁺/Al < Zn²⁺/Zn < Fe²⁺/Fe < Cu²⁺/Cu < Ag⁺/Ag.
Tính mỗi trường hợp: • Fe-Cu: 0{,}340 - (-0{,}440) = 0{,}780\,\text{V}. • Fe-Ag: 0{,}799 - (-0{,}440) = 1{,}239\,\text{V}. • Al-Zn: -0{,}763 - (-1{,}676) = 0{,}913\,\text{V}. • Al-Ag: 0{,}799 - (-1{,}676) = 2{,}475\,\text{V}.
Chỉ có cặp Al-Ag cho đúng 2{,}475\,\text{V}.
✅ Đáp án: Al-Ag.
❌ Các đáp án khác:
Fe-Cu: cho 0{,}780\,\text{V}\neq2{,}475\,\text{V}.
Fe-Ag: cho 1{,}239\,\text{V}\neq2{,}475\,\text{V}.
Al-Zn: cho 0{,}913\,\text{V}\neq2{,}475\,\text{V}.
Bạn đang luyện đề THPTQG Môn Hoá thuộc chuyên mục luyện thi THPT Quốc gia. Để tiếp tục với nhiều đề thi khác, bạn học có thể tham khảo những đề thi liên quan khác bên dưới.


